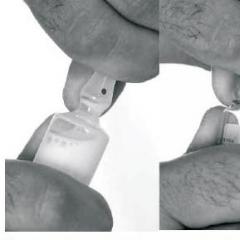
Sinteza krute faze peptida sa zaštitnim skupinama VOS i Fmoc. Struktura sinteze krute faze u krutoj fazi kardioaktivnog peptida
Komunikacija peptida ima svojstva djelomično dvojne komunikacije. To se manifestira u smanjenju duljine ove veze (0,132 nm) u usporedbi s duljinom jednostavne veze s N (0.147 nm). Djelomično Bobbling priroda peptidnih komunikacija čini nemogućom slobodnom rotacijom supstituenata oko nje, tako da je peptidna skupina ravna i obično ima trans-konfiguraciju (F-la i). Da, osovina peptidnog lanca je niz tvrdih zrakoplova s \u200b\u200bpokretnim ("šarkama") artikulacijom na mjestu gdje su asimetrični atomi s (u F-LE-u označeni zvjezdicom).
U peptidnim otopinama postoji poželjna stvaranje određenih konformera. Uz produljenje lanca, dobiva se izraženija stabilnost (slično proteinima) naručenim elementima sekundarne strukture. Formiranje sekundarne strukture posebno je karakteristično za redovite peptide, posebno za poliamin kiseline.
Svojstva
Oligopeptidi po svojstvima su blizu aminokiselina, polipeptidi su slični proteinima. Oligopeptidi su obično kristalne tvari koje se razgrađuju kada se zagrijavaju do 200300 ° C. Oni su dobro topljivi u vodi, razrijeđenim kiselinama i alkalizu, gotovo nisu topljivi u organskim otapalima. Iznimke su oligopeptidi iz hidrofobnih aminokiselinskih ostataka.
Oligopeptidi imaju amfoterična svojstva i, ovisno o kiselosti medija, mogu postojati u obliku kationa, aniona ili iona Zwitter. Glavne apsorpcijske trake u IR spektar za skupinu NH3300 i 3080 cm -1, za skupinu C \u003d o 1660 cm -1. U UV spektrima, apsorpcijski pojas peptidne skupine nalazi se u regiji 180-230 nm. Peptidna izoelektrična točka (PI) uvelike varira i ovisi o sastavu aminokiselinskih ostataka u molekuli. Magnitude RK i peptida su za a-coxy cca. 3, za -h 2 cca. osam.
Kemijska svojstva oligopeptida određena su funkcionalnim skupinama sadržanim u njima, kao i značajke peptida. Njihove kemijske transformacije su u velikoj mjeri slične odgovarajućoj aminokiselinske reakcije. Oni daju pozitivnu reakciju pire i reakcija ningdrin. Dipeptidi i njihovi derivati \u200b\u200b(posebno eteri) se lako cikliziraju, pretvarajući se u diketopiperazine. Pod djelovanjem 5,7 Normalni peptidi klorovodične kiseline hidroliziraju se do aminokiselina tijekom 24 sata na 105 ° C.
Sinteza peptid
Koriste se u sintezi peptida, poznati iz organske kemije reakcije dobivanja amida i posebno razvijenih metoda za sintezu peptida. Uspješno implementirati ove sinteze, potrebno je aktivirati karboksilnu skupinu, tj. Povećati ugljik karbonil. To se postiže kemijskom modifikacijom karboksilne skupine aminokiselina. Vrsta takvog modifikacije obično određuje naziv metode sinteze peptida.
1. Metoda klorhidrida.
Postupak se temelji na reakciji dobivanja amida na interakciju kiselinskog klorida s odgovarajućim aminima. Ova metoda je dobivena prva peptida. Trenutno je ova metoda iznimno rijetka, jer je popraćena formiranjem nusproizvoda i peptida racemik.

2. Metoda azida
Početna tvar u ovoj metodi najčešće je etil eterska n-zaštićena aminokiselina, iz kojeg se dobije hidrazid, potonji se dobije upotrebom natrijevog nitrita u prisutnosti klorovodične kiseline u kiselom azidu. U reakciji se obično koristi hidrazin, u kojem je jedan od nitrava blokiran zaštitnom skupinom (Z-karbobenzoksi ili ugljikohithiteratuclear), koji izbjegava formiranje bočnih dihidrazida. Azidi pri interakciji s aminokiselinama zaštićenih C u blagim uvjetima tvore peptide.
Raceminizacija u ovoj metodi je minimizirana, ali mogu postojati nuspojave, naime: azidi se mogu preurediti u izocijanati, što je zauzvrat, kada je u interakciji s alkoholom koji se koristi kao otapalo, oblika uretana.

3. Mješoviti anhidridi
Miješani anhidridi aminokiselina s derivatima ugljena dobiveni, na primjer, nađeni su široki upotreba u sintezi peptida, dobivene, na primjer, upotrebom izobutilklorikarbonata: 
Reakcija u ovoj sintezi se provodi pri niskoj temperaturi (-10 -20 s), vrlo brzo, što značajno smanjuje mogućnost formiranja nusproizvoda i račemije. Brzna stepena sinteza peptida upotrebom miješanih anhidrida naziva se Rema-sinteza. Metode obrazovanja koristeći miješani anhidridi naširoko se koriste u sintezi krute faze peptida.
Prema tome, sinteza peptida zahtijeva računovodstvo i oštre usklađenost s nekim čimbenicima. Dakle, kako bi se smanjila formiranje nusproizvoda i račemije, preporučuju se sljedeći uvjeti za reakciju formiranja peptidne komunikacije:
1) postupak se mora provesti na niskim temperaturama, vrijeme reakcije mora biti minimalno;
2) reakcijska masa mora imati pH blizu neutralne;
3) Organske baze se koriste kao reagensi za vezanje kiselina kao piperidin, morfolin, itd.;
4) Reakcija je poželjno u bezvodnom mediju.
Sinteza solidne faze
Sinteza solidne faze - Metodički pristup sintezi oligomera (polimera) pomoću krutog netopljivog medijakoji predstavljaju organski ili anorganski polimer.
Početkom šezdesetih godina prošlog stoljeća predložen je novi pristup za rješavanje problema izolacije i pročišćavanja nastajanja u sintezi peptida. Kasnije otvaranjem ovog pristupa, R.B. Merrifield, u njegovom Nobelovom predavanju rekao je kako se to dogodilo: "Jednom sam razmišljao o tome kako je postignut cilj učinkovitije sinteze peptida. Plan je bio skupljati peptidni lanac poštanskog, a tijekom sinteze krug bi trebao biti na jednom kraju vezan za kruti nosač. " Kao rezultat toga, oslobađanje i pročišćavanje srednjih i ciljnih peptidnih derivata je jednostavno reducirana na filtraciju i temeljito pranje krutog polimera za uklanjanje svih viška reagensa i nusproizvoda koji ostaju u otopini. Takav mehanički postupak može se provesti kvantitativno, lako standardizirano i može se čak i automatizirati. Razmotrite ovaj postupak detaljnije.
Sinteza krute faze,
metodich. Pristup sintezi oligo (poli) mjera pomoću krutog netopljivog nosača (N.), koji je težak. ili nooror. polimer. To jest, temelji se na činjenici da je prva veza budućnosti oligomera kovalentno fiksirana na "sidro" skupinu N., nastavak kruga se provodi standardnim monomerima konvencionalnim shemama koji se koriste za sintezu u R-RAX. O izradi. Sintesovska faza. Oligomer se cijepa iz N. i pročišćen je odgovarajućim metodama. T. s. Prijavite se u OSN. Za dobivanje polipeptida, oligo-nukleotida i oligosaharida.
U sintezi polipeptida kao N. NAB. Stiren kopolimer i 1-2% divinil benzena, modificira se primjenom dimetoksibenzil kloridne sidrene skupine za pričvršćivanje prve (s zaštićenom NH2 skupinom) pomoću C-kraja, na primjer:
Nakon uklanjanja N-zaštitne skupine, zgrada polipeptidnog lanca provodi se standardnim metodama sinteze peptida u P-re (vidi. Peptidi). Kao sredstva za kondenziranje je nab. Često se koriste ili pretvaraju aminokiseline u aktiviranje. Eter.
U sintezi oligonukleotida kao N. Koristite makroporne naočale ili. Sidrena skupina služi karboksilnu skupinu odvojenu od N. SPET. "Noga", npr .:

U purinskoj ili pirimidičkoj bazi
U prvoj fazi, nukleozid je pričvršćen na nosač 3 "-hidroksilne deoksiribose skupine, u K-roj, jaka skupina u položaju 5" je zaštićena dimobiotilturnom skupinom (CH3S 6N 4) 2 (C6 h 5) C (dmtr); Broj kasno nakon cijepanja se lako mjeri spektropometrijski, koji služi kao citata. Karakteristika opterećenja nosača i omogućuje vam da procijenite izlaze u narednim fazama produženja oligonukleotidnog lanca. Nakon uklanjanja DMTR skupine, sklop kruga se provodi upotrebom fosfilatidida (F-La I; M. Kapožeri, 1980) ili fosfonata (hidrofosfonati) (II; R. Ryiszgg, 1986):

Za provedbu T. s. Potrebni su visoki prinosi (na razini od 96-99%) u svakoj fazi mirovine, kao i učinkovite metode za čišćenje i naglašavanje sinteze. veze.
Korištenje krute faze omogućuje značajno pojednostavljeno i ubrzati svaku fazu povećanja lanca oligomera, budući da se odvajanje viška komponenti, sredstva za kondenzaciju i nusproizvode smještene u P-RE, filtriraju reakciju , Mješavine i pranje N. Prikladan skup P-Rite-Lei. T. OBR., Proces sastavljanja oligomera lanac se raspada u brojnim standardnim operacijama: oslobađanje rastućeg kraja lanca, doziranje sljedeće zaštićenog monomera i sredstva za kondenziranje, dovod ove smjese na kolonu s n , Za izračunato vrijeme i pranje N. prikladan r-jahač. Ciklus proširenja monomerne jedinice m. B. Automatiziran.
U srcu automatskog. Maturalna večer. Sinhesizers leži s općim shematskim dijagramom (vidi sl.). Brojni Modeli sinteze koja se razlikuju u dizajnu stupaca i njihov broj, metoda hranjenja reagensa i R-Ryteli, itd. Kontrola i programiranje se provode pomoću ugrađenog ili izvedenog računala.

Automatika koncepta. Maturalna večer. sintetizatori (električni. upravljačka linija označena je isprekidana linija): 1-rini opskrbe monomera (m 1, m N.) i sredstva za kondenziranje (KA); 2-line hranjenje reagensa (npr. Oksidirajuća sredstva, sredstva za aciliranje, KT, itd.) I fllers (p 1, r N.); 3 - prebacivanje ventila; 4-stupac s nosačem, opremljen distribucijom. ventil; 5-fotometrijska. ćelija; 6 metara; 7-kontrolna i programska jedinica; 8-zaslon.
Potencijalne značajke o tome dokazuju sintezu A (R. Merryfield, 1969) i ljudski hormon rasta (D. Yamashiro, 1970) s duljinom 124 i 183 aminokiselina, respektivno. Međutim, zbog male, ali konstantne racemikacije koje se događaju u formiranju peptidnih komunikacija, sinteza. Posjeduju nisku biol. Aktivnosti, stoga automatska. Sintezeri se koriste ch. arrant Za dobivanje kratkih polipeptida (10-30 linkova), uključujući i za preparativnu sintezu proteina (1 g).
To jest, predloži se Merryphield (1962) za sintezu polipeptida i uđe u praksu polipeptida, a zatim je sinteza oligonukleotida (R. Letzinger, 1964) i oligosaharidi (A. Pancernik, 1973) uobičajeni.
Postoji još jedan važan aspekt korištenja N. za držanje MN. Org. P-Qii (, halogeniranje, itd.). U ovom slučaju, izmijenjena. N. djeluje kao polimer reagens ili katalizator, a sve transformacije supstrata javljaju se u p-re. Na primjer, ROP (OH) 2 fosfat (OH) 2 fosfati se provodi upotrebom umreženog polistirena, modificirana sulfokloridnom skupinom kao sredstvo za kondenziranje.
Lit: Kemija polipeptida, po. s engleskog, M., 1977; Polirne podržane reakcije u organskoj sintezi, ed. P. Hodge, D.C. Sherrington, Chichester, 1980; Oligonukleotidna sinteza, praktični pristup. Operite., 1984. Branitelj Potapov.
Kemijska enciklopedija. - m.: Sovjetska enciklopedija. Ed. I. L. Knunyants. 1988 .
Gledajte što je "sinteza solidne faze" u drugim rječnicima:
sinteza solidne faze - Kombinatorna sinteza kemijske sinteze različitih pripravaka koji koriste čvrstu potporu za razdvajanje pripravaka tijekom sinteze, čime se pojednostavljuje identifikacija dobivenih pripravaka, pričvršćen je na rastući peptidni lanac, dok je dicikloheksilkarbodiimid korišten kao kondenzacijski agens (DCC s aditivom N-hidroksiukcinimid (GS). Aktivni peptid je odvojen od polimera, zaštitne skupine su uklonjene djelovanjem sve to može biti napisan kao shema (vidi stranicu 336; TFUK - trifluorooctena kiselina).
Ukupni prinos proizvoda 85 bio je oko 40%, od kojih se može dobiti samo 10% pročišćenog aktivnog 84.
Blokovi su sintetizirani vezanjem fragmenata dobivenim ili linearnom ili konvergentnom sintezom. Prilikom izgradnje bloka (1-12), vezanje fragmenata provedeno je kroz linkove proline, jer je racemizacija minimalna. U većini slučajeva, vezanje je provedeno aktiviranim eterom pomoću pentaklorofenila (RSR) ili -netrofenil etera. Shema sinteze je limeloksikarbonil protetski blok prikazan je u nastavku.

U slučajevima kada se linkovi prolina ne mogu koristiti kao mjesto vezanja fragmenata, njihov spoj se provodi azidni postupak na kojem manje racemizacije.
Ukupna aktivnost proizvoda (80%) je veća nego u slučaju sinteze malicrop pijedestala (30%).

Kombinatorna sinteza može se provesti ne samo u otopini (sinteza tekuće faze), već i na površini krute kemijski inertne faze. U tom slučaju, prvi početni materijal je kemijski "ušiven" na funkcionalne skupine na površini polimernog nosača (ester ili amidna veza se najčešće koristi) i tretira se s otopinom druge izvorne tvari, koja se uzima u značajan višak reakcije na kraj. U takvom obliku reakcije postoje definitivno pogodnost, budući da je proizvod oslobođen: polimer (obično u obliku granula) je jednostavno filtriran, temeljito je ispran od ostataka drugog reagensa i kemijski cijepanje ciljanog spoja iz nje.
U organskoj kemiji ne postoji niti jedna reakcija koja u praksi ionako osigurava kvantitativni prinos ciljnih proizvoda. Jedina iznimka očigledno je potpuni izgaranje organskih tvari u kisiku na visokim temperaturama do CO2 i H2O. Stoga je čišćenje ciljnog proizvoda uvijek neophodan, a često i najteži i dugotrajniji zadatak. Posebno težak zadatak je izolirati proizvode sinteze peptida, na primjer, odvajanje složene smjese polipeptida. Stoga je bio u peptidnoj sintezi da je metoda sinteze na čvrstoj polimerni supstrat, razvijen početkom 60-ih godina dvadesetog stoljeća, dobila je najveća raspodjela razvijena na početku 60-ih godina.
Polimerni nosač u Merryfield metodi je granulirani umreženi polistiren koji sadrži klorometilne skupine u benzenskoj jezgri, koji su liniji koji povezuju supstrat s prvim aminokiselinskim ostatkom polipeptida. Ove skupine pretvaraju polimer u funkcionalni analog benzil klorida i prijavili su sposobnost da lako formiraju spojeve esterne veze pri reakcijama s karboksilatnim anionima. Kondenzacija takve smole s N-zaštićenim aminokiselinama dovodi do stvaranja odgovarajućih benzil estera. Uklanjanje N-zaštite od daje C-zaštićenog derivata prve aminokiseline, kovalentno povezanog s polimerom. Aminoocilacija oslobađajućeg derivata amino skupina N-zaštićenog drugog aminokiseline, nakon čega slijedi uklanjanje N-zaštite dovodi do sličnog derivata dipheptida također vezanog za polimer:
Takav dvostupanjski ciklus (uklanjanje zaštite - aminoocilacije) može biti, u načelu, ponovio onoliko puta koliko je potrebno za izgradnju polipeptidnog lanca određene duljine.
Daljnji razvoj memorijskih ideja usmjeren je prvenstveno na pretraživanje i stvaranje novih polimernih materijala za podloge, razvoj metoda za odvajanje proizvoda i stvaranje automatiziranih instalacija za cijeli ciklus sinteze polipeptida
Učinkovitost metode Merofield pokazana je uspješnom sintezom brojnih prirodnih polipeptida, posebno inzulin. Posebno su prikazane vizualne prednosti na primjeru sinteze reprodukluklea enzima. Na primjer, cijena znatnog napora, već nekoliko godina, Hirschmen s 22 zaposlenika izvršio je sintezu enzima ribonuklease (124 aminokiselinske ostatke) uz pomoć tradicionalnih metoda tekuće faze. Gotovo u isto vrijeme, isti protein je dobiven automatskom sintezom krute faze. U drugom slučaju, sinteza, uključujući samo 11.931 različitih operacija, uključujući 369 kemijskih reakcija, proveli su dva sudionika (GATT i Merryfin) u samo nekoliko mjeseci.
Ideje serryPhorusa služilo je kao osnova za stvaranje različitih metoda kombinatorne sinteze knjižnica polipeptida različitih zgrada.
Dakle, 1982. godine, izvorna strategija multistage paralelne sinteze peptida na čvrstoj fazi poznatoj kao "podijeljena metoda" je predložena ( podjela. - Podjela, razdvajanje) ili "Mix i skinuti" metoda (sl. 3). Njegova suština je sljedeća. Pretpostavimo da se od tri aminokiseline (a, b i c) trebate dobiti sve moguće kombinacije tripeptida. Za to su granule krutog polimera (P) odvojene s tri jednaka dijela i tretiraju se s otopinom jedne od aminokiselina. U tom slučaju, sve aminokiseline kemijski su povezane s površinom polimera jedne od njegovih funkcionalnih skupina. Dobiveni polimeri triju sorti temeljito se miješaju i smjesa se ponovno razdvoji u tri dijela. Zatim svaki dio koji sadrži sve tri aminokiseline u istim količinama ponovno se tretira s jednom od istu tri aminokiseline i prima devet dipeptida (tri smjese od tri proizvoda). Druga smjesa, odvajanje u tri jednaka dijela i liječenje aminokiselina daju željeni 27 tripleptidi (tri smjese od devet proizvoda) u samo devet faza, dok bi primitak od njih zahtijevala sintezu 27 × 3 \u003d 81 stupnjeva.
Ministarstvo obrazovanja i znanosti Ruske Federacije
FGAOU VPO "URAL FEDERALNI UNITIVNICI nazvano po prvom predsjedniku Rusije B. N. Yeltsin"
Odjel za tehnologiju organske sinteze
Sažetak na temu: "Načela i metode sinteze krute faze. Peptidi sinteze »
Izvršeni student c. X-300803.
Shaikutdinova a.i.
Provjeri Berseneva V.S.
Yekaterinburg 2013.
1. Uvod ............................................... ..................................... 3
2. Što je peptidi? ............................................ ... .............................................. četiri
2.1. Struktura peptida .............................................. .................. 5
2.2. Sinteza peptida ............................................... ................... .7
3. Sinteza krute faze peptida .......................................... ......... 10
3.1. Metoda Merrinfield ............................................... ............. 10
3.2. Čvrsti supstrat ................................................ ................
3.3. Odabir supstrata ............................................... ................ ... 14
3.4. Linkeri ................................................. ........................... 16
4. Prva sinteza prirodnog hormona - oksitocina ............................... 22
5. Sinteza inzulina u kavezu ........................................... ............................ ..30
6. Zaključak ............................................... ........................................ ..34
7. Literatura ............................................... ............................ ... 35
Uvod
U organskoj kemiji ne postoji niti jedna reakcija koja u praksi ionako osigurava kvantitativni prinos ciljnih proizvoda. Jedina iznimka je očito ukupni izgaranje organskih tvari u kisiku na visokim temperaturama do CO2 i H2O. Stoga je čišćenje ciljnog proizvoda složen i dugotrajan zadatak. Na primjer, 100% pročišćavanje proizvoda sinteze peptida je težak problem. Doista, prva puna sinteza peptida, oksitocin hormona (1953. g) koji sadrži samo 8 aminokiselinskih ostataka, smatralo se izvanrednim postignućima koje ga je dovelo u autora, V. du Vino, Nobelovu nagradu 1955. Međutim, u Sljedećih dvadeset godina sinteza polipeptida takve složenosti pretvorila se u rutinu, tako da se sada sinteza polipeptida koji se sastoji od 100 i više aminokiselinskih ostataka više ne smatra neodoljivim teškim zadatkom.
Cilj: rastavljanje i objasniti: "Što je uzrokovalo takve dramatične promjene u području polipeptidne sinteze?"
Što je peptidi?
Peptidi - prirodni ili sintetski spojevi,molekulekoji su izgrađeni od ostatakaalfa-aminokiseline međusobno povezane peptidom (amidnim) vezama C (O) NH. Može sadržavati B.molekulatakođer neimvana komponenta (npr. Ostatakkarbohidrat). Po broju aminokiselinskih ostataka uključenih umolekulepeptidi razlikuju dipeptide, tripleptide, tetrapeptide itd. Peptidi koji sadrže do 10 aminokiselinskih ostataka nazivaju se oligopeptidi koji sadrže više od 10 aminokiselinskih ostataka prirodnih polipeptida polipeptidi.s molekulskom težinom više od 6 tisuća zvanihproteini.
Po prvi put, peptidi su izolirani iz enzimskih proteinskih hidroliza. Pojam "peptidi" predlaže E. Fisher. Prvi sintetski peptid primio je T. Kursuus 1881. godine. E. Fisher do 1905. razvio je prvi opći način sinteze peptida i sintetizirao brojne oligopeptide različitih zgrada. Postojeći doprinos razvoju kemije peptida napravio je studente E. Fisher E. Abdergalden, jezero i M. Bergman. Godine 1932., M Bergman i L. Zervas se koristi u sintezi peptida benziloksikarbonilne skupine (karbobenzoksi skupina) kako bi se zaštitili alfa-amino skupine aminokiselina, koji su označili novu fazu u razvoju sinteze peptida. Dobivene N-zaštićene aminokiseline (N-karbobenzoksiaminske kiseline) su naširoko korištene za dobivanje različitih peptida, koji su uspješno korišteni za proučavanje brojnih ključnih problema kemije i biokemije tih tvari, na primjer, za proučavanje specifičnosti supstrata proteolitičkog enzimi. Uz upotrebu N-karboksiksijskih kiselina, prirodni peptidi (glutation, karnozin itd.) Prvi su sintetizirani. Važno postignuće u ovom području razvijen je početkom 50-ih. P. Vogan i drugi. Sinteza peptida miješanim anhidridima.
Godine 1953. V. du Vino sintetizirao je prvi peptidni hormon-toksotcin. Na temelju pojmova koje je razvio P. Merryphield 1963. godine stvoreni su automatski peptidni sintetizatori. Prihvatili su intenzivne metode razvoja kontrolirane enzimske sinteze peptida. Korištenje novih metoda omogućilo je da se provede sinteza hormonskog inzulina itd.
Uspjesi sintetičke kemije peptida pripremljena su postignućima u razvoju takvih metoda razdvajanja, pročišćavanja i analize peptida, kao što je kromatografija na ionsku izmjenu, elektroforezu na različitim nosačima, gel filtracija, visoko učinkovita tekućinska kromatografija (HPLC), imuno- Kemijska analiza, itd. Pribili su velike metode razvoja za analizu krajnjih skupina i metoda podjele stepenaste peptida. Posebno je bilo automatsko analizatore aminokiselina i automatskih instrumenata kako bi se odredila primarna struktura peptida-tzv. Seksektora.