Развитие на хроматография. Хроматография като изследвателен метод
Хроматографията е руски учен, ботаника и физикохимист Михаил Семенов цвят.
Откриването на хроматографията се отнася до времето на завършване на работата по магистърската теза в Санкт Петербург (1900 - 1902 г.) и първият период на работа във Варшава (1902 - 1903). Проучване на пигментите на растенията, цветът преминава разтвор на сместа много малко различен от цвета на пигментите през тръбата, напълнена с адсорбентен калциев карбонат и след това се промива след това адсорбент с чист разтворител. Отделни компоненти на сместа бяха разделени и оформени цветни ивици. Според съвременната терминология цветът е открил развиващия се вариант на хроматография (разработване на течна адсорбционна хроматография). Основните резултати от изследванията за развитието на създадената от него хроматография. Цвят, очертан в книгата "Хромофили в растителния и животинския свят" (1910), която е докторска дисертация. Хроматографска газова седиментна йонна обмяна
Цветът широко използва хроматографския метод не само за отделянето на сместа и само за нейното мултиконсонсионерност, но и за количествен анализ, за \u200b\u200bтази цел тя счупи стъклената колона и наряза адсорбентната колона към слоевете. Цветът е разработил оборудване за течна хроматография, за първи път провежда хроматографски процеси при понижено налягане (помпено) и при известно свръхналягане, разработени препоръки за приготвяне на ефективни колони. Освен това той въведе много основни концепции и условия на нов метод, като "хроматография", "проявление", "изместване", "хроматограма" и др.
Хроматографията първо се използва много рядко, нейният скрит период продължи около 20 години, по време на който се появява само много малък брой съобщения за различни приложения на метода. И едва през 1931 г., R. Kunu (Германия) А. Winterstein (Германия) и Е. Ледтер (Франция), които са работили в химическа лаборатория (водена от Р. Кун), Института за император Вилхелм за медицински изследвания в Хайделберг, \\ t успя да отпусне този метод А - и В-каротин от суров каротин и по този начин демонстрират стойността на отвора на цвета.
Важен етап от развитието на хроматографията беше откриването на съветски учени N.A. Измайлов и М.А. SCHREIBER Метод на хроматография в тънък слой (1938), който позволява анализ с микроколизъм на веществото.
Следващата важна стъпка беше откриването на A. Martin и R. Sing (England) на варианта на течна разпределителна хроматография върху примера на отделяне на ацетилови производни на аминокиселини върху колона, напълнена със силикагел, наситен с вода, като се използва хлороформ като разтворител (1940). В същото време беше отбелязано, че не само течността може да се използва като мобилна фаза, но и газ. Няколко години по-късно бяха предложени тези учени да извършат отделянето на производни на аминокиселини върху навлажнени с вода с бутанол като мобилната фаза. Те също така прилагат първата двуизмерна система за разделяне. За откриването на разпространението на хроматографията, Мартин и пея получиха Нобелова награда в химията. (1952). Освен това, Мартин и А. Джеймс извърши вариант на газоразпределителна хроматография, отделяща сместа върху смесен сорбент от DS-550 силикон и стеаринова киселина (1952 - 1953). От това време най-интензивното развитие се получава чрез метод на газов хроматография.
Един от варианта на газов хроматография е хромантография, при който да се подобри отделянето на газовата смес едновременно с движението на движещата се фаза - газ, засяга сорбента и отделената смес с движещо се термословно поле, имащо определен градиент по дължина ( AA Zhukhovitsky и SOTR., 1951).
Забележим принос за развитието на хроматографския метод е въведен от град Schwab (Германия), който е основателят на йонообменна хроматография (1937 - 1940). Тя получи по-нататъшно развитие в творбите на съветските учени, напр. Gapona и TB. Gapona, която провежда хроматографско отделяне на смес от йони в разтвора (заедно с FM шимиякин, 1947), и също така провежда идеята за хроматографско разделяне на смес от вещества на базата на разликата в разтворимостта на разтворимостта (седиментна хроматография, 1948).
Съвременният етап в развитието на йонообменна хроматография започва през 1975 г. след работата на град МАЛКА, Т. Стивънс и У. Бауман (САЩ), в която те предложиха нов аналитичен метод, наречен йонна хроматография (опция за високо ефективна йонообменна хроматография с конденкометрично откриване).
Създаването на компанията "Perkin-Elmer" M. Golley (САЩ) на капилярния вариант на хроматографията (1956), в която сорбент се прилага към вътрешните стени на капилярната тръба, което позволява да се анализира микроколизмът на многокомпонентни смеси.
В края на 60-те години. Повишен интерес към течната хроматография. Имаше високоефективна течна хроматография (HPLC). Това се улеснява от създаването на силно чувствителни детектори, нови селективни полимерни сорбенти, ново оборудване, което позволява да се работи при високо налягане. В момента HPLC заема водеща позиция сред други методи за хроматография и се прилага в различни версии.
Хроматографията е метод за разделяне и определяне на вещества на базата на разпределението на компонентите между двете фази и фиксирани. Фиксираната (стационарна) фаза се обслужва твърдото поресто вещество (често наричано сорбент) или течен филм, приложен към твърдо вещество. Мобилната фаза е течност или газ, протичащ през неподвижна фаза, понякога под налягане. Компонентите на сместа от сместа (ядро) заедно с подвижната фаза се движат по стационарната фаза. Обикновено се поставя в стъклена или метална тръба, наречена колона. В зависимост от силата на взаимодействие с повърхността на сорбент (поради адсорбция или по друг механизъм), компонентите ще се движат по колоната при различни скорости. Някои компоненти ще останат в горния слой на сорбент, други, в по-малка степен, взаимодействащи с сорбент, ще бъдат в долната част на колоната, а някои ще оставят колоната заедно с подвижната фаза (такива компоненти са неплатени, и Техното време за задържане определя ораторите "Dead Time").
По този начин се случва бързо разделяне на сложни смеси от компоненти.
Откриване на историята:
Раждане на хроматография
Вечерта на този ден на среща на биологичното отдел на Варшавското общество на натуралистите, асистентът на катедра "Анатомия и физиология на растението Михаил Семенович" е направен от доклада "на нова категория явления за адсорбция и за използването от тях до биохимичен анализ. "
За съжаление, M.S. Tsvet, като се формира ботаника, не оценява химическия аналитичен аспект на откриването му като правилно и малко публикува работата си в химическите списания. Впоследствие тя е била химионес, която оценява реалния мащаб на предложените M.S. Цветът на хроматографския метод, който се превърна в най-често използвания метод за аналитична химия.
Трябва да се подчертаят следните подробности за хроматографските методи:
1. Разделянето е динамично и актовете на сорбционно-десорбция на споделени компоненти се повтарят многократно. Това причинява значително по-голяма ефективност на хроматографията
разделяне в сравнение със статичните методи на сорбция и
екстракция.
2. По време на разделянето се използват различни видове взаимодействие на сорбатите и стационарните фази: от чисто физически до хемосербция.
Това води до възможността за селективно разделяне на широк диапазон
3. На отделените вещества можете да прилагате различни допълнителни полета (гравитационни, електрически, магнитни и т.н.), които променят условията на разделяне, разширяване на възможностите за хроматография.
4. Хроматографията е хибриден метод, който съчетава едновременното разделяне и дефиниране на няколко компонента.
5. Хроматографията ви позволява да решите двете аналитични задачи (разделяне, идентификация, определение) и препаративна (почистване, избор, концентрация). Решаването на тези задачи може да се комбинира, като ги изпълнява в режим "онлайн".
Многобройни методи се класифицират от съвкупното състояние на фазите, механизма за разделяне и техниката на разделяне.
Хроматографските методи се различават в метода на извършване
процеса на разделяне отпред, от решаващо значение и елуент.
Йонна хроматография
Йонна хроматография е високоефективна течна хроматография за разделяне на катиони и аниони върху йонообменници
нисък капацитет. Широко разпространена йонна хроматография
поради броя на предимствата й:
- способността да се определи голям брой неорганични и
органични йони, както и едновременно дефиниране на катиони и
- висока чувствителност на определяне (до 1 ng / ml без
предварителна концентрация;
- висока селективност и експресивност;
- малък обем от анализираната проба (не повече от 2 ml проба);
- широк диапазон от определени концентрации (от1 ng / ml до
- възможността за използване на различни детектори и техните комбинации, което дава възможност да се осигури селективност и малка дефиниция на времето;
- способността да се автоматизира напълно определението;
- В много случаи пълното отсъствие на предварителна подготовка на извадката.
В същото време, като всеки аналитичен метод, йонна хроматография не е лишена от недостатъци, които могат да се приписват на:
- сложността на синтеза на йонообменници, които значително усложняват
развитие на метода;
- по-ниска ефективност на разделяне в сравнение с HPLC в сравнение с HPLC;
- необходимостта от висока устойчивост на корозия
хроматографска система, особено при определяне
катиони.
2.1 История на развитието:
Изследването на йонообменните процеси започна в началото на XIX век. С наблюдения за ефекта на почвите върху химическия състав на солените разтвори в контакт с него. В края на 40-те години Томпсън отбеляза, че почвата абсорбира амоняк от въведените органични торове, съответните експерименти са извършени от специалиста на тяхната Йорк Д. Спенс. Първите резултати от експериментите Г. Спенс бяха публикувани от Г. Томпсън през 1850 г. Статията отбелязва, че "първото откритие на висококачествените свойства на почвата едва ли може да се провали като полезно за селското стопанство" и последната му работа е публикувана e През 1852 и 1855 година.
2.3 Принципи на отделяне на йони в сорбционни процеси
Хроматографията на йонообменната хроматография се отнася до течна твърда фазова хроматография, в която подвижната фаза е течност (елуент), а фиксираната фаза е твърд (йонообменник). Методът на йонообменна хроматография се основава на динамичен заместващ процес на йони, свързани с фиксирана фаза, елуент йони, влизащи в колоната. Разделянето се дължи на различен афинитет към йонообменността на йони в сместа, което води до различни скорости на движението им в колоната.
Йонна хроматография е вариант на колонна йонообменна хроматография.
Според препоръките на JUPAK (1993) термините йонообмен (МОК) и йонната (тяхната) хроматография се определят, както следва. "Йонообменната хроматография се основава на разликата в взаимодействията на йонообмен за индивидуални анализирани вещества. Ако йоните са разделени и могат да бъдат открити с детектор за проводник или индиректно UV детекция, то се нарича йонна хроматография."
Модерна (2005) Текстът: "йонна хроматография включва всички високоефективни течни хроматографски (HPLC) разделяне на йони в колоните, комбинирани с директно откриване в дебитния детектор и количествената обработка на получените аналитични сигнали." Това определение характеризира йонна хроматография без позоваване на механизма за разделяне и метода за откриване и по този начин го разделя от класическия йонообмен.
Следните принципи на разделяне се прилагат в йонна хроматография:
Йонообмен.
Обучение на йонни двойки.
Изключващи йони.
ION Exchange.
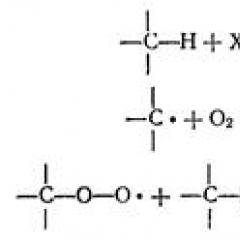
Йонният обмен е реверсивен хетерогенен отговор на еквивалентни йонизационни йони в йонната фаза (противойони), синдикатите на елуента. Анти -аците се държат от функционалните групи йони за сметка на електростатичните сили. Като правило, в катионна хроматография, тези групи са групи сулфонови киселини; В случай на анионна хроматография - кватернерни амониеви основания. На фиг. 1 показва схемата на процеса на обмен на катиони и аниони. Йоните на определеното вещество са маркирани като елуент йони, които се конкурират с тях за обменни центрове - E.

Фиг. 1. йонообменността на катиони (A +) и аниони (a-) върху елуент йони (e + или e-) с участието на катион-обменник, съдържащ функционални сулфови групи - SO3- и анионен обменник (кватернерна амониева база групи -N + R3).
Обучение на йонна ал
За да се приложи този механизъм за разделяне, се използват йоно-сдвоени реагенти, които се добавят към елуентния разтвор. Такива реагенти са анионни или катионни повърхностно активни вещества, например, алкилсулфонови киселини или тетралламониеви соли.
Заедно с противоположно заредените йонно-дефинирани йони, йони на този йон-чифт реагент образуват беззавързана йонна двойка, която може да се съхранява на фиксираната фаза, дължаща се на междумолекулни взаимодействия. Разделянето се извършва поради разликата в константи на образуването на йонни двойки и степените на адсорбцията им върху матрицата сорбент. На фиг. Фигура 2 показва статичен йонен обменен модел в хроматография с йонна двойка след адсорбция на реагента върху фиксираната фаза. Този принцип на разделяне се използва както за аниони, така и за катиони.

Фиг. 2.. ION обменен модел в йонно-парна хроматография.
Йонно изключване
Йонеклузионна хроматография (IEX). По принцип, той се използва за отделяне на слаби киселини или бази. Най-голямата стойност на IEX трябва да определи карбоксилни и аминокиселини, феноли, въглехидрати.
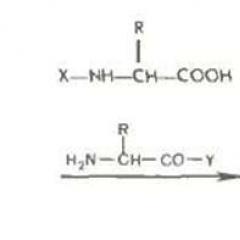
На фиг. 3 показва принципа на разделяне, използвайки iex върху примера на R-CoOH киселини.
Фиг. 3. Схема за разделяне на R-CoOH карбоксилна киселина, използваща хроматография с йонокелузия.

В хроматографията на йонокесулнузин като фиксирана фаза често се използва напълно селзален катионен обменник, съдържащ йон-вода (противойони), често се използва. Във воден разтвор на елуент групите на йони се хидратират селфонова киселина. Хидратната обвивка е ограничена до въображаема отрицателно заредена мембрана (Donnan membrane). Мембраната е пропусклива само за не-експострурани молекули (например вода).
Биологичните карбоксилни киселини могат да бъдат разделени, ако се използват силни минерални киселини като елуент. Благодарение на ниските стойности на константи на киселинността, карбоксилните киселини присъстват в такива решения в нелоялната форма. Тези форми могат да преминат през Доннанската мембрана и да се адсорбират върху фиксираната фаза.
Изпратете добрата си работа в базата знания е проста. Използвайте формата по-долу
Студентите, завършилите студенти, млади учени, които използват базата на знанието в обучението и работата ви, ще ви бъдат много благодарни.
Публикувано от http://www.allbest.ru.
1. История на откриването и развитието на хроматография
2. Основни разпоредби
3. Класификация на методите за хроматографски анализ
4. Адсорбционна хроматография. Тънкослойна хроматография
4.1 Техника на експеримента в тънкослойна хроматография
5. Газова хроматография
5.1 Газо-адсорбционна хроматография
5.2 Газова-течна хроматография
6. Разпределителна хроматография. Хартиена хроматография
7. Хроматография със седименти
7.1 Класификация на методите за седиментна хроматография върху техниката на експеримента
7.2 Хроматография на седименти на хартия
8. Йонообменна хроматография
Заключение
Библиография
1. ИсторияХроматография открития и развитие
Хроматографията е руски учен, ботаника и физикохимист Михаил Семенов цвят.
Откриването на хроматографията се отнася до времето на завършване на работата по магистърската теза в Санкт Петербург (1900 - 1902 г.) и първият период на работа във Варшава (1902 - 1903). Проучване на пигментите на растенията, цветът преминава разтвор на сместа много малко различен от цвета на пигментите през тръбата, напълнена с адсорбентен калциев карбонат и след това се промива след това адсорбент с чист разтворител. Отделни компоненти на сместа бяха разделени и оформени цветни ивици. Според съвременната терминология цветът е открил развиващия се вариант на хроматография (разработване на течна адсорбционна хроматография). Основните резултати от изследванията за развитието на създадената от него хроматография. Цвят, очертан в книгата "Хромофили в растителния и животинския свят" (1910), която е докторска дисертация. Хроматографска газова седиментна йонна обмяна
Цветът широко използва хроматографския метод не само за отделянето на сместа и само за нейното мултиконсонсионерност, но и за количествен анализ, за \u200b\u200bтази цел тя счупи стъклената колона и наряза адсорбентната колона към слоевете. Цветът е разработил оборудване за течна хроматография, за първи път провежда хроматографски процеси при понижено налягане (помпено) и при известно свръхналягане, разработени препоръки за приготвяне на ефективни колони. Освен това той въведе много основни концепции и условия на нов метод, като "хроматография", "проявление", "изместване", "хроматограма" и др.
Хроматографията първо се използва много рядко, нейният скрит период продължи около 20 години, по време на който се появява само много малък брой съобщения за различни приложения на метода. И едва през 1931 г., R. Kunu (Германия) А. Winterstein (Германия) и Е. Ледтер (Франция), които са работили в химическа лаборатория (водена от Р. Кун), Института за император Вилхелм за медицински изследвания в Хайделберг, \\ t успя да отпусне този метод А - и В-каротин от суров каротин и по този начин демонстрират стойността на отвора на цвета.
Важен етап от развитието на хроматографията беше откриването на съветски учени N.A. Измайлов и М.А. SCHREIBER Метод на хроматография в тънък слой (1938), който позволява анализ с микроколизъм на веществото.
Следващата важна стъпка беше откриването на A. Martin и R. Sing (England) на варианта на течна разпределителна хроматография върху примера на отделяне на ацетилови производни на аминокиселини върху колона, напълнена със силикагел, наситен с вода, като се използва хлороформ като разтворител (1940). В същото време беше отбелязано, че не само течността може да се използва като мобилна фаза, но и газ. Няколко години по-късно бяха предложени тези учени да извършат отделянето на производни на аминокиселини върху навлажнени с вода с бутанол като мобилната фаза. Те също така прилагат първата двуизмерна система за разделяне. За откриването на разпространението на хроматографията, Мартин и пея получиха Нобелова награда в химията. (1952). Освен това, Мартин и А. Джеймс извърши вариант на газоразпределителна хроматография, отделяща сместа върху смесен сорбент от DS-550 силикон и стеаринова киселина (1952 - 1953). От това време най-интензивното развитие се получава чрез метод на газов хроматография.
Един от варианта на газов хроматография е хромантография, при който да се подобри отделянето на газовата смес едновременно с движението на движещата се фаза - газ, засяга сорбента и отделената смес с движещо се термословно поле, имащо определен градиент по дължина ( AA Zhukhovitsky и SOTR., 1951).
Забележим принос за развитието на хроматографския метод е въведен от град Schwab (Германия), който е основателят на йонообменна хроматография (1937 - 1940). Тя получи по-нататъшно развитие в творбите на съветските учени, напр. Gapona и TB. Gapona, която провежда хроматографско отделяне на смес от йони в разтвора (заедно с FM шимиякин, 1947), и също така провежда идеята за хроматографско разделяне на смес от вещества на базата на разликата в разтворимостта на разтворимостта (седиментна хроматография, 1948).
Съвременният етап в развитието на йонообменна хроматография започва през 1975 г. след работата на град МАЛКА, Т. Стивънс и У. Бауман (САЩ), в която те предложиха нов аналитичен метод, наречен йонна хроматография (опция за високо ефективна йонообменна хроматография с конденкометрично откриване).
Създаването на компанията "Perkin-Elmer" M. Golley (САЩ) на капилярния вариант на хроматографията (1956), в която сорбент се прилага към вътрешните стени на капилярната тръба, което позволява да се анализира микроколизмът на многокомпонентни смеси.
В края на 60-те години. Повишен интерес към течната хроматография. Имаше високоефективна течна хроматография (HPLC). Това се улеснява от създаването на силно чувствителни детектори, нови селективни полимерни сорбенти, ново оборудване, което позволява да се работи при високо налягане. В момента HPLC заема водеща позиция сред други методи за хроматография и се прилага в различни версии.
2. Основни разпоредби
Хроматографията е метод за разделяне и определяне на вещества въз основа на разпределението на компонентите между двете фази - подвижни и фиксирани. Фиксираната (стационарна) фаза се обслужва твърдото поресто вещество (често наричано сорбент) или течен филм, приложен към твърдо вещество. Мобилната фаза е течност или газ, протичащ през неподвижна фаза, понякога под налягане. Компонентите на сместа от сместа (ядро) заедно с подвижната фаза се движат по стационарната фаза. Обикновено се поставя в стъклена или метална тръба, наречена колона. В зависимост от силата на взаимодействие с повърхността на сорбент (поради адсорбция или по друг механизъм), компонентите ще се движат по колоната при различни скорости. Някои компоненти ще останат в горния слой на сорбент, други, в по-малка степен, взаимодействащи с сорбент, ще бъдат в долната част на колоната, а някои ще оставят колоната заедно с подвижната фаза (такива компоненти са неплатени, и Техното време за задържане определя ораторите "Dead Time"). По този начин се случва бързо разделяне на сложни смеси от компоненти. Трябва да се подчертаят следните подробности за хроматографските методи:
1. Разделянето е динамично и актовете на сорбционно-десорбция на споделени компоненти се повтарят многократно. Това причинява значително по-голяма ефективност на хроматографското разделяне в сравнение със статичните методи на сорбция и екстракция.
2. По време на разделянето се използват различни видове взаимодействие на сорбатите и стационарните фази: от чисто физически до хемосербция. Това води до възможността за селективно разделяне на широк кръг вещества.
3. На отделените вещества можете да прилагате различни допълнителни полета (гравитационни, електрически, магнитни и т.н.), които променят условията на разделяне, разширяване на възможностите за хроматография.
4. Хроматографията е хибриден метод, който съчетава едновременното разделяне и дефиниране на няколко компонента.
5. Хроматографията ви позволява да решите двете аналитични задачи (разделяне, идентификация, определение) и препаративна (почистване, избор, концентрация). Решението на тези задачи може да се комбинира чрез извършване на режима "On Line".
6. Многобройни методи се класифицират чрез агрегирано състояние на фазите, разделяния механизъм и техниката на разделяне. Хроматографските методи се различават в метода за извършване на процеса на разделяне към предната, тигела и елуента.
3. Класификация на методите за хроматографски анализ
Формирането на хроматографски методи се основават на принципите, които вземат предвид следните различни характеристики на процеса на разделяне:
* Разлики в съвкупното състояние на фазите на използваната хроматографска система;
* различия в естеството на взаимодействията на отделените вещества с фиксирана фаза;
* Експериментални разлики в методите за процеса на хроматографско разделяне.
В таблици 1? 3 показва основните варианти на класификацията на известните хроматографски методи.
Тъй като естеството на взаимодействието на отделените съединения с фази на различни хроматографски системи може да варира значително, почти няма обекти, за отделянето, от което не би било възможно да се намери подходяща фиксирана фаза (твърда или течна) и подвижен разтворител системи. Обхватът на основните варианти на хроматография в зависимост от молекулното тегло на изследваните съединения е даден в таблица. четири.
4. Адсорбционна хроматография. Тънкослойна хроматография
Една от най-често срещаните техники за адсорбционна хроматография е тънкослойната хроматография (TLC) - вид равнинна хроматография, при която адсорбентът се използва като тънък слой върху плочата.
Принципа и основните понятия на метода на TLC. На чиста равна повърхност (плоча от стъкло, метал, пластмаси) по един или друг начин се прилага тънък слой от сорбент, който най-често се фиксира върху повърхността на плочата. Размерите на плочата могат да бъдат различни (дължина и ширина - от 5 до 50 cm, въпреки че не е необходимо). На повърхността на плочата, внимателно, да не се повреди сорбентният слой, очертан (например, молив) на началната линия (на разстояние 2-3 см от долния край на плочата) и линията на. \\ T Разтворител.
Схема за разделяне на компонентите А и в метода на TLC
В стартовата линия плаката се прилага (чрез микро риза, капилярна) проба - малко количество течност, съдържаща смес от отделими вещества, например, две вещества А и В в подходящ разтворител. Възможно е разтворителят да се изпари, след което плочата е потопена в хроматографската камера в течната фаза на PF, която е специално подбран разтворител или смес от разтворителя за даден случай. Под действието на капилярните сили на PF спонтанно се движат по NF от началната линия до линията на предаването на разтворителя, които се грижат с тях компоненти А и в проби, които се движат при различни скорости. В този случай, афинитетът на компонента А към НФ е по-малък афинитет за една и съща фаза на компонента В, така че компонентът А се движи по-бързо от компонента Б. след достигане на движещата се фаза (разтворител) на линията на разтворителя Хроматографията се прекъсва, плочата се отстранява от хроматографската камера, суши се във въздуха и се определя позицията на петна от вещества А и в повърхността на плочата. Петна (зони) обикновено имат овална или кръгла форма. В разглеждания случай петна компонент се премества от началната линия до разстоянието л. А. , спот компонент в - за разстояние л. Ви разтворителят премина през разстоянието Л..
Понякога едновременно с прилагането на образци на отделни вещества върху началната линия се прилагат малки количества от стандарта стандарт, както и на свидетелски вещества (тези, които се твърдят, че се съдържат в анализираната проба).
За да се характеризират споделените компоненти, RF мобилността (или RF факторът) се въвежда в системата:
R. е.\u003d V. 1 / V. Д.\u003d (L. 1 / T) / (l / t) \u003d l 1 / L. ,
където В. 1 = л. 1 / t. и В. Д.= Л./ t. - съответно скоростта на движение i.- един компонент и разтворител e; л. 1 иЛ. - минаваше път i.- компонентът и разтворителят, съответно, t е времето, необходимо за преместване на разтворителя от началната линия към предната линия на разтворителя. Разстояния л. 1 изстискайте от началната линия до центъра на точката на съответния компонент.
Обикновено коефициентът на мобилност се крие в преразпределението R. е. =0 - 1. Оптималната стойност е 0.3-0.7, се избират хроматографските условия, така че стойността r f се различава от нула и единици.
Коефициентът на мобилност е важна характеристика на сорбатната система сорбент. За възпроизводими и строго константни условия на хроматография R. е. = конст.
Коефициентът на мобилност на RF зависи от редица фактори: естеството и качеството на разтворителя, неговата чистота; природа и качество на сорбент (тънък слой), еднородност на зърната, дебелината на слоя; активността на сорбента (съдържание в тя влага); техники на експеримента (масови проби, дължината на луната на разтворителя); Умение за експериментатори и др. Постоянството за възпроизвеждане на всички тези параметри на практика понякога е трудно. За да се намали въздействието на условията на процеса, се въвежда относителен мобилност фактор Rs..
RS \u003d l / l изкуство\u003d R. е./ R. f ( изкуство ) ,
където R. е. = л./ Л.; R. е. (st)= л. изкуство/ Л.; л. см. - разстоянието от началната линия до центъра на стандартното място.
Относителният коефициент на мобилност на РС е по-обективна характеристика на мобилността на веществото, отколкото коефициента на мобилност R f.
Като стандарт, такова вещество често се избира, за което при тези условия r f? 0.5. В химическата природа стандартът е избран близо до отделените вещества. Използвайки стандарта, стойността на Rs обикновено се намира в Rs \u003d 0.1-10, оптималните граници са около 0.5--2.
За по-надеждна идентификация на споделените компоненти използват "свидетели" - референтни вещества, чието присъствие се приема в анализираната проба. Ако Rf \u003d Rf (SVID), където R F и Rf (SVID) - съответно коефициентите на мобилността на този компонент и свидетел, тогава най-вероятно могат да приемат, че изпитваното вещество присъства в хроматографската смес.
За да се характеризират отделянето на два компонента А и при тези условия, степента (критерий) на разделянето R (A / B) се въвежда:
R (a / b) \u003d d л.(\u003d 2D л. ,
къде. л. - разстоянието между центровете на петна от компоненти А и Б; A (а) и a б) съответно диаметрите на петна А и В върху хроматограмата.
Колкото по-голяма е стойността R (A / B), по-ясните петна на компонентите А и В са разделени върху хроматограмата.
Да се \u200b\u200bоцени селективността на разделянето на две вещества А и Б, използват коефициента на разделяне но:
a \u003d.л. Б. / л. А.
Ако a \u003d 1,че компонентите А и В не са разделени.
За да се определи степента на разделяне R (A / B) на компоненти А и V.
4.1 Експериментална техника в тънкослойна хроматография:
но) Прилагане на проба. Анализираната течна проба се прилага към линията на започване, използвайки капилярната, микро-лайна, микропипета, внимателно докосване на сорбентния слой (диаметърът на петна върху началната линия обикновено е от един до няколко милиметра). Ако към началната линия се нанасят няколко проби, тогава разстоянието между петна от пробите върху началната линия не трябва да бъде по-малко от 2 cm. Ако е възможно, се използват концентрирани разтвори. Петна се изсушават във въздуха, след което се извършва хроматография.
б) Развитие на хроматограма (хроматография).Процесът се извършва в затворени хроматографски камери, наситени с водолазни двойки, използвани като PF, например в стъклен съд, покрит върху капака.
В зависимост от посоката на движение, PF се отличава възходящ, низходящ и хоризонтален хроматография.
Под формата на възходяща хроматография се използват само плочи с фиксиран сорбентен слой. PF се излива върху дъното на камерата (като последното, стъклено химическо стъкло с подходящ размер може да се използва със стъклен капак), хроматографската плоча се поставя вертикално или косо в камерата, така че PF слой на дъното на дъното на Камерата намокри дъното на плочата (под началната линия с ~ 1.5 - 2 cm). PF се движи поради действието на капилярните сили отдолу нагоре (срещу гравитацията) сравнително бавно.
В низходящия вариант на хроматография се прилагат и само плочи с фиксиран слой. PF се подава отгоре и се движи надолу по слоя сорбентния слой. Силата на гравитацията ускорява движението на PF. Това изпълнение се осъществява при анализиране на смеси, съдържащи компоненти, бавно се движат с PF.
В изпълнението на хоризонталната хроматография плаката се поставя хоризонтално. Можете да използвате правоъгълни или кръгли плочи. При прилагане на кръгли плочи (кръгъл вариант на хоризонтална хроматография), началната линия се обозначава като кръг от подходящ радиус (~ 1,5-2 cm), който се прилагат проби. В центъра на кръглата чиния дупката се нарязва, в която е вмъкнат фитилът, за да се снабдява PF. Последният се движи по сорбентния слой от центъра на кръга към периферията си. Хроматографията се извършва в затворена камера - ексикатора или в петриевата печка. С кръгова версия можете едновременно да анализирате до няколко дузини проби.
В TLC методи, едноизмерно, двуизмерно, многократно (RE), се използва етап хроматография.
В еднократна хроматография, анализът се извършва, без да се променя посоката на движение на PF. Този метод е най-често срещан.
Двуизмерна хроматография обикновено се използва за анализ на сложни смеси (протеини, аминокиселини и др.), Сместа се извършва първо с помощта на първия PF 1. Хроматограмата се получава петна, а не отделни вещества и смеси от няколко неразделни компонента. След това през тези петна се извършва нова стартна линия, плочата се завърта на 90 ° и отново се хроматографира, но вече с втория PF 2, стремеж към окончателно разделяне на петна със смеси на петна от отделни компоненти.
Ако плаката е квадрат, тогава пробата се нанася върху диагонала на този квадрат в долния му ъгъл. Понякога двуизмерна хроматография се извършва със същия PF върху квадратна плоча.
Схемата, илюстрираща принципа на двуизмерна хроматография: \\ t
а - хроматограма, получена от PF1;
в - хроматограма, получена от PF2
При многократна (повторна) хроматография, процесът се извършва няколко пъти последователно от същия PF (всеки път - след следващото сушене), докато желаното отделяне на петна на компонентите на сместа (обикновено - не повече от три пъти).
В случай на стъпална хроматография, процесът се извършва със същата плоча последователно използване всеки път на нов PF, докато се достигне ясно разделяне на петна.
в) Декодиране на хроматограми. Ако петна върху хроматограмата са боядисани, след изсушаване на плочите, определете разстоянието от началната линия до центъра на всяко място и изчислете коефициентите на мобилността. Ако съставът на анализираната проба се състои от безцветни вещества, дават неоцветени, т.е. Визуално не са идентифицирани петна върху хроматограма, трябва да похарчите откриване тези петна, за които хроматограма шоу.
Най-често срещаните методи за откриване са описани по-долу.
Облъчване с ултравиолетова светлина.Използва се за откриване на флуоресцентни съединения (петна са светещи по време на облъчването на UV светлинната плоча) или петроленоскуларни вещества, но се използва сорбент с флуоресцентна индикатора (сорбент свети, петна няма да бъдат осветени). Така се откриват, например алкалоиди, антибиотици, витамини и други лекарствени вещества.
Топлинна обработка.Изсушаването на плочата след хроматография се нагрява внимателно (до ~ 200 ° С), като се избягва потъмването на самия сорбент (например, когато тънък слой на сорбент съдържа нишесте). В същото време, петна обикновено се проявяват под формата на кафяви зони (поради частична термолиза на органични компоненти).
Химическа обработка.Често хроматограми показват, обработват ги с реагенти, които образуват цветни съединения с общите компоненти на смесите. За тези цели се използват различни реагенти: чифт йод, амоняк, бром, серен диоксид, сероводород, специално приготвени разтвори, които се третират с плочи. Нанесете както универсални, така и селективни реагенти (концепцията за "универсална" е достатъчно условно).
Universal Reagentamimogoot сервира, например, концентрирана сярна киселина (при нагряване, има потъмняване на органични съединения), кисело воден разтвор на калиев перманганат (зони се наблюдават под формата на кафяви петна върху пурпурен сорбент фон), разтвор на фосфори-молибденова киселина по време на нагряване (сини петна се появяват на жълт фон) и др.
Като селективна употреба, например, реагент на Dragendorf; Zimmerman реагент; воден амониев разтвор на меден сулфат (10% от CUSO 4, 2% в амоняк); Смес от нинхидрин С9Н4О3Н20 с етанол и оцетна киселина.
Реагентът на Dragandorf е разтвор на основния свързващ нитрат на Bondo 3, KJ калиев йодид и оцетна киселина във вода. Използвани за определяне на амини, алкалоиди, стероиди.
Реагента на Zimmerman се приготвя чрез лечение на алкален разтвор КОН2% етанол разтвор на динитробензен, последвано от нагряване на сместа при ~ 70-100 ° С. Нанесете за откриване на стероиди.
С помощта на Ningidrin се откриват петна от амини, аминокиселини, протеини и други връзки.
Използват се някои други начини за откриване на петна. Например, тяхната радиоактивност се измерва, ако някои от отделените компоненти на радиоактивните или се въвеждат специално добавки от радиоактивни изотопи от елементи, които са част от отделените компоненти на сместа.
След откриване на петна върху хроматограмата, те са идентифицирани, т.е. Тя се определя, чрез която съединението съответства на това или онова място. За тази цел най-често се използват референтните места на "свидетели". Понякога петна се идентифицират по степента на коефициентите на мобилност R F, сравнявайки ги с стойностите на RF, известни с тези условия. Въпреки това, такава идентификация на r f често е предварителна.
Цветът на флуоресцентните петна се използва и за целите на идентификацията, тъй като различни съединения са флуоресцентни чрез излъчване на различни дължини на вълните (различни цветове).
При химическо откриване на петна, селективни реагенти придават боядисани петна със съединения с определен характер, който се използва и за целите на идентификацията.
С помощта на TLC метода можете да отворите не само, но и да определите количествено съдържанието на компонентите в смесите. За да направите това, петна върху самите хроматограма се анализират, или отделените компоненти от хроматограмата се отстраняват по един или друг начин (екстракция, елуиране с подходящи разтворители).
Когато се анализират, петна предполагат съществуването на определена връзка между зоната на петна и съдържанието на това вещество (например наличието на пропорционална или линейна зависимост), която се установява чрез метода за изграждане на графика на дипломирането, измерване на графика, измерване на петна от петна "свидетели" с известно съдържание на анализирания компонент.
Понякога те сравняват интензивността на цвета на петна, смятайки, че интензивността на цветните петна е пропорционална на броя на този боядисан компонент. За измерване на интензивността се използват различни техники.
При отстраняване на отделените компоненти от хроматограмата се получава разтвор, съдържащ този компонент. След това последното се определя по един или друг аналитичен метод.
Относителната грешка на количественото определяне на веществото от TLC е 5-10%.
TLC е фармакопеен метод и се използва широко за анализ и контролиране на качеството на различни лекарства.
5. Газова хроматография
В газов хроматография (GC) като подвижна фаза се използва инертен газ (азот, хелий, водород), наречен газов носител. Пробата се подава под формата на пари, фиксирана фаза сервира или твърда - сорбент (хроматография с газ-адсорбтура) или високо кипяща течност, нанесена от тънък слой върху твърд носител (газово-течна хроматография). Помислете за опцията за газо-течна хроматография (GLC). Kizelgur (диатомит) се използва като носител - използва се вид хидратиран силикагел, който често се лекува с реагенти, които превеждат Si-OH групите в групата Si-O-Si (CH3) 3, която увеличава инертността на. \\ T превозвач по отношение на разтворителите. Това са например носителите на "Chromosorb W" и "GasohromQ". В допълнение се използват стъклени микрости, тефлон и други материали.
5.1 Газа- адсорбционна хроматография
Особеността на метода на газовата помпа хроматография (GA) е, че като фиксирана фаза се използват адсорбенти с висока специфична повърхност (10-1000 т2 g-1) и разпределението на вещества между фиксирани и движещи се фази е определен от процеса на адсорбция. Адсорбция на молекули от газовата фаза, т.е. Концентрира се върху повърхността на отделянето на твърди и газообразни фази, настъпва поради междумолекулни взаимодействия (дисперсия, ориентационна, индукция) с електростатичен характер. Възможно е, че образуването на водородни връзки и приносът на този тип взаимодействие в запазените обеми е значително намален с нарастваща температура.
За аналитична практика е важно при постоянна температура, количеството на адсорбираното вещество върху повърхността със S е пропорционално на концентрацията на това вещество в газовата фаза с m:
° С. с. = kc. м. (1)
тези. така че разпределението е настъпило в съответствие с линейната изотерма на адсорбцията (да се - постоянен). В този случай всеки компонент се движи по колоната с постоянна скорост, независима от нейната концентрация. Разделянето на веществата се дължи на различни скорости на тяхното движение. Следователно, изборът на адсорбент, площта и естеството на повърхността, чиято определя селективността (разделянето) при дадена температура, е изключително важно в пропуските.
Топлината на адсорбция намалява с нарастваща температура DH / T.от това откриване зависи и съответно t. R. . Това се използва в практиката на анализ. Ако съединенията се разделят силно на волатилността при постоянна температура, тогава ниското кипене вещества се елуират бързо, високо кипене има по-голямо време, техните пикове на хроматограмата ще бъдат по-ниски и по-широки, анализът отнема много време. Ако, в процеса на хроматография, повишаване на температурата на колоната с постоянна скорост (температурно програмиране), след това пиковете, близки по ширината върху хроматограмата, ще бъдат поставени равномерно.
Като адсорбенти за GI, активни въглища, силикагел, поресто стъкло, се използват главно алуминиев оксид. Нехомогенността на повърхността на активните адсорбенти се дължи на основните недостатъци на методите на GAH и невъзможността за определяне на високо адсорбираните полярни молекули. Въпреки това, за геометрично и химически хомогенни макропорести адсорбенти, е възможно да се анализират смеси от силни полярни вещества. През последните години адсорбентите в наскоро произвеждат адсорбенти с повече или по-малко хомогенна повърхност, като порести полимери, макропоречни силикагел (Satlohroom, ударен, спрей), порести очила, зеолити.
Най-големият метод за хроматография на газовата помпа се използва за анализиране на смеси от газове и нискокипящи въглеводороди, които не съдържат активни функционални групи. Адсорбционните изотерми на такива молекули са близки до линейни. Например, за разделяне на 2, N2, СО, СН4, СО2 се използва успешно от глина. Температурата на колоната е програмирана, за да се намали времето за анализ, като намалява високите газове. При молекулярни срещи - високо фармацевтични естествени или синтетични кристални материали, всички пори, на които имат около същите размери (0.4--1.5 пМ), - могат да бъдат разделени от водородни изотопи. Сорбентите, наречени ловци, се използват за отделяне на метални хидриди (GE, AS, SN, SB). Методът GA на колони с порест полимерни сорбенти или въглеродни молекулни размери е най-бързият и най-удобният начин за определяне на водата в неорганични и органични материали, например в разтворители.
5.2 Газа- течна хроматография
При аналитична практика методът на газо-течна хроматография (GLC) се използва по-често. Това се дължи на крайното разнообразие на фиксираните фаза на течността, което улеснява избирането на селективна фаза за този анализ, като линейността на изотермите на разпределение в по-широка област на концентрация, която ви позволява да работите с големи проби и лесно да получите възпроизводим колони.
Механизмът на разпределение на компонентите между носителя и фиксирана течна фаза се основава на разтварянето им в течната фаза. Селективността зависи от два фактора: парна еластичност на определеното вещество и нейния коефициент на активност в течната фаза. Съгласно закона на Раул, когато се разтваря еластичността на пара от вещество над решение пс. i. пряко пропорционално на коефициента на активност g molar фракция Н. i. в разтвор и налягане на парата на чистото вещество R. i. При тази температура:
p i \u003d n i p ° I (2)
Тъй като концентрацията на I-тия компонент в равновесната парафатна фаза се определя от нейното частично налягане, можете да приемете това
P i ~ c m и n i ~ c s тогава
и коефициент на селективност:
По този начин, долната точка на кипене на веществото (по-голямото Р 0 i), толкова по-слабо се поддържа в хроматографската колона.
Ако точката на кипене на вещества е еднаква, тогава разликите във взаимодействието с фиксирана течна фаза се използват за отделяне: по-силно взаимодействието, толкова по-малко коефициента на активност и по-запазване.
Фиксирани течни фази . За да се гарантира селективността на колоната, е важно да се избере правилно фиксираната течна фаза. Тази фаза трябва да бъде добър разтворител за компонентите на сместа (ако разтворимостта е малка, компонентите се простират от колоната много бързо), нелетлив (така че да не се изпаряват при работната температура на колоната), трябва да се изпаряват имат лек вискозитет (в противен случай процесът на дифузия се забавя) и когато се прилага към носителя, за да образува равномерен филм е здраво свързан с него. Капацитетът на разделяне на фиксираната фаза за компонентите на тази проба трябва да бъде максимален.
Течните фази на три вида се отличават: не-полярни (наситени въглеводороди и др.), Умерено полярни (естери, нитрили и др.) И полярни (полигликоли, хидроксиламия и др.).
Познаване на свойствата на фиксирана течна фаза и естеството на отделимите вещества, като клас, структура, е възможно бързо да се избере селективна течна фаза за разделяне на тази смес. Трябва да се има предвид, че времето за задържане на компонентите ще бъде приемливо за анализ, ако полярността на стационарната фаза и веществото на анализираната проба са близо. За разтворени вещества със тясна полярност, редът на елуиране обикновено корелира с температурата на кипене и ако температурната разлика е достатъчно голяма, е възможно да се завърши разделянето. За отделянето на тясно кипене вещества с различна полярност се използва стационарната фаза, като селективно държи един или повече компоненти, дължащи се на диполнополовото взаимодействие. С увеличаване на полярността на течната фаза, времето за задържане на полярните съединения се увеличава.
За равномерно прилагане на течната фаза към твърдия носител, той се смесва с летлив разтворител, като етер. Към този разтвор се добавя твърд носител. Сместа се нагрява, разтворителят се изпарява, течната фаза остава на носителя. Сух носител с фиксирана течна фаза, приложен по този начин, се пълни с колона, опитвайки се да се избегне образуването на кухини. За равномерно опаковане през колоната, газовият поток се предава и едновременно подслушване на колоната за опаковане на уплътнения. След това, преди да се прикрепите към детектора, колоната се загрява до температура от 50 ° С над тази, на която трябва да се използва. В този случай може да има загуби на течната фаза, но колоната е включена в стабилния режим на работа.
Носител на фиксирани течни фази. Твърдата среда за дисперсия на фиксирана течна фаза под формата на хомогенен тънък филм трябва да бъде механично издръжлив с умерена специфична повърхност (20m 2 / g), малък и равен размер на частиците, и също така да бъде достатъчно инертна към адсорбция на повърхността на твърдото и газообразно фази Беше минимално. Най-ниската адсорбция се наблюдава при носители на силиноразпределени хромозорба, стъклени гранули и флуоропак (флуоровъглероден полимер). В допълнение, твърдите носители не трябва да реагират на увеличаване на температурата и трябва лесно да се правят с течна фаза. В газовата хроматография на хелати като твърд носител носителите на бяла диатомит са най-често използвани - дитомитичен силициев диоксид или kizelgour. Дитомитът е микронорфна, съдържаща вода, силициев диоксид. Такива носители включват хромозорб W, GasoHroom Q, Chromaton N, et al. В допълнение, стъклени топки и тефлонова употреба.
Химически свързани фази. Често се използват модифицирани носители, ковалентно свързани с течна фаза. В този случай стационарната течна фаза е по-здраво върху повърхността дори при най-високите температури на колоната. Например, диатомитският носител се третира с хлоросилан с дълъг верижен заместител, който има определена полярност. Химически свързаната фиксирана фаза е по-ефективна.
6. Разпределителна хроматография. Хартиена хроматография (хроматография върху хартия)
Разпределителната хроматография се основава на използването на разлики в разтворимостта на разпределеното вещество в две контактуващи неинтегриращи течни фази. И двете фази - PF и NF са течни фази. При преместване на течност PF по течността NF, хроматографските вещества се преразпределят непрекъснато между двете течни фази.
Разпределителна хроматография се отнася хартиена хроматураграфична (или хроматография върху хартия) в обичайните си възможности. В този метод, вместо плочи с тънък слой сорбент, използван при TLC, се използва специална хроматографска хартия, съгласно която, импрегнираща, течността PF се премества по време на хроматография от началната линия към линията на разтворителя.
Разграничавам нормална фаза и вярност хартиена хроматография.
В изпълнението нормална фаза хартиената хроматография на течността NF е вода, сорбират под формата на тънък слой върху влакната и в порите хидрофилни хартия (до 25% от теглото). Тази свързана вода в нейната структура и физическо състояние е много различна от конвенционалната течна вода. В него компонентите на общите смеси се разтварят.
Ролята на PF се движи през хартия се играе от друга течна фаза, например органична течност с добавяне на киселини и вода. Течният органичен PF преди хроматография е наситен с вода, така че PF да не разтвори водата с вода на влакната на хидрофилна хроматографска хартия.
Хроматографската хартия се произвежда от индустрията. Тя трябва да отговаря на редица изисквания: да се приготвят от висококачествени влакнести памучни сортове, за да бъдат хомогенни при плътност и дебелина, по посока на ориентиране на влакната, химически чист и инертна спрямо NF и споделените компоненти.
В нормално фазово изпълнение течните смеси, съставени от различни разтворители, най-често се използват като PF. Класически пример за такъв PF е смес от оцетна киселина, n-бутанол и вода в обемно съотношение 1: 4: 5. Използват се разтворители като етилацетат, хлороформ, бензен и др.
В изпълнението вяра хартиена хроматография Течността NF е органичен разтворител, докато вода, водни или алкохолни разтвори и алкохолни смеси с алкохоли действат като течен PF. Процесът се извършва с помощта на хидрофобски хроматографска хартия. Получава се чрез третиране (импрегниране) с нафтален, силиконови масла, парафин и др. Неполярни и ниско-полярни органични разтворители са сорбират върху хидрофобни хартиени влакна и проникват в порите, образувайки тънък слой течен NF. Водата не се съхранява на такава хартия, не го намокри.
Техниката на хартиената хроматография като цяло е същата като в TLC метода. Обикновено се прилага кашпо от анализирано решение, съдържащо смес от общи вещества, се прилага към лентата на хроматографската хартия върху началната линия на старта. След изпаряване на разтворителя, хартията под стартовата линия е потопена в PF, поставяйки хартия вертикално (висяща). Затворете фотоапарата с капак и хроматография, докато PF не достигне линията на преден разток, означен на хартия. След това процесът се прекъсва, хартията се изсушава във въздуха и открива петна и идентифициране на компонентите на сместа.
Хартиената хроматография е подобна на метода на TLC, използван както в качествен, така и в количествен анализ.
За да се определи количествено съдържанието на един или друг компонент на смес, се използват различни методи:
1) продължете от наличието на определена зависимост (пропорционална, линейна) между количеството на веществото в зоната на петна и петна (често графикът за калибриране е предварително изграден);
2) претеглят оцветяването с веществото и същата чиста хартия в областта, а след това по отношение на разликата, която намират, определеното вещество;
3) Вземете под внимание връзката между интензивността на цвета на петна и съдържанието в нея в нея, което дава цвета на петна.
В някои случаи веществата, съдържащи се в петна, се екстрахират с всеки разтворител и след това се анализират екстракта.
Хартиената хроматография е метод на фармакопея, използван за отделяне на смеси, съдържащи както неорганични, така и органични вещества. Методът е на разположение, лесен за изпълнение, но като цяло той е по-малък от по-модерен TLC метод, в който се прилага тънък слой от сорбент.
7. Седиментна хроматография
Методът на седиментна хроматография се използва главно за разделяне и идентифициране на неорганични йони, които съставляват смесите.
Същността на метода. Хроматографията на седименти се основава на използването на химични реакции на утаяване на споделени компоненти на смес с прецизен реагент, който е част от NF. Разделянето се извършва поради неравномерната разтворимост на образуваните съединения, които се прехвърлят в подвижната фаза при различни скорости: по-малко разтворимите вещества се прехвърлят към PF по-бавно от разтворимите.
Можете да илюстрирате използването на метода при примера на отделянето на халогенидните йони: CL-йонно-йон-йон-йон и йодид-йон-йон-йон, едновременно съдържащ се в анализирания воден разтвор. За да направите това, използвайте хроматографска колона (представляваща стъклена тръба с кран на дъното), напълнен с сорбент. Последното се състои от техния носач - алуминиев оксид ал 2 О3 или Si02 силиций, импрегниран със сребърен разтвор на нитрат на Agno 3 (съдържанието на сребърен нитрат е около 10% тегловни от масата на носещия сорбент).
През хроматографската колона се пропуска воден разтвор, съдържащ смес от общи аниони. Тези аниони взаимодействат със сребърни катиони AG +, образувайки толкова разтворими сребърни халидни утайки:
AG + + I -\u003e agiv (жълто)
AG + + BR -\u003e AGBRV (крем)
AG + + CL -\u003e AGCLV (бял)
Разтворимостта на сребърните халиди във вода се увеличава в последователността:
AGL (K ° \u003d 8.3 * 10 -17)< АgВг (К° = 5,3*10 -13) < AgCl (K°= 1,78*10 -10),
където в скоби са стойностите на продуктите за разтворимост при стайна температура. Следователно, първоначално ще се образува жълтата утайка от сребърен йодид, тъй като най-малко разтворим върху хроматограмата ще бъде наблюдаван жълт (отгоре) зона. След това се образува оста на сребърния сребърен бромид (междинна зона). Накрая се образува бяла утайка от сребърен хлорид - долната бяла зона е тъмна поради фотохимичното разлагане на сребърен хлорид с освобождаване на фино метално сребро.
В резултат на това се получава първична седиментна хроматограма.
За по-ясно разделяне на зони, след получаване на първичната хроматограма, през колоната се пропуска чист разтворител, за да се получи вторична седиментна хроматограма с ясно разделяне на зони за утаяване.
В описания пример утаят е част от NF и през колоната се прекарва разтвор, съдържащ смес от общи йони. Възможно е, напротив, да премине разтвор на утаятора през колоната в NF, които са хроматографски йони. В същото време се образуват смесени зони.
Схемата за отделяне на CL-, BR- и I- йони в хроматографската колона по метода на седиментна хроматография.
7.1 Класификация на методите за седиментна хроматография върху техниката на експеримента
Обикновено се разграничават колона седиментна хроматография, проведена в хроматографски колони и самолет Седиментна хроматография, прилагана на хартия или в тънък слой сорбент.
Като сорбенти в седиментна хроматография се използват смеси от инертна среда с инспиратор; Сорбенти със задържащи утаи във формата на йони (йонообменни смоли) или под формата на молекули (активиран въглерод); Хартия, импрегнирана с утаен разтвор.
Носителите най-често избират силикагел, нишесте, алуминиеви оксиди, калций, бариев сулфат, йонообменни смоли и др. Носителят се използва при фино диспергирано състояние с размери от около 0.02-0.10 mm.
Като утайки, такива реагенти, които образуват нискоразтворими утайки с хроматографски йони, се използват например натриев йодид Nai, сулфид натриев Na2S, сребърен сулфат Ag2S04, калиев фероцианид К 4, оксихинолин, пиридин и др.
Обикновено, когато се използва методът на колона седиментна хроматография след преминаване през колоната на чист разтворител, се получават ясно разделени зони, всеки от които съдържа само един компонент (в случай на разтворимост на валежите се различават най-малко три пъти). Методът се характеризира с добра възпроизводимост на резултатите.
В случай на образуване на безцветни зони на утаяване, хроматограмата е показана или преминава през разработчик на колона-разработчик, който дава на утаяващи рисувани реакционни продукти или веднага въвежда разработчик в PF или в NF.
7.2 Хроматография на седименти на хартия
Помислете за същността на този метод върху примера за анализ на воден разтвор, съдържащ смес от медни катиони CU 2+? Желязо Fe 3+ и алуминиев al 3+.
В центъра на хартията, импрегнирана с утаен разтвор - калиев фероцианид К 4, капилярът се прилага с анализиран воден разтвор. CU 2+ и железни йони Fe 2+ взаимодействат с фероцианидни йони с образуването на слабо разтворими валежи:
2CU 2+ + 4-\u003e CU 2 (кафяв)
4FE 3+ + 3 4-\u003e FE4 (син)
Тъй като мед (II) фероцианид е по-малко разтворим от фероцианид на желязо (III), след това утайката на мед (II) фероцианид се отличава, образувайки централната кафяво зона. След това синята утайка от фероцианидно желязо (III), което придава на синята зона. Алуминиеви йони са преместени към периферията, давайки безцветна зона, тъй като те не образуват боядисани алуминиев фероцианид.
Схемата за разделяне CU2 +, FE3 + и AL3 + по метода на седиментна хроматография.
По този начин се получава първичната хроматограма, където зони за утаяване са частично припокриващи се.
След това се получава вторичната хроматограма. За тази цел, подходящ разтворител (в разглеждания случай е амоняк воден разтвор) се прилага от капиляра до центъра на основната хроматограмата. Разтворителят спонтанно се придвижва от центъра на хартията към периферията, който се пренася със себе си и се утаява при различни скорости: зоната на по-разтворима утайка от фероцианидно желязо се движи по-бърза зона на по-малко разтворим утайка на медния фероцианид. На този етап, поради разликата в скоростите на зоните за преместване, се появява тяхното по-ясно разделение.
За отваряне на алуминиеви йони, образуване на безцветна периферна зона, вторична хроматограма - спрей (от спрей) Разтвор на Alizhar - органичен реагент, образуващ се с алуминиеви йони розови продукти. Вземете външен розов пръстен.
8. Йонообменна хроматография
В йонообменна хроматография, отделянето на компонентите на сместа се постига чрез обратимо взаимодействие на йонизиращите вещества с групи с йонни сорбент. Запазването на електронното обзавеждане на сорбента се осигурява от наличието на противоотронки, способни на йонообмен, разположен в непосредствена близост до повърхността. Йон на въведената проба, взаимодействаща с фиксирания заряд на сорбент, обмен с противойон. Веществата, които имат различен афинитет към фиксиран заряд, са разделени на анионика или на катион. Анионатите са положително заредени групи по повърхността и сорбита от мобилната фаза на анионите. Катиаите съответно съдържат групи с отрицателен заряд, взаимодействат с катиони.
Като подвижна фаза се използват водни разтвори на киселинни соли, основи и разтворители на вида течен амоняк, т.е. Системи за разтворители, които имат високо значение на диелектричната константа и голяма тенденция към йонизират съединения. Обикновено работят с буферни разтвори, което позволява регулиране на стойността на рН.
Когато хроматографското разделяне на йони на анализираното вещество се конкурира с йони, съдържащи се в елуента, като се стреми да взаимодейства с противоположните заредени сорбент групи. Следва, че йонообменната хроматография може да се използва за разделяне на всички съединения, които могат да бъдат йонизирани по никакъв начин. Възможно е да се анализират дори неутрални захари молекули под формата на техните комплекси с боратен йон.
Хроматографията на йонообменността е необходима при разделянето на соковите вещества, които не могат да бъдат анализирани от GLC без превод на производни. Такива съединения включват аминокиселини, пептиди, захар.
Йонообменна хроматография се използва широко в медицината, биологията, биохимията, за контрол на околната среда, при анализиране на съдържанието на лекарства и техните метаболити в кръвта и урината, изкоренява в хранителни суровини, както и за отделяне на неорганични съединения, включително \\ t радиоизотопи, lantanoids, actinoids и др. Анализ на биополимери (протеини, нуклеинови киселини, и т.н.), които обикновено прекарани часове или дни, с помощта на йонообменна хроматография се извършва в 20-40 минути с по-добро разделяне. Използването на йонообменна хроматография в биологията направи възможно спазването на пробите директно в биоразрурванията, намалявайки възможността за прегрупиране или изомеризация, което може да доведе до неправилно тълкуване на крайния резултат. Интересно е да се използва този метод за контрол на промените, настъпили с биологични течности. Използването на порести слаби анионен обмен върху основата на силикагел направи възможно разделянето на пептиди. Механизмът на йонообменността може да бъде представен като следните уравнения:
за анионен обмен X - + R + Y - - Y - + R + X -
за катионна борса X + + R - Y + - Y + + R - X +
В първия случай, X-проба йон се конкурира с йон на подвижната фаза У - за йон центрове R + йонообменна смола, а във втория за конкуренция с йоните на фаза у мобилната + за йонни центрове R са катиони на пробата X +.
Естествено, йони на пробите, които са слабо взаимодействащи с йонен обменник, с тази конкуренция ще бъдат слабо съхраняват върху колоната и се промиват първо от него и, напротив, по-силно запазени йони ще елуират от колоната последния. Обикновено вторичните взаимодействия на не-йонна природа произтичат поради адсорбция или водородни връзки на пробата с не-йонната част на матрицата или поради ограничената разтворимост на пробата в подвижната фаза.
Разделянето на специфични вещества зависи предимно от избора на най-подходящия сорбент и мобилната фаза. Като фиксирана фаза в йонообменна хроматография се използват йонообменни смоли и силикагел с присадени йонни групи.
Полистиролни йонообменни смоли за HPLC зърно от 10 цт и по-малко притежават селективност и стабилност, но структурата на окото им, характеризираща се с разстоянието между отворите на окото от 1.5 пМ, което е значително по-малко от размера на порите, използвани за силикагел за силикагел адсорбционна хроматография (10 пМ), забавя прехвърлянето маса и, следователно, намалява значително ефективността. Йонообменните смоли, използвани в HPLC, са предимно съполимери на стирен и дивинил бензен. Обикновено се добавят 8-12% от последния. Колкото по-голямо е съдържанието на ди-винилбензол, толкова по-голяма е твърдостта и якостта на полимера, над капацитета и, като правило, селективност и по-малкото подуване.
Подобни документи
Общите характеристики на хроматографския процес. Физико-химични основи на тънкослойна хроматография, класификация на методите за анализ. Варианти на хроматография по фаза състояния. Контрол на качеството на хранителните продукти посредством TLC метод, оборудване.
курсова работа, добавена 12/27/2009
Явления, които се срещат по време на хроматография. Два подхода за обяснение са теорията за теоретичните плочи и кинетичната теория. Газ, течност, хартиена хроматография. Метод на йонообмен. Случаи на прилагане на йонообменна хроматография. Гелхроматография.
резюме, добавено 01/24/2009
Концепцията и структурата на полимерните сорбенти, историята на тяхното създаване и развитие, стойност в процеса на разпределителна хроматография. Видове полимерни сорбенти, възможностите за тяхното използване в изключителна хроматография. Характеристики на употребата на твърди гелове.
резюме, добавен 07.01.2010
Появата и развитието на хроматография. Класификация на хроматографски методи. Хроматография върху твърда фиксирана фаза: газ, течност (течна адсорбция). Хроматография върху течната фиксирана фаза: газ-течност и гел хроматография.
резюме, добавен 01.05.2009
Същността на метода на хроматография, историята на нейното развитие и видове. Обхват на хроматография, устройства или инсталации за хроматографско разделяне и анализ на смеси от вещества. Схемата на газовия хроматограф, нейните основни системи и принципа на експлоатация.
резюме, добавен 09/25/2010
Основи на метода на предавана хроматография. Газова хроматография е универсален метод за високо качество и количествен анализ на комплексни смеси и метод за производство на отделните компоненти в чист вид. Използването на облицовъчна газова хроматография.
курсова работа, добавена 01/09/2010
Същността и съдържанието на хроматография с йонна двойка, използването му в течна хроматография и екстракция за извличане на лекарства и техните метаболити от биологични течности в органичната фаза. Варианти на хроматография с йонна двойка, отличителни черти.
резюме, добавен 07.01.2010
Газната хроматография е една от най-обещаващите физикохимични изследвания, бързо развиваща се в момента. Класификация на хроматографски методи. Различни характерни признаци на процеса. Същността на хроматографските методи.
резюме, добавен 01/25/2010
Същността на високоефективната течна хроматография (HPLC) като метод за анализиране и разделяне на сложни примеси. Сорбенти, координация и наситени хелати; Моделите на влиянието на структурата на лиганда върху поведението на хелатите при условията на заразена хроматография.
резюме, добавен 11/10/2011
Концепцията и основните етапи на потока на хроматография за изключване, нейната принципна характеристика и обхват на приложение, сортове и техните отличителни черти. Характеристики на оборудването, използвано в процеса на изключителна хроматография.
Много открития от миналия век са длъжни на руския учен Mikhail цвят и неговия метод за хроматографски анализ. Голям брой изключителни изследователи го трябва да бъдат успехи и много и Нобелова награда!
"... без работата на Майкъл, няма да имаме нищо общо с всички" пигменти ", няма да има нищо общо ..." - тук е мнението на един известен английски учен.
Михаил Семенов цвят (1872-1919) - син на италиански и руския интелектуален. Той е роден в Италия в град Асти, недалеч от Торино. През 1891 г. Михаил завършва гимназията в Женева и влезе в Факултета по физика и Математика на Женевския университет. Представяне на дисертацията "Изследване на физиологията на килията. Материалите за познаване на движението на протоплазма, плазмените мембрани и хлоропластите" Цвят през октомври 1896 г. получил лекар на доктора на естествените науки. През декември същата година той идва в Санкт Петербург.
Михаил не знаеше, че стипендията на Женевската университет не е призната в Русия. Затова той трябваше да работи в известния ботаника Андрей Сергеевич Глимсин, който също проучи хлорофил, може да се каже на правата на птиците. В Санкт Петербург, цветът се запозна с други изключителни ботанически и растителни физиолози: i.p. Бородин, М.А. Воронин, а.н. Берково. Беше блестящо общество с оригинални богати на идеи за мислители и умели експериментатори. Цветът продължи да изследва хлоропластите, като се подготвя едновременно с новите изпити на магистърска степен и за защита на тезата. Той преминал изпита през 1899 г. и защити магистърската си теза в Университета в Казан на 23 септември 1901 година.
От ноември 1901 г. цветът работи като асистент на отдел "Анатомия" и физиологията на растенията във Варшава. В XI конгресът на натуралистите и лекарите, Михаил Семенов направи доклада "Методи и цели на физиологичния изследователски изследвания хлорофил", в който за първи път се съобщава за метода на адсорбционна хроматография.
Михаил Семенов е решил проблема за разделяне на зелени пигменти на листа и те са много близки от свойствата. В допълнение, има и други, много светли, пигменти - каротеноиди в листата. Благодарение на каротеноидите и на есенното жълт, портокал, се появяват пурпурни листа. Въпреки това, докато хлорофилите не са унищожени, беше почти невъзможно да ги отделят от каротеноиди.
Колко бележки yu.g. Чирков, "очевидно отварянето на цвета е реакция на съществуващите методи на груби и убийствени методи за тяхното разделяне. Ето една от техниките.
Първо, хлорофил алкохол екстракт се добива, след това три часа кипене с прибавяне на силен алкален (каустичен калий). В резултат на това хлорофил се разлага в композитни части - зелени и жълти пигменти.
Но в процеса на производство на тази отвара (почти алхимични манипулации), естественият хлорофил може да се срутят. И тогава изследователят би се занимавал с парчета от пигменти и дори с продуктите на тяхната химическа трансформация. "
За това как се е случило голямото откритие, пише с. Shnol: "Той взе стъклена тръба, напълни с прах от тебешир и наля малко алкохол екстракт от екстракт от листа на най-горния слой, и най-горния слой на колоната с тебешир е един и същи цвят И тогава MS започна да се излива. отгоре в тръба с креда чист алкохол. капка по капка. Друга част от разтворителя се елуира с пигменти от зърна зърно, което се премества надолу по тръбата. Там пресни грам гробове адсорбирани пигменти и от своя страна ги изведе до нови порции разтворителя. по силата на няколко различни адсорбционната сила (лекота на елуиране) Пропуснато с подвижен разтворител, различни пигменти придвижва по колона креда с различни скорости и образува хомогенен боядисани ивици на чисти вещества в колоната креда. беше красиво. в ярко зелена лента, лентата на жълти жълти - това са два типа хлорофил -. и ярки жълто-оранжеви barotinoids M.S. нарича тази картина хроматограма ".
"Цветът показа, - пише Чирков - че когато овце разтваря растителни пигменти през слой от безцветно порест сорбент, отделните пигменти са разположени под формата на латекс зони - всеки пигмент има собствен цвят или поне сянка сорбент прах (. тя може да бъде креда, захар на прах ...) адсорбция (повърхностно абсорбира: Латинска adSorbere средства "за гълтане") различни пигменти с неравно мощност:. някои могат да "приплъзване" с разтвор ток нататък, други ще бъдат задържани близо Така слоят -в-закон боядисан сорбент цвят, наречен хроматограма и метод - хроматография ".
Така се решава привидно неподатната задача. Методът беше изобретателен прост. Във всички случаи не е подобно на обемист, като се искат големи реактивни процедури, прилагани преди.
Може би тази простота е причинила факта, че повечето от съвременниците или не възприемат това невероятно откритие, или, което все още е тъжно, бунтусното срещу автора си.
Но всичко време се поставя на място. Цвят изобретен хроматография за изследвания на хлорофил. Първо е разпределил вещество, наречено хлорофил алфа и хлорофил бета. Оказа се, че е подходящо за изследвания не само пигменти, но и от безцветни, неоцветени смеси - протеини, въглехидрати. За шейсетте от Хроматографията на ХХ век бяха посветени няколко хиляди проучвания. Хроматографията се превърна в универсален метод.
"... Принципът на хроматографското разделяне на веществата, открито с М. цвят, е в основата на набора от различни методи за хроматографски анализ. Без неговото използване повечето от постиженията в науката и техниката на 20-ти век биха били невъзможни .. .
В основата на всичко това е една обща идея. Тя е проста. Това по същество е идеята за геометрична прогресия. Нека има две вещества много близки във всичките му свойства. Нито едно отлагането, нито екстракцията, нито адсорбцията се разделят в забележима степен. Нека едно вещество се адсорбира на повърхността, например, калциев карбонат (т.е. по-малко от 1%).
С други думи, неговото съдържание на адсорбент ще бъде 0.99 от съдържанието на другото. Ние третираме адсорбент чрез всеки разтворител, така че десорбцията (изключването) и елуирането (зачервяване) на двете вещества и и двете ще се движат от адсорбент към разтворителя и ние преместваме това получаване на прясна част от адсорбент. След това делът на първото вещество върху повърхността на адсорбент отново ще бъде 0.99 от съдържанието на второто, т.е. частта е адсорбирана, равна на 0.99 х 0.99 \u003d 0.98 от първоначалното количество. Още веднъж ще извършим елуиране и отново адсорбция - сега делът на първото вещество ще бъде 0.98 x 0.99 \u003d 0.97 от съдържанието на втория. За да може съдържанието на първото вещество на следващата част от адсорбент, само 1% от съдържанието на второто, ще бъде необходимо да се повтори абсорбционният цикъл на елуиране от около 200 пъти ...
Идеята за многократна разговор за разделяне на веществата може да бъде модифицирана в многократно преразпределение на сместа от вещества в системата на нездрави разтворители. Това е в основата на разпределителната хроматография. Същата идея е в основата на настоящите методи на електрофореза, когато сместа от вещества се движи при различни скорости на различни адсорбенти в електрическото поле.
1. ВЪВЕДЕНИЕ.
2. Появата и развитието на хроматография.
3. Класификация на хроматографски методи.
4. Хроматография върху твърда фиксирана фаза:
а) хроматография върху газ (газ-адсорбция;
б) хроматография върху течност (течност).
5. Хроматография върху фиксираната фаза на течността:
а) газово-течна хроматография;
б) гел хроматография.
6. Заключение.
Като лъчи на спектъра, различните компоненти на сместа от пигменти са естествено разпределени в колоната въглероден диоксид, позволявайки на нейното качествено и количествено определяне. Лекарството, получено по този начин, наричам хроматограма и предложения метод - хроматография.
М. С. Цвят, 1906
Въведение
С необходимостта да се разделят и анализират сместа от вещества, е необходимо да се изправят не само на химика, но и на много други специалисти.
В мощен арсенал от химически и физикохимични методи за разделяне, анализ, изследване на структурата и свойствата на отделни химични съединения и техните сложни смеси, едно от водещите места заема хроматография.
Хроматографията е физико-химичен метод за разделяне и анализ на смеси от газове, пари, течности или разтворени вещества и определяне на физикохимичните свойства на отделните вещества въз основа на разпределението на споделените компоненти на смесите между двете фази: подвижни и фиксирани. Вещества, които съставляват фиксираната фаза, се наричат \u200b\u200bсорбенти. Фиксираната фаза може да бъде твърда и течност. Мобилната фаза е поток от течност или газ, филтрува се през сорбентния слой. Мобилната фаза изпълнява функциите на разтворителя и носителя на анализираната смес от вещества, преведени в газообразно или течно състояние.
Има два вида сорбция: адсорбция - абсорбция на твърди вещества и абсорбция - разтваряне на газове и течности в течни разтворители.
2. Тя е възникналахроматография и развитие и развитие
Появата на хроматография като научен метод е свързана с името на изключителния руски учен Михаил Семенович цветове (1872 - 1919), който през 1903 г. откри хроматография по време на изследването на механизма за трансформиране на слънчевата енергия в растителни пигменти. Тази година трябва да се счита за датата на създаване на хроматографския метод.
ГОСПОЖИЦА. Цветът премина с разтвора на анализираните вещества и подвижната фаза през адсорбирания стълб, разположен в стъклена тръба. В това отношение неговият метод получи името на колонна хроматография. През 1938 г. N.A. Измайлов и М.А. Schreiber предложи метода на цветовете и извършва отделянето на сместа от вещества на плочата, покрита с тънък слой от адсорбент. По този начин се появява тънкослойна хроматография, което дава възможност да се анализира микроколизмът на веществото.
През 1947 г. TB. Gapon, напр. Gapon и f.m. За първи път се извършва хьоматографско отделяне на смес от йони в разтвор, което обяснява присъствието на обменна реакция между сорбент йони и йони, съдържащи се в разтвор. Така, друга посока на хроматография е отворена хроматография върху йонообмен. Понастоящем йонообменната хроматография е една от най-важните направления на хроматографския метод.
E.N. и G. B. Gapon през 1948 г., изпълнена от M.S. Идеята за възможността за хроматографско отделяне на смес от вещества въз основа на разликата в разтворимостта на твърдоразтворими утайки. Имаше седиментна хроматография.
През 1957 г. М. Голай предложи да нанесе сорбент на вътрешните стени на капилярната тръба - капилярна хроматография. Този вариант ви позволява да анализирате микроколизма на многокомпонентни смеси.
През 60-те години имаше възможност да се синтезират както йонни, така и незаредени гелове, които имат строго определени размери на порите. Това позволи да се разработи опция за хроматография, чиято същност се състои в разделяне на сместа от вещества въз основа на разликата в способността им да проникнат в гел-гел хроматография. Този метод ви позволява да разделяте смесите на веществата с различно молекулно тегло.
В момента хроматографията е натрупала значително развитие. Днес, различни методи за хроматография, особено в комбинация с други физически и физикохимични методи, помагат на изследователите и инженерите да решават най-различните, често много сложни задачи в научните изследвания и техника.
3. Classifik.хроматографски методи
Разнообразието от модификации и варианти на метода на хроматография изисква тяхната систематизация или класификация.
Основата на класификацията може да бъде поставена на различни признаци, а именно:
1. обобщеното състояние на фазите;
2. механизмът за разделяне;
3. метода за провеждане на процеса;
4. целта на процеса.
Класификация от съвкупното състояние на фазите:
газ (подвижна фаза - газ), газово-течност (подвижна фаза - газ, фиксирана фаза - течност), течна (подвижна фаза - течна) хроматография.
Класификация чрез механизъм за разделяне.
Адсорбционната хроматография се основава на селективна адсорбция (абсорбция) на отделните компоненти на смесената смес с подходящи адсорбенти. Адсорбционната хроматография е разделена на течна (течност-адсорбционна хроматография) и газ (газо-адсорбционна хроматография).
Хроматографията на йонообменната хроматография се основава на използването на йонообменни процеси между движимите йони на адсорбент и електроливите йони, когато разтворът на аналита се анализира през колоната, напълнена с йонообменно вещество (IONITE). Ионитите са неразрешими неорганични и органични съединения с високо молекулно тегло. Алуминиевият оксид се използва като йонити, пермутит, сулфуггол и различни синтетични органични йонообменни вещества - йонообменни смоли.
Седиментната хроматография се основава на различна разтворимост на утаяването, образувано от компонентите на анализираната смес със специални реагенти. Например, когато разтворът на сместа от NG (II) и PB соли се прекарва през колона с носач, предварително импрегниран с Ki разтвор, се образуват 2 цветни слоя: горната, боядисана в оранжево-червено (HGI 2), \\ t и дъното, боядисано в жълто (PBI 2).
Класификация съгласно процеса на провеждане на процеса.
Колонна хроматография е тип хроматография, в която се използва колона като носител за фиксиран разтворител.
Хартиената хроматография е тип хроматография, в която ленти или листове от филтърна хартия, които не съдържат минерални примеси, се използват като носител за фиксиран разтворител вместо говорител. В този случай, например капка от тестов разтвор, например, смес от разтвори на Fe соли (III) и Ко (II), се прилага към ръба на хартиените ленти. Хартията се суспендира в затворена камера (фиг. 1), спускайки ръба му с капка от изпитвателния разтвор в съд с подвижен разтворител, например с N-бутилов алкохол. Подвижен разтворител, движещ се през хартия, го изсмуква. В този случай всяко вещество, съдържащо се в анализираната смес с присъщата на скоростта, се движи в същата посока като разтворителя. След завършване на отделянето на йони, хартията се суши и след това се напръсква с реагент, в този случай с разтвор К 4, който образува боядисани съединения с отделни вещества (синьо - с железни йони, зелени - с кобалтови йони). Зоните, образувани с всичко това под формата на боядисани петна, ви позволяват да установите наличието на отделни компоненти.
Хартиената хроматография в комбинация с употребата на органични реагенти дава възможност да се извърши качествен анализ на сложни смеси от катиони и аниони. На една хроматограма, с помощта на един реагент, могат да бъдат открити редица вещества, тъй като се характеризира не само със съответното оцветяване, но и определено място за местоположение върху хроматограмата.
Тънкослойната хроматография е вид хроматография в неговия механизъм за разделяне, подобен на хартиената хроматография. Разликата между тях се крие във факта, че вместо листа хартия, разделянето се извършва върху плочи, покрити с тънък слой сорбент, изработен от прахообразен алуминиев оксид, целулоза, зеолити, силикагел, кизелур и др. и задържане на фиксиран разтворител. Основното предимство на тънкослойната хроматография е лесността на оборудването, простотата и високата скорост на експеримента, достатъчна яснота на отделянето на сместа от вещества и в способността да се анализира ултрамикроколизмът на веществото.
Класификация за целите на хроматографския процес.
Хроматографията има най-голяма стойност като метод за качествен и количествен анализ на смеси от вещества (аналитична хроматография).
Препаративна хроматография - вид хроматография, при която се произвежда отделянето на сместа от вещества в препаративни цели, т.е. За повече или по-малко значителни количества вещества в чист, без примеси. Задачата на препаративната хроматография може също да бъде концентрирана и последваща освобождаване от сместа от вещества, съдържащи се под формата на microstrum до основното вещество.
Неин анализатната хроматография е вид хроматография, която се използва като метод на научни изследвания. Използва се за изследване на свойствата на системите, като решения, кинетика на химически процеси, свойства на катализатори и адсорбенти.
Така, хроматографията е универсален метод за анализ на смеси от вещества, произвеждащи вещества в чиста форма, както и метод за изследване на свойствата на системите.
4. Хроматограффиксиране на твърда фиксирана фаза
но)Газ (G.азо Адсорбявация) Хроматография
Газова хроматография - хроматографски метод, при който мобилната фаза е газ. Газната хроматография получава най-голямото приложение за разделяне, анализ и изследване на вещества и техните смеси, движещи се без разлагане в състояние на пари.
Един от варианта на газовата хроматография е газо-адсорбционна хроматография - това е метод, при който фиксираната фаза е твърд адсорбент.
В газовата хроматография като подвижна фаза (газов носител) използва инертен газ: хелий, азот, аргон, значително по-малък от водород и въглероден диоксид. Понякога газовият газ служи на чифт летливи течности.
Газов хроматографският процес обикновено се извършва в специални устройства, наречени газови хроматографи (фиг. 3). Във всяка от тях има система за поток от газ, система за приготвяне и вмъкване на изследваната смес, хроматографска колона с система за управление на температурата, анализираща системата (детектор) и система за регистриране на резултатите от разделянето и Анализ (рекордер).
Температурата в газо-адсорбционната хроматография има температура. Неговата роля се състои главно в променянето на равновесието на сорбцията в газовата система - твърдо вещество. От правилния избор на температурата на колоната зависи, степента на отделяне на компонентите на сместа и ефективността на колоната и общата скорост на анализа. Има известен температурен диапазон на колоната, в която хроматографският анализ е оптимален. Обикновено, този интервал на температура се намира в регион близо до точката на кипене на химичното съединение. Когато точките на кипене на компонентите на сместа се различават значително между тях, нанесете температурата на температурата на колоната.
Разделянето на хроматографската колона е най-важната, но предварителна работа на целия процес на газов хроматографски анализ. Над двоичните смеси (газов газ - компонент) попадат в детектиращото устройство. Тук има преобразуване на промени в концентрациите на компонентите във времето в електрически сигнал, записани с помощта на специална система под формата на крива, наречена хроматограма. Резултатите от целия опит до голяма степен зависят от правилния избор на вида на детектора, неговия дизайн. Има няколко класификации на детектори. Различни диференциални и интегрални детектори. Диференциалните детектори регистрират моментната стойност на една от характеристиките (концентрация или поток) във времето. Интегралните детектори обобщават количеството вещество за определен период от време. Детекторите се използват и в принципа на действие, чувствителност и цел: термокондикантност, йонизация, спектроскопски, масспектрометрични, капулометрични и много други.
Прилагане на хроматография с газ-адсорбция
Хроматографията на газ-адсорбцията се използва в химическата и нефтохимическата промишленост за анализ на продуктите на химическия и нефтохимическия синтез, съставът на маслени фракции, определящ чистотата на реагентите и съдържанието на ключови продукти на различни етапи от технологични процеси и др.
Анализ на постоянни газове и леки въглеводороди, включително изомери, газов хроматография заема 5 до 6 минути. По-рано, на традиционните газови анализатори, този анализ продължи 5 до 6 часа. Всичко това доведе до факта, че газов хроматографията започва да се използва широко не само в изследователски институти и контролни и измервателни лаборатории, но и в системата на цялостна автоматизация на промишлените предприятия.
Днес газов хроматография се използва при търсене на нефтени и газови полета, което позволява да се определи съдържанието на органични вещества, които показват близостта на петролните и газовите полета, избрани от почвени проби.
Газовата хроматография се използва успешно в криминалистика, където се използва за установяване на идентичността на проби от петна от кръв, бензин, масла, фалшиви скъпи храни и др. Много често се използва газов хроматография за определяне на съдържанието на алкохол в кръвта на шофьорите на автомобили. Няколко капки кръв от пръста достатъчно, за да разберат колко кога и какво пие алкохол, той пиеше.
Газната хроматография ви позволява да получите ценна и уникална информация за състава на миризмите на храна, като сирене, кафе, хайвер, бренди и т.н. Понякога информацията, получена от газовия хроматографска анализ, не е щастлива. Например, често в хранителните продукти, ненужно е от пестициди или плодов сок, съдържащ трихлоретилен, който противоречи на забрани, се използва за увеличаване на степента на каротин от плодове и др. Но тази информация защитава човешкото здраве.
Въпреки това, често има случаи, когато хората просто пренебрегват получената информация. Преди всичко се отнася до тютюнопушенето. Подробен газов хроматографски анализ отдавна установява, че пушенето на цигари и цигари съдържа до 250 различни въглеводорода и техните производни, от които около 50 имат канцерогенен ефект. Ето защо пушачите имат рак на белия дроб в 10 пъти по-често, но все още милиони хора продължават да се отровиха себе си, техните колеги и роднини.
Газната хроматография се използва широко в медицината, за да се определи съдържанието на множество лекарства, определящи нивото на мастни киселини, холестерол, стероиди и др. В тялото на пациента. Такива анализи осигуряват изключително важна информация за състоянието на човешкото здраве, хода на заболяването му, ефективността на използването на някои лекарства.
Научни изследвания в металургията, микробиологията, биохимията, в развитието на растителна защита и нови лекарства, в създаването на нови полимери, строителни материали и в много други различни области на човешката практическа дейност е невъзможно да се представи без такъв мощен аналитичен метод като газ хроматография.
Газната хроматография се използва успешно за определяне на съдържанието на полициклични ароматни съединения, опасни за човешкото здраве, във вода и във въздуха, нивото на бензина във въздуха на равнините на бензиностанциите, състава на изгорелите газове във въздуха и др.
Този метод е широко използван като един от основните методи за наблюдение на чистотата на околната среда.
Газната хроматография заема важно място в нашия живот, което ни осигурява колосално количество информация. В националната икономика и в изследователските организации се използват повече от 20 хиляди газови хроматографи, които са необходими помощници при решаването на много сложни задачи, ежедневно произтичащи от изследователи и инженери.
б)Течност (ликвидна адсорбция)хроматография
Течната хроматография е група от хроматографски варианти, в които подвижната фаза е течна.
Едно изпълнение на течна хроматография е ликвидсорбционна хроматография - това е метод, при който фиксираната фаза е твърда адсорбент.
Въпреки че течната хроматография е отворена по-рано от газ, тя само през втората половина на ХХ век влезе в периода изключително интензивно развитие. Понастоящем, според степента на развитие на теорията на хроматографския процес и техники на инструменталния дизайн, според ефективността и скоростта на разделяне, е малко вероятно да се откаже от метода на газовия хроматографски раздяла. В същото време всеки от тези два основни вида хроматография има свой първичен обхват. Ако газов хроматография е подходяща за анализ, разделяне и изследване на химикали с молекулно тегло 500 - 600, тогава течната хроматография може да се използва за вещества с молекулно тегло от няколко стотин и няколко милиона, включително изключително сложни макромолекули на полимери, протеини и нуклеинови киселини. В същото време, противопоставянето на различни хроматографски методи е присъщо лишено от здрав разум, тъй като хроматографските методи са успешно допълнени един от друг и самата задача на конкретно проучване е необходимо да се подходи по различен начин, а именно какъв хроматографски метод Позволява ви да го решите с повече скорост, информативност и с по-малко разходи.
Както при газова хроматография, детекторите се използват в модерна течна хроматография, която непрекъснато да се прикрепи концентрацията на определеното вещество в потока на течността, изтичаща от колоната.
Универсалният детектор за течна хроматография не съществува. Следователно във всеки конкретен случай той трябва да бъде избран в най-големия детектор на Съюза. Ултравиолетовите, рефрактометрични, микро лекарства детектори, детектори за рефракция са най-големи.
Спектрометрични детектори. Детекторите от този тип са силно чувствителни селективни устройства, позволяващи много малки вещества концентрации в потока на течната фаза. Тяхното свидетелство зависи малко върху температурните колебания и други случайни промени в средата. Една от важните характеристики на спектрометричните детектори е прозрачността на повечето разтворители, използвани в ликвидната адсорбционна хроматография в работната зона на дължини на вълните.
Най-често се използва абсорбция в UV, по-рядко в IR региона. В UV региона се използват уреди, работещи в широк диапазон - от 200 nm до видимата част на спектъра, или върху определени дължини на вълните, най-често при 280 и 254 nm. Луковиците с ниско налягане на живак (254 nm), средно налягане (280 nm) и съответните филтри се използват като източници на радиация.
Микросторпизиращи детектори. Основата на детекторите на микроцелността се основава на освобождаването на топлина по време на адсорбцията на веществото върху адсорбент, който се пълни с детекторната клетка. Той обаче се измерва, а не топлината, а температурата на адсорбент, към която се нагрява в резултат на адсорбция.
Чистоцерният детектор е доста силно чувствителен инструмент. Неговата чувствителност зависи преди всичко от топлината на адсорбция.
Микросетерните детектори са универсални, подходящи за откриване на органични и неорганични вещества. В същото време те са трудни за получаване на доста ясни хроматограми, особено с непълното отделяне на компонентите на сместа.
5. Хроматографатия на течна фиксирана фаза
а) газово-течна хроматография
Газо-течна хроматография - газов хроматографски метод, при който фиксирана фаза е млада течност, приложена към твърд носител.
Този тип хроматография се използва за отделяне на газове и пари от течности.
Основната разлика в газовата течност от газо-адсорбционна хроматография е, че в първия случай методът се основава на използването на процеса на разтваряне и последващо изпаряване на газа или пара от течния филм, държан от твърдия инертен носител; Във втория случай процесът на разделяне се основава на адсорбция и последваща десорбция на газ или пара на повърхността на твърдата адсорбент.
Хроматографският процес може да бъде схематично представен, както следва. Смес от газове или изпарения от летливи течности се инжектира с поток на носещ газ в колона, напълнена с фиксиран инертен носител, върху който е разпределен нелетлив течност (фиксирана фаза). Изследваните газове и двойки се абсорбират от тази течност. След това компонентите на споделената смес се изместват селективно в определен ред от колоната.
В газово-течна хроматография се използват няколко детектори, специфично реагиращи на всякакви органични вещества или върху органични вещества със специфична функционална група. Те включват йонизационни детектори, електронни детектори за улавяне, термични, спектрофотометрични и някои други детектори.
Детектор за йонизация (PID). Работата на PID се основава на факта, че органичните вещества, попадащи в пламъка на горелката за водород, са обект на йонизация, в резултат на което йонизацията е едновременно йонизация, която е едновременно йонизационна камера, която е пропорционална на броя на заредените частици.
PID е чувствителен само към органични съединения и не е чувствителен или много слабо чувствителен към такива газове като въздушен, сяра и въглеродни оксиди, сероводород, амоняк, въглерод, водна пара и на няколко други неорганични съединения. Нечувствителността на PID към въздуха позволява да го приложи за определяне на замърсяването на въздуха от различни органични вещества.
При работа с PID, се използва 3 газ: газов носител (хелий или азот), водород и въздух. Всички 3 газа трябва да имат висока степен на чистота.
Детектор на аргон. В детектора на аргона йонизацията се причинява от сблъсък на молекулите на определеното вещество с метастабилни аргонови атоми, произтичащи от ефектите на радиоактивното в радиация.
Термичен детектор. Принципът на термо-йонния детектор е, че солите на алкални метали, изпаряващи се в горелката на пламъка, селекват селективно със съединения, съдържащи халогени или фосфор. При липса на такива съединения в йонизационната камера на детектора е установено равновесие на атомите на алкални метали. Наличието на фосфорни атоми поради тяхната реакция с атомите на алкални метали нарушава този баланс и причинява появата в йонната текуща камера.
Тъй като топлинният детектор има най-висока чувствителност към връзките, съдържащи фосфор, той получава името на фосфата. Този детектор се използва главно за анализ на фосфородинорганични пестициди, инсектициди и редица биологично активни съединения.
б)Гел хроматограма.fIA.
Гел хроматография (гел филтрация) - метод за разделяне на смеси от вещества с различни молекулни тегла чрез филтриране на анализирания разтвор чрез напречни-омрежени клетъчни гелове.
Разделянето на сместа от вещества настъпва в случай, че размерите на молекулите на тези вещества са различни и диаметърът на гел зърната е постоянен и само тези молекули могат да преминат, размерите на които са по-малки от диаметъра на. \\ T гел пори. При филтриране на разтвора на смес от сместа, по-малките молекули, проникнали в порите на гела, се забавят в разтворителя, съдържащи се в тези пори, и се движат по геловия слой по-бавно от големите молекули, които не са способни да проникнат в порите. Така гел хроматографията ви позволява да отделите сместа от вещества в зависимост от размера и молекулното тегло на частиците на тези вещества. Този метод на разделяне е доста прост, бърз и най-важното, той ви позволява да отделяте смеси от вещества при условия на тиня, отколкото други хроматографски методи.
Ако гел гранулите запълват колоната и след това се наливат разтвор на различни вещества с различно молекулно тегло в него, след това, когато разтворът се премества по геловия слой в колоната, тази смес ще се осъществи.
Началният период на опита: прилагане на разтвора на анализираната смес върху геловия слой в колоната. Вторият етап - гел не пречи на дифузията на малки молекули в порите, най-големите молекули остават в разтвор около геловите гранули. Когато се промива със слой гел с чист разтворител, големи молекули започват да се движат със скорост близо до скоростта на движението на разтворителя, докато малките молекули трябва първо да предофекнат от вътрешната възраст на гела в обема между зърната и като Резултатът от това се забавя и отмива с разтворителя по-късно. Настъпва смес от вещества според тяхното молекулно тегло. Настъпва измиване от колоната, за да се намали тяхното молекулно тегло.
Използването на гел хроматография.
Основната цел на гел хроматография е отделянето на смеси от високомолекулни съединения и определяне на молекулното разпределение на полимерите.
В същото време се използва еднакво гел хроматография за разделяне на сместа от вещества със средно молекулно тегло и дори с ниско молекулни връзки. В този случай е важно гел хроматографията да позволи да се отделят при стайните температури, което благоприятно го отличава от газо-течна хроматография, изискваща нагряване за прехвърляне на анализираните вещества в парата фаза.
Разделянето на сместа от вещества чрез гел хроматография е възможно и когато молекулните тегла на анализираните вещества са много близки или дори равни. В този случай се използва взаимодействието на разтворените вещества с гел. Това взаимодействие може да бъде толкова значимо, което намалява разликите в размерите на молекулите. Ако естеството на взаимодействието с гела за различни вещества е не IDAS, тази разлика може да се използва за отделяне на смес от интерес.
Пример за това е използването на гел хроматография за диагностициране на заболявания на щитовидната жлеза. Диагнозата се определя от броя йод, определен по време на анализа.
Горните примери за използването на гел хроматография показват своите достатъчно възможности за решаване на голямо разнообразие от аналитични задачи.
Заключение
Като научен метод за обучение около нас, хроматографията непрекъснато се развива и подобрява. Днес тя се прилага толкова често и широко в научни изследвания, медицина, молекулярна биология, биохимия, технологии и национална икономика, което е много трудно да се намери областта на знанието, в която няма да се използва хроматография.
Хроматографията като метод на изследване с изключителните му възможности е мощен фактор при знанието и трансформацията на усложняващ свят в интерес на създаването на приемливи условия на човешко местообитания на нашата планета.
С P и с на пътL и t e r и t u r s
1. Ивазов Б.в. Въведение в хроматография. - m.: По-високо. SK., 1983 - s. 8-18, 48-68, 88-233.
2. Кресков А.П. Основи на аналитичната химия. Теоретична основа. Качествен анализ, първата книга, ED.4-E, отдих. М., "Химия", 1976 - стр. 119-125.
3. Sakodynsky k.i., Orekhov b.i. Хроматография в науката и технологиите. - m.: Знание, 1982 - s. 3-20, 28-38, 58-59.