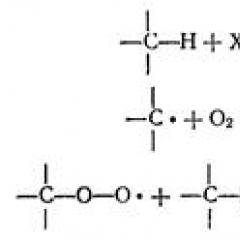
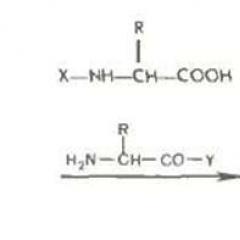
Desarrollo de la cromatografía. Cromatografía como método de investigación.
La cromatografía es un científico ruso, botánica y fisicoquímista de Mikhail Semenovich Color.
El descubrimiento de la cromatografía se refiere al momento de finalización del trabajo en la tesis del maestro en San Petersburgo (1900 - 1902) y el primer período de trabajo en Varsovia (1902 - 1903). Explorando los pigmentos de las plantas, el color pasó la solución de la mezcla muy poco diferente en el color de los pigmentos a través del tubo lleno de un carbonato de calcio en polvo en polvo, y luego se lavó el adsorbente con un solvente limpio. Los componentes separados de la mezcla se dividieron y formaron rayas de colores. Según la terminología moderna, el color descubrió la variante de cromatografía en desarrollo (desarrollando cromatografía de adsorción líquida). Los principales resultados de la investigación sobre el desarrollo de la cromatografía creada por él. Color descrito en el libro "Chromophyls en la planta y el mundo animal" (1910), que es su disertación de doctorado. Intercambio de iones sedimentarios de gas de cromatografía
El color ha utilizado ampliamente el método cromatográfico no solo para la separación de la mezcla y estableciéndola multicomponencia, sino también para un análisis cuantitativo, para este propósito, se rompió la columna de vidrio y cortó la columna adsorbente a las capas. El color ha desarrollado equipos para cromatografía líquida, por primera vez realizó procesos cromatográficos a presión reducida (bombeo) y en alguna sobrepresión, desarrolló recomendaciones para la preparación de columnas eficientes. Además, introdujo muchos conceptos básicos y términos de un nuevo método, como "cromatografía", "manifestación", "desplazamiento", "cromatograma", etc.
La cromatografía se usó por primera vez en raras ocasiones, su período oculto duró aproximadamente 20 años, durante el cual apareció un número muy pequeño de mensajes sobre diversas aplicaciones del método. Y solo en 1931, R. Kunu (Alemania) A. WinterStein (Alemania) y E. Lederre (Francia), que trabajaron en un laboratorio químico (liderado por R. kun), el Instituto de Emperador Wilhelm en la investigación médica en Heidelberg, Se las arregló para asignar este método a y b-caroteno de caroteno crudo y, por lo tanto, demostrar el valor de la abertura del color.
Una etapa importante en el desarrollo de la cromatografía fue el descubrimiento de los científicos soviéticos n.A. Izmailov y M.S. Método Schreiber de cromatografía en una capa delgada (1938), que permite el análisis con el microcolismo de la sustancia.
El siguiente paso importante fue el descubrimiento de A. Martin y R. Cantar (Inglaterra) de la variante de cromatografía de distribución de líquidos en el ejemplo de la separación de derivados de acetilo de aminoácidos en una columna llena de gel de sílice, saturado con agua, utilizando cloroformo. como solvente (1940). Al mismo tiempo, se observó que no solo se puede usar líquido como fase móvil, sino también a gas. Unos años más tarde, se propuso a estos científicos para llevar a cabo la separación de derivados de aminoácidos para humedecerse con agua con butanol como la fase móvil. También implementaron el primer sistema de separación bidimensional. Para la apertura de la versión de distribución de la cromatografía, Martin y Sing recibió el Premio Nobel de Química. (1952). Además, Martin y A. James llevaron a cabo una variante de cromatografía de distribución de gas, separando la mezcla en un sorbente mixto de la silicona DS-550 y el ácido esteárico (1952 - 1953). A partir de este momento, el desarrollo más intensivo se obtuvo mediante método de cromatografía de gases.
Una de las variantes de cromatografía de gases es la cromantografía, para mejorar la separación de la mezcla de gas a la simultánea con el movimiento de la fase móvil: gas, afecta al sorbente y la mezcla separada con un campo de temperatura en movimiento que tiene un cierto gradiente en longitud ( AA Zhukhovitsky y Sotr., 1951).
La ciudad de Schwab (Alemania) presentó una contribución notable al desarrollo del método cromatográfico, que fue el fundador de la cromatografía de intercambio iónico (1937 - 1940). Ella recibió un mayor desarrollo en las obras de científicos soviéticos, E.N. GAPONA Y TB Gapona, que realizó una separación cromatográfica de una mezcla de iones en la solución (junto con FM Shemyakin, 1947), y también llevó a cabo la idea de la posibilidad de la separación cromatográfica de una mezcla de sustancias basadas en la diferencia en la solubilidad de la solubilidad. (Cromatografía sedimentaria, 1948).
El escenario moderno en el desarrollo de la cromatografía de intercambio iónico comenzó en 1975 después de la labor de la ciudad de Smallla, T. Stevens y W. Bauman (EE. UU.), En los que propusieron un nuevo método analítico llamado cromatografía de iones (una opción para altamente eficiente Intercambio de la cromatografía de iónes con detección condacométrica).
La creación de la compañía "Perkin-Elmer" M. Golley (EE. UU.) De la variante capilar de cromatografía (1956), en la que se aplica el sorbente a las paredes internas del tubo capilar, lo que permite analizar el microcolismo de las mezclas multicomponentes.
A finales de los 60. Mayor interés en la cromatografía líquida. Hubo cromatografía líquida altamente eficiente (HPLC). Esto fue facilitado por la creación de detectores altamente sensibles, nuevos sorbentes de polímeros selectivos, equipos nuevos, que permitieron operar a altas presiones. Actualmente, HPLC ocupa una posición de liderazgo entre otros métodos de cromatografía e implementado en varias versiones.
La cromatografía es un método de separación y determinación de sustancias basadas en la distribución de componentes entre las dos fases-forro y fijadas. La fase fija (estacionaria) sirve una sustancia porosa sólida (a menudo llamada sorbente) o una película líquida aplicada a un sólido. La fase móvil es un líquido o gas que fluye a través de una fase fija, a veces bajo presión. Los componentes de la mezcla de la mezcla (núcleo) junto con el movimiento de fase móvil a lo largo de la fase estacionaria. Por lo general, se coloca en un tubo de vidrio o metal, llamado columna. Dependiendo de la fuerza de interacción con la superficie sorbente (debido a la adsorción o por cualquier otro mecanismo), los componentes se moverán a lo largo de la columna a diferentes velocidades. Algunos componentes permanecerán en la capa superior del sorbente, otros, en menor medida, interactuarán con el sorbente, estarán en la parte inferior de la columna, y algunos dejarán la columna junto con la fase móvil (tales componentes no se pagan, y Su tiempo de espera determina los altavoces de "tiempo muerto").
Por lo tanto, se produce la rápida separación de mezclas complejas de componentes.
Apertura de la historia:
Nacimiento de la cromatografía.
En la tarde de este día, en una reunión del Departamento Biológico de la Sociedad de Varsovia de Naturalistas, asistente del Departamento de Anatomía y Fisiología de la Planta Mikhail Semenovich fue realizado por el informe "en una nueva categoría de fenómenos de adsorción y en el uso de ellos al análisis bioquímico ".
Desafortunadamente, M.S. Tsvet, que está en la formación de botánica, no apreció el aspecto analítico químico de su apertura como un poco, y poco publicó su trabajo en revistas químicas. Posteriormente, fueron químicos los que apreciaron la escala real de los M.s.S. propuestos. El color del método cromatográfico, que se ha convertido en el método más común de química analítica.
Se deben enfatizar los siguientes detalles de los métodos cromatográficos:
1. La separación es dinámica, y se repiten los actos de extracción-desorción de componentes compartidos repetidos. Esto causa una eficiencia significativamente mayor de cromatográfico.
separación en comparación con los métodos de sorción estática y
extracción.
2. Durante la separación, se utilizan varios tipos de interacción de los sorbatos y las fases estacionarios: de puramente físico a la hemosorción.
Esto provoca la posibilidad de separación selectiva de un amplio rango.
3. En las sustancias separadas, puede aplicar varios campos adicionales (gravitacionales, eléctricos, magnéticos, etc.), que, cambiando las condiciones de separación, expandan las posibilidades de cromatografía.
4. La cromatografía es un método híbrido que combina la separación simultánea y la definición de varios componentes.
5. La cromatografía le permite resolver ambas tareas analíticas (separación, identificación, definición) y preparativas (limpieza, selección, concentración). La solución de estas tareas se puede combinar realizándolos en el modo "en línea".
Numerosos métodos se clasifican por el estado agregado de las fases, el mecanismo de separación y la técnica de la separación.
Los métodos cromatográficos difieren en el método de llevar a cabo.
el proceso de separación en el frente, crucial y eluyente.
Cromatografía iónica
La cromatografía de iones es una cromatografía líquida altamente eficiente para separar los cationes y los aniones en los intercambiadores de iones
capacidad baja. Cromatografía de iones generalizados.
debido a la cantidad de sus ventajas:
- la capacidad de determinar un gran número de inorgánicos y
iones orgánicos, así como simultáneamente definir cationes y
- Alta sensibilidad de la determinación (hasta 1 ng / ml sin
concentración preliminar;
- Alta selectividad y expresividad;
- pequeño volumen de la muestra analizada (no más de 2 ml de muestra);
- una amplia gama de concentraciones definidas (desde 1 ng / ml a
- la posibilidad de usar varios detectores y sus combinaciones, lo que hace posible proporcionar selectividad y definición de tiempo pequeña;
- la capacidad de automatizar completamente la definición;
- En muchos casos, la ausencia completa de preparación preliminar de la muestra.
Al mismo tiempo, como cualquier método analítico, la cromatografía de iones no está desprovista de deficiencias, que pueden atribuirse a:
- la complejidad de la síntesis de los intercambiadores de iones, que se complica enormemente
desarrollo del método;
- menor eficiencia de la separación en comparación con HPLC en comparación con HPLC;
- La necesidad de alta resistencia a la corrosión.
sistema cromatográfico, especialmente al determinar.
cationes.
2.1 Historial de desarrollo:
El estudio de los procesos de intercambio de iones comenzaron a principios del siglo XIX. Con observaciones sobre el efecto de los suelos en la composición química de las soluciones de sal en contacto con él. A fines de la década de 1940, Tompson señaló que el suelo absorbe el amoníaco de los fertilizantes orgánicos ingresados, los experimentos relevantes fueron llevados a cabo por el especialista de su York D. Spence. Los primeros resultados de los experimentos D. SPENSE fueron publicados por G. Thompson en 1850. El artículo señala que "el primer descubrimiento de las propiedades de alta calidad del suelo apenas puede fallar tan útil para la agricultura" y su último trabajo fue publicado e en 1852 y 1855.
2.3 Principios de separación de iones en procesos de sorción.
La cromatografía de intercambio de iones se refiere a la cromatografía líquida-fase de fase sólida, en la que la fase móvil es un líquido (eluyente), y una fase fija es un sólido (intercambiador de iones). El método de cromatografía de intercambio iónico se basa en un proceso de reemplazo dinámico de iones asociados con una fase fija, iones eluyentes que ingresan a la columna. La separación se produce debido a la diferente afinidad por el intercambio de iones de iones en la mezcla, lo que conduce a diferentes velocidades de su movimiento a lo largo de la columna.
La cromatografía de iones es una variante de la cromatografía de intercambio de iones de columna.
De acuerdo con las recomendaciones de JUPAK (1993), los términos de intercambio de iones (COI) y la cromatografía iónica (su) se definen de la siguiente manera. "La cromatografía de intercambio de iones se basa en la diferencia en las interacciones de intercambio de iones para sustancias analizadas individuales. Si los iones están separados y se pueden detectar utilizando un detector de conductores o detección de UV indirecta, entonces se llama cromatografía de iones".
Redacción moderna (2005): "La cromatografía de iones incluye toda la separación cromatográfica líquida de alto rendimiento (HPLC) de iones en las columnas, combinada con la detección directa en el detector de flujo y el procesamiento cuantitativo de las señales analíticas obtenidas". Esta definición caracteriza la cromatografía de iones sin referencia al mecanismo de separación y al método de detección y, por lo tanto, la separa del intercambio de iones clásicos.
Los siguientes principios de separación se aplican en la cromatografía de iones:
Intercambio iónico.
Educación de pares de iones.
Iones de exclusión.
Intercambio iónico
El intercambio de iones es una respuesta heterogénea reversible de los iones de ionización equivalentes en la fase ionata (contraiones), los sindicatos deluyentes. Los anti -ónones son sostenidos por los grupos funcionales de los IIONETs a expensas de las fuerzas electrostáticas. Como regla general, en cromatografía catiónica, estos grupos son grupos de ácidos sulfónicos; En el caso de la cromatografía aniónica - terrenos de amonio cuaternario. En la Fig. 1 muestra el esquema del proceso de intercambio de cationes y aniones. Los iones de la sustancia determinados están marcados como A, los iones eluyentes que compiten con ellos para los centros de intercambio - E.

Higo. 1. El intercambio de iones de cationes (A +) y aniones (A) en iones eluyentes (E + o E-) con la participación de un intercambiador de cationes que contienen grupos de sulfo funcional, SO3-, y Cambiador de aniones (base de amonio cuaternario Grupos -n + R3).
Educación del ion par
Para implementar este mecanismo de separación, se utilizan reactivos emparejados por iones, que se agregan a la solución eluyente. Tales reactivos son tensioactivos aniónicos o catiónicos, por ejemplo, ácidos alquilulfónicos o sales de tetralalklamonio.
Junto con los iones de iones de iones cargados opuestos, los iones de este reactivo de pareja de iones forman un par iónico desagradable, que se puede mantener en la fase fija debido a las interacciones intermoleculares. La separación se lleva a cabo debido a la diferencia en las constantes de la formación de pares iónicos y los grados de su adsorción en la matriz sorbente. En la Fig. 2 muestra un modelo de intercambio de iones estático en cromatografía de iones, después de la adsorción del reactivo en la fase fija. Este principio de separación se utiliza tanto para aniones como para cationes.

Higo. 2.. Modelo de intercambio iónico en cromatografía de vapor ión.
Exclusión iónica
Cromatografía en ioneseClusion (IEX). Básicamente, se utiliza para separar ácidos o bases débiles. El mayor valor de IEX tiene que determinar carboxílicos y aminoácidos, fenoles, carbohidratos.
En la Fig. 3 muestra el principio de separación utilizando IEX en el ejemplo de ácidos R-COOH.
Higo. 3. Esquema de separación de ácido carboxílico R-COOH con cromatografía de ionoecklusion.

En la cromatografía de ionoeckskoluzion como una fase fija, se usa a menudo un intercambiador de cationes totalmente aclarado, que contiene agua de iones (contraónimas). En una solución acuosa de eluyentes, se hidratan grupos de ácidos sulfónicos de ionis. La cubierta del hidrato se limita a una membrana cargada negativa imaginaria (membrana de Donnan). La membrana es permeable solo para moléculas no expulsadas (por ejemplo, agua).
Los ácidos carboxílicos orgánicos se pueden separar si se utilizan ácidos minerales fuertes como eluyentes. Debido a los bajos valores de las constantes de acidez, los ácidos carboxílicos están presentes en dichas soluciones en forma injusta. Estos formularios pueden pasar a través de la membrana de Donnan y adsorberse en la fase fija.
Envíe su buen trabajo en la base de conocimientos es simple. Usa el siguiente formulario
Los estudiantes, los estudiantes de posgrado, los jóvenes científicos que usan la base de conocimientos en sus estudios y el trabajo le estarán muy agradecidos.
publicado por http://www.allbest.ru.
1. Historia de la apertura y desarrollo de la cromatografía.
2. Disposiciones básicas.
3. Clasificación de los métodos de análisis cromatográfico.
4. Cromatografía de adsorción. Cromatografía de capa fina
4.1 Técnica de experimento en cromatografía de capa fina.
5. Cromatografía de gases.
5.1 cromatografía de adsorción de gas
5.2 cromatografía de gas-líquido.
6. Cromatografía de distribución. Cromatografía en papel
7. Cromatografía de sedimentos.
7.1 Clasificación de métodos de cromatografía sedimentaria sobre la técnica del experimento.
7.2 cromatografía de sedimentos sobre papel.
8. Cromatografía de intercambio iónico.
Conclusión
Bibliografía
1. HISTORIADescubrimientos y desarrollo de cromatografía.
La cromatografía es un científico ruso, botánica y fisicoquímista de Mikhail Semenovich Color.
El descubrimiento de la cromatografía se refiere al momento de finalización del trabajo en la tesis del maestro en San Petersburgo (1900 - 1902) y el primer período de trabajo en Varsovia (1902 - 1903). Explorando los pigmentos de las plantas, el color pasó la solución de la mezcla muy poco diferente en el color de los pigmentos a través del tubo lleno de un carbonato de calcio en polvo en polvo, y luego se lavó el adsorbente con un solvente limpio. Los componentes separados de la mezcla se dividieron y formaron rayas de colores. Según la terminología moderna, el color descubrió la variante de cromatografía en desarrollo (desarrollando cromatografía de adsorción líquida). Los principales resultados de la investigación sobre el desarrollo de la cromatografía creada por él. Color descrito en el libro "Chromophyls en la planta y el mundo animal" (1910), que es su disertación de doctorado. Intercambio de iones sedimentarios de gas de cromatografía
El color ha utilizado ampliamente el método cromatográfico no solo para la separación de la mezcla y estableciéndola multicomponencia, sino también para un análisis cuantitativo, para este propósito, se rompió la columna de vidrio y cortó la columna adsorbente a las capas. El color ha desarrollado equipos para cromatografía líquida, por primera vez realizó procesos cromatográficos a presión reducida (bombeo) y en alguna sobrepresión, desarrolló recomendaciones para la preparación de columnas eficientes. Además, introdujo muchos conceptos básicos y términos de un nuevo método, como "cromatografía", "manifestación", "desplazamiento", "cromatograma", etc.
La cromatografía se usó por primera vez en raras ocasiones, su período oculto duró aproximadamente 20 años, durante el cual apareció un número muy pequeño de mensajes sobre diversas aplicaciones del método. Y solo en 1931, R. Kunu (Alemania) A. WinterStein (Alemania) y E. Lederre (Francia), que trabajaron en un laboratorio químico (liderado por R. kun), el Instituto de Emperador Wilhelm en la investigación médica en Heidelberg, Se las arregló para asignar este método a y b-caroteno de caroteno crudo y, por lo tanto, demostrar el valor de la abertura del color.
Una etapa importante en el desarrollo de la cromatografía fue el descubrimiento de los científicos soviéticos n.A. Izmailov y M.S. Método Schreiber de cromatografía en una capa delgada (1938), que permite el análisis con el microcolismo de la sustancia.
El siguiente paso importante fue el descubrimiento de A. Martin y R. Cantar (Inglaterra) de la variante de cromatografía de distribución de líquidos en el ejemplo de la separación de derivados de acetilo de aminoácidos en una columna llena de gel de sílice, saturado con agua, utilizando cloroformo. como solvente (1940). Al mismo tiempo, se observó que no solo se puede usar líquido como fase móvil, sino también a gas. Unos años más tarde, se propuso a estos científicos para llevar a cabo la separación de derivados de aminoácidos para humedecerse con agua con butanol como la fase móvil. También implementaron el primer sistema de separación bidimensional. Para la apertura de la versión de distribución de la cromatografía, Martin y Sing recibió el Premio Nobel de Química. (1952). Además, Martin y A. James llevaron a cabo una variante de cromatografía de distribución de gas, separando la mezcla en un sorbente mixto de la silicona DS-550 y el ácido esteárico (1952 - 1953). A partir de este momento, el desarrollo más intensivo se obtuvo mediante método de cromatografía de gases.
Una de las variantes de cromatografía de gases es la cromantografía, para mejorar la separación de la mezcla de gas a la simultánea con el movimiento de la fase móvil: gas, afecta al sorbente y la mezcla separada con un campo de temperatura en movimiento que tiene un cierto gradiente en longitud ( AA Zhukhovitsky y Sotr., 1951).
La ciudad de Schwab (Alemania) presentó una contribución notable al desarrollo del método cromatográfico, que fue el fundador de la cromatografía de intercambio iónico (1937 - 1940). Ella recibió un mayor desarrollo en las obras de científicos soviéticos, E.N. GAPONA Y TB Gapona, que realizó una separación cromatográfica de una mezcla de iones en la solución (junto con FM Shemyakin, 1947), y también llevó a cabo la idea de la posibilidad de la separación cromatográfica de una mezcla de sustancias basadas en la diferencia en la solubilidad de la solubilidad. (Cromatografía sedimentaria, 1948).
El escenario moderno en el desarrollo de la cromatografía de intercambio iónico comenzó en 1975 después de la labor de la ciudad de Smallla, T. Stevens y W. Bauman (EE. UU.), En los que propusieron un nuevo método analítico llamado cromatografía de iones (una opción para altamente eficiente Intercambio de la cromatografía de iónes con detección condacométrica).
La creación de la compañía "Perkin-Elmer" M. Golley (EE. UU.) De la variante capilar de cromatografía (1956), en la que se aplica el sorbente a las paredes internas del tubo capilar, lo que permite analizar el microcolismo de las mezclas multicomponentes.
A finales de los 60. Mayor interés en la cromatografía líquida. Hubo cromatografía líquida altamente eficiente (HPLC). Esto fue facilitado por la creación de detectores altamente sensibles, nuevos sorbentes de polímeros selectivos, equipos nuevos, que permitieron operar a altas presiones. Actualmente, HPLC ocupa una posición de liderazgo entre otros métodos de cromatografía e implementado en varias versiones.
2. Provisiones básicas
La cromatografía es un método de separación y determinación de sustancias basadas en la distribución de los componentes entre las dos fases: móvil y fijo. La fase fija (estacionaria) sirve una sustancia porosa sólida (a menudo llamada sorbente) o una película líquida aplicada a un sólido. La fase móvil es un líquido o gas que fluye a través de una fase fija, a veces bajo presión. Los componentes de la mezcla de la mezcla (núcleo) junto con el movimiento de fase móvil a lo largo de la fase estacionaria. Por lo general, se coloca en un tubo de vidrio o metal, llamado columna. Dependiendo de la fuerza de interacción con la superficie sorbente (debido a la adsorción o por cualquier otro mecanismo), los componentes se moverán a lo largo de la columna a diferentes velocidades. Algunos componentes permanecerán en la capa superior del sorbente, otros, en menor medida, interactuarán con el sorbente, estarán en la parte inferior de la columna, y algunos dejarán la columna junto con la fase móvil (tales componentes no se pagan, y Su tiempo de espera determina los altavoces de "tiempo muerto"). Por lo tanto, se produce la rápida separación de mezclas complejas de componentes. Se deben enfatizar los siguientes detalles de los métodos cromatográficos:
1. La separación es dinámica, y se repiten los actos de extracción-desorción de componentes compartidos repetidos. Esto causa una eficiencia significativamente mayor de la separación cromatográfica en comparación con los métodos estáticos de sorción y extracción.
2. Durante la separación, se utilizan varios tipos de interacción de los sorbatos y las fases estacionarios: de puramente físico a la hemosorción. Esto provoca la posibilidad de separación selectiva de un amplio círculo de sustancias.
3. En las sustancias separadas, puede aplicar varios campos adicionales (gravitacionales, eléctricos, magnéticos, etc.), que, cambiando las condiciones de separación, expandan las posibilidades de cromatografía.
4. La cromatografía es un método híbrido que combina la separación simultánea y la definición de varios componentes.
5. La cromatografía le permite resolver ambas tareas analíticas (separación, identificación, definición) y preparativas (limpieza, selección, concentración). La solución de estas tareas se puede combinar realizándolas en modo "en línea".
6. Numerosos métodos se clasifican por el estado agregado de las fases, el mecanismo de separación y la técnica de separación. Los métodos cromatográficos difieren en el método para llevar a cabo el proceso de separación al frente, crisol y eluyente.
3. Clasificación de los métodos de análisis cromatográfico.
Las formificaciones de los métodos cromatográficos se basan en los principios que tienen en cuenta las siguientes características diferentes del proceso de separación:
* Diferencias en el estado agregado de las fases del sistema cromatográfico utilizado;
* Diferencias en la naturaleza de las interacciones de sustancias separadas con fase fija;
* Diferencias experimentales en los métodos para el proceso de separación cromatográfica.
En las tablas 1? 3 muestra las variantes básicas de la clasificación de los métodos cromatográficos conocidos.
Dado que la naturaleza de las interacciones de los compuestos separados con fases de diversos sistemas cromatográficos puede variar mucho, casi no hay objetos, de la separación de los cuales no sería posible encontrar una fase fija adecuada (sólida o líquida) y en el solvente enrollado sistemas. El alcance de las variantes básicas de cromatografía dependiendo del peso molecular de los compuestos en estudio se da en la tabla. cuatro.
4. Cromatografía de adsorción. Cromatografía de capa fina
Una de las técnicas de cromatografía de adsorción más comunes es la cromatografía de capas delgadas (TLC): un tipo de cromatografía plana, a la que se utiliza el adsorbente como una capa delgada en la placa.
El principio y los conceptos básicos del método TLC. En una superficie plana limpia (placa de vidrio, metal, plásticos) de una forma u otra, se aplica una capa delgada del sorbente, que a menudo se fija en la superficie de la placa. Las dimensiones de la placa pueden ser diferentes (longitud y anchura, de 5 a 50 cm, aunque no es necesario). En la superficie de la placa, con cuidado, no dañar la capa de sorbente, esbozado (por ejemplo, un lápiz) de la línea de inicio (a una distancia de 2-3 cm desde el borde inferior de la placa) y la línea de la Acabado solvente.
Esquema de separación de componentes A y en el método TLC
En la línea de salida, se aplica la placa (por una microeléctrica, una muestra capilar), una pequeña cantidad de líquido que contiene una mezcla de sustancias separables, por ejemplo, dos sustancias A y B en un disolvente adecuado. Es posible evaporar el disolvente, después de lo cual la placa se sumerge en la cámara cromatográfica en la fase líquida de la PF, que es un disolvente especialmente seleccionado o una mezcla de disolventes para un caso determinado. Bajo la acción de las fuerzas capilares de PF se mueve espontáneamente a lo largo de la NF de la línea de partida a la línea del frente de solvente, cuidando con ellos los componentes A y en muestras que se mueven a diferentes velocidades. En este caso, la afinidad del componente A a la NF es menos afinidad por la misma fase del componente B, por lo que el componente A se está moviendo más rápido que el componente B. Después de alcanzar la fase móvil (solvente) de la línea de solvente, La cromatografía se interrumpe, la placa se retira de la cámara cromatográfica, se seca en el aire y determina la posición de las manchas de sustancias A y en la superficie de la placa. Los puntos (zonas) generalmente tienen una forma óvalo o redonda. En el caso en consideración, el componente de la mancha A se movió de la línea de inicio a la distancia l. UNA. , componente de punto en - por distancia l. EN, y el disolvente pasó a través de la distancia. L..
A veces, simultáneamente con la aplicación de muestras de sustancias separadas en la línea de inicio, se aplican pequeñas cantidades de la norma de la norma, así como las sustancias testigos (aquellas supuestamente contenidas en la muestra analizada).
Para caracterizar los componentes compartidos, la movilidad de RF (o el factor RF) se introduce en el sistema:
R. f.\u003d V. 1 / V. MI.\u003d (L. 1 / T) / (l / t) \u003d l 1 / L. ,
dónde V. 1 = l. 1 / t. y V. MI.= L./ t. - en consecuencia la velocidad de movimiento. i.- componente y solvente e; l. 1 yL. - pASADO PASADO i.- el componente y el disolvente, respectivamente, T es el tiempo requerido para mover el disolvente desde la línea de inicio a la línea frontal del solvente. Distancias l. 1 apriete desde la línea de salida hasta el centro del lugar del componente correspondiente.
Por lo general, el coeficiente de movilidad se encuentra en la redistribución. R. f. =0 - 1. El valor óptimo es 0.3-0.7, se seleccionan condiciones de cromatografía para que el valor R f sea diferente de cero y las unidades.
El coeficiente de movilidad es una característica importante del Sistema Sorbato Sorbente. Para condiciones de cromatografía reproducible y estrictamente constante. R. f. = const.
El coeficiente de movilidad de RF depende de una serie de factores: la naturaleza y la calidad del disolvente, su pureza; Naturaleza y calidad del sorbente (capa delgada), uniformidad de sus granos, grosor de la capa; la actividad del sorbente (contenido en su humedad); técnicas del experimento (muestras de masas, la longitud de la luna del solvente); Habilidad del experimentador, etc. La constancia de reproducir todos estos parámetros en la práctica es a veces difícil. Para nivelar el impacto de las condiciones del proceso, se introduce el factor de movilidad relativa. Rs..
Rs \u003d l / l arte\u003d R. f./ R. f ( arte ) ,
dónde R. f. = l./ L.; R. f. (S t)= l. arte/ L.; l. cm. - la distancia desde la línea de inicio hasta el centro del lugar estándar.
El coeficiente relativo de la movilidad RS es una característica más objetiva de la movilidad de la sustancia que el coeficiente de movilidad R f.
Como estándar, una sustancia de este tipo a menudo se elige para la cual en estas condiciones r f? 0.5. En la naturaleza química, el estándar se selecciona cerca de las sustancias separadas. Usando el estándar, el valor de RS generalmente se encuentra dentro de RS \u003d 0.1--10, los límites óptimos son aproximadamente 0.5--2.
Para una identificación más confiable de los componentes compartidos, use "testigos": sustancias de referencia, cuya presencia se asume en la muestra analizada. Si R F \u003d R F (SVID), en el que R F y R F (SVID), respectivamente, los coeficientes de la movilidad de este componente y un testigo, entonces es lo más probable que pueda asumir que la sustancia de prueba está presente en la mezcla cromatográfica.
Para caracterizar la separación de dos componentes a y en estas condiciones, se introduce el grado (criterio) de la separación R (A / B):
R (A / B) \u003d D l.(\u003d 2d l. ,
donde D. l. - la distancia entre los centros de puntos de los componentes A y B; A (a) y A (B), respectivamente, los diámetros de los puntos A y B en el cromatograma.
Cuanto mayor sea el valor R (A / B), más claro que las manchas de los componentes A y B están separadas en el cromatograma.
Para estimar la selectividad de la separación de dos sustancias A y B use el coeficiente de separación pero:
a \u003d.l. B. / l. UNA.
Si un a \u003d 1,que los componentes A y B no están divididos.
Para determinar el grado de separación R (A / B) de los componentes A y V.
4.1 Técnica experimental en cromatografía de capa fina:
pero) Muestra de aplicación. La muestra líquida analizada se aplica a la línea de inicio usando el capilar, micro-mierda, micropipetas, cuidadosamente tocar la capa absorbente (el diámetro de la mancha en la línea de salida es por lo general de uno a unos pocos milímetros). Si algunas muestras se aplican a la línea de salida, entonces la distancia entre las manchas de las muestras en la línea de salida no debe ser inferior a 2 cm. Si se utilizan las posibles soluciones, concentrados. Los puntos se secan en el aire, después de lo cual se lleva a cabo la cromatografía.
b) Desarrollo del cromatograma (cromatografía).El proceso se lleva a cabo en cámaras cromatográficas cerradas saturadas con pares de solventes utilizados como PF, por ejemplo, en un recipiente de vidrio, cubierto sobre una tapa.
Dependiendo de la dirección de movimiento, el PF se distingue. ascendiendo descendiendo y horizontal cromatografía.
En forma de cromatografía ascendente, solo se utilizan placas con una capa de sorbente fija. PF se vierte sobre la parte inferior de la cámara (como este último, se puede usar un vidrio químico de tamaño adecuado con una tapa de vidrio), la placa cromatográfica se coloca verticalmente u oblicuamente en la cámara de modo que la capa PF en la parte inferior de la cámara se humedeció la parte inferior de la placa (por debajo de la línea de salida por aproximadamente 1,5 - de 2 cm). El PF se mueve debido a la acción de las fuerzas capilares desde abajo hacia arriba (contra la gravedad) con relativa lenta.
En la variante descendente de cromatografía, también se aplican las placas con una capa fija. PF se alimenta de arriba y se mueve hacia abajo a lo largo de la capa de sorbent. El poder de la gravedad acelera el movimiento del PF. Esta realización se implementa al analizar mezclas que contienen componentes, moviéndose lentamente con PF.
En la realización de la cromatografía horizontal, la placa se coloca horizontalmente. Puedes usar placas rectangulares o redondas. Al aplicar placas redondas (variante circular de la cromatografía horizontal), la línea de salida se denota como un círculo de un radio adecuado (~ 1,5-2 cm), que se aplican muestras. En el centro de la placa redonda, el orificio se corta en el que se inserta la mecha para suministrar PF. Este último se mueve a lo largo de la capa sorbente del centro del círculo a su periferia. La cromatografía se realiza en una cámara cerrada, el desecador o en la olla de petri. Con una versión circular, puede analizar simultáneamente hasta varias docenas de muestras.
En los métodos TLC, se utilizan cromatografía unidimensional, bidimensional, múltiple (re), paso a paso.
En cromatografía de una sola vez, el análisis se realiza sin cambiar la dirección del movimiento del PF. Este método es el más común.
cromatografía bidimensional se utiliza generalmente para analizar mezclas complejas (proteínas, aminoácidos, etc.), la mezcla se lleva a cabo en primer lugar usando la primera PF 1. El cromatograma se obtiene manchas no sustancias individuales, y mezclas de varios componentes inseparables. Luego, a través de estas manchas, se realiza una nueva línea de inicio, la placa se convierte en 90 ° y se cromatografía nuevamente, pero ya con la segunda PF 2, esforzándose por finalmente dividir las manchas con mezclas en las manchas de los componentes individuales.
Si la placa es cuadrada, entonces la muestra se aplica a la diagonal de este cuadrado cerca de su esquina inferior. A veces se lleva a cabo cromatografía bidimensional con el mismo PF en una placa cuadrada.
El esquema que ilustra el principio de cromatografía bidimensional:
a - cromatograma obtenido de PF1;
b - cromatograma obtenido de PF2
En múltiples (re) cromatografía, el proceso se lleva a cabo varias veces secuencialmente desde el mismo PF (cada vez, después del siguiente secado) hasta la separación deseada de las manchas de los componentes de la mezcla (generalmente, no más de tres veces).
En el caso de la cromatografía en pasos, el proceso se lleva a cabo con la misma placa que usa secuencialmente cada vez que se alcanza una nueva PF, hasta que se alcanza una separación clara de las manchas.
en) Decodificación de cromatogramas. Si se pintan las manchas en el cromatograma, después de secar las placas, determine la distancia desde la línea de inicio hasta el centro de cada lugar y calcule los coeficientes de movilidad. Si la composición de la muestra analizada consiste en sustancias incoloras, dando sin pintar, es decir,. Visualmente no identificó lugares en el cromatograma, necesitas gastar detección estos puntos para los cuales cromatograma. show.
Los métodos de detección más comunes se describen a continuación.
Irradiación con la luz ultravioleta.Se utiliza para detectar compuestos fluorescentes (manchas son brillantes durante la irradiación de la UV placa de la luz) o sustancias petrolevascular, pero usando un sorbente con un indicador fluorescente (el sorbente está encendido, los puntos no se encienden). De este modo, detectado, por ejemplo, alcaloides, antibióticos, vitaminas y otras sustancias medicinales.
Tratamiento térmico.La placa secada después de la cromatografía se calienta suavemente (hasta ~ 200 ° C), evitando el oscurecimiento del sorbente en sí (por ejemplo, cuando la capa delgada del sorbente contiene almidón). Al mismo tiempo, las manchas generalmente se manifiestan en forma de zonas marrones (debido a la termólisis parcial de los componentes orgánicos).
Procesamiento químico.A menudo, los cromatogramas exhiben, procesándolos con reactivos que forman compuestos de colores con los componentes compartidos de las mezclas. Para estos fines, se usan varios reactivos: un par de yodo, amoníaco, bromo, dióxido de azufre, sulfuro de hidrógeno, soluciones especialmente preparadas que se tratan con placas. Aplique los reactivos tanto universales como selectivos (el concepto de "universal" es lo suficientemente condicional).
Universal ReactentAgOot Sirva, por ejemplo, ácido sulfúrico concentrado (cuando se calienta, hay un oscurecimiento de los compuestos orgánicos), una solución acuosa de permanganato de potasio (zonas se observan en forma de manchas marrones en un fondo de sorbente púrpura), una solución de Ácido de fósforo-molibdeno durante el calentamiento (las manchas azules aparecen sobre fondo amarillo), etc.
Como uso selectivo, por ejemplo, el reactivo de dragendorf; Reactivo de Zimmerman; solución acuosa de amonio de sulfato de cobre (10% de CUSO 4, 2% en amoníaco); Una mezcla de ninhidrina C 9 H 4 O 3 H2O con etanol y ácido acético.
El reactivo Dragandorf es una solución del nitrato de unión principal de Bondo 3, yoduro de potasio KJ y ácido acético en agua. Se utiliza para determinar las aminas, alcaloides, esteroides.
El reactivo de Zimmerman se prepara tratando la solución alcalina KOH 2% de la solución de etanol de dinitrobenceno, seguido del calentamiento de la mezcla a ~ 70-100 ° C. Aplicar para detectar esteroides.
Con la ayuda de Ningidrin, se detectan las manchas de aminas, aminoácidos, proteínas y otras conexiones.
Se utilizan algunas otras formas de detectar puntos. Por ejemplo, su radioactividad se mide si algunos de los componentes separados de radioactivos se introducen especialmente los aditivos de isótopos radiactivos de elementos que forman parte de los componentes separados de la mezcla.
Después de detectar puntos en el cromatograma, se identifican, es decir, Está determinado por el cual el compuesto corresponde a este o ese punto. Para este propósito, los puntos de referencia de los "testigos" se usan con mayor frecuencia. A veces, las manchas se identifican por la magnitud de los coeficientes de movilidad RF, comparándolos con los valores de R F conocido por estas condiciones. Sin embargo, tal identificación de R F es a menudo preliminar.
El color de los puntos fluorescentes también se usa con fines de identificación, ya que varios compuestos son fluorescentes por radiación de varias longitudes de onda (diferentes colores).
Con la detección química de manchas, los reactivos selectivos dan manchas pintadas con compuestos de cierta naturaleza, que también se utilizan con fines de identificación.
Con la ayuda del método TLC, no solo puede abrir, sino que también puede cuantificar el contenido de los componentes en las mezclas. Para hacer esto, se analizan los puntos sobre el cromatograma en sí mismos, o los componentes separados del cromatograma se eliminan de una forma u otra (extracción, elución con solventes adecuados).
Al analizar, las manchas implican la existencia de una cierta conexión entre el área de puntos y el contenido de esta sustancia (por ejemplo, la presencia de una dependencia proporcional o lineal), que se establece mediante el método de construcción de un gráfico de graduación, midiendo el Manchas de los "testigos" puntos con un contenido conocido del componente que se está analizando.
A veces, comparan la intensidad del color de las manchas, creyendo que la intensidad de las manchas de color es proporcional al número de este componente pintado. Para la intensidad de medición, se utilizan diferentes técnicas.
Al eliminar los componentes separados del cromatograma, se obtiene una solución que contiene este componente. Este último se determina por uno u otro método analítico.
El error relativo de la determinación cuantitativa de la sustancia por parte del TLC es del 5-10%.
TLC es un método farmacopea y se usa ampliamente para analizar y controlar la calidad de varios medicamentos.
5. Cromatografía de gases
En cromatografía de gases (GC), gas inerte (nitrógeno, helio, hidrógeno), llamado portador de gas, se usa como la fase móvil. La muestra se alimenta en la forma de un vapor, A sirve de fase fija o un sólido - un sorbente (cromatografía de adsorción de gas) o un (cromatografía gas-líquido) de alta ebullición líquido aplicado por una capa delgada sobre un soporte sólido. Considere la opción de cromatografía de gas-líquido (GLC). Kizelgur (Diatomitis) se utiliza como portador: se usa un tipo de gel de sílice hidratado, que a menudo se trata con reactivos que traducen los grupos Si-OH en el grupo SI-O-SI (CH3) 3, lo que aumenta la inerte de la Transportista con respecto a los solventes. Estos son, por ejemplo, los portadores del "cromosorb w" y "gasohromq". Además, se utilizan microsistas de vidrio, teflón y otros materiales.
5.1 GAZA- cromatografía de adsorción.
La peculiaridad del método de cromatografía de gas de la bomba (GA) es que como fase fija, se utilizan adsorbentes con una superficie específica elevada (10 a -1,000 m 2 g -1), y la distribución de sustancias entre las fases fijas y móviles es Determinado por el proceso de adsorción. Adsorción de moléculas de la fase gaseosa, es decir, Concentrado en la superficie de la separación de fases sólidas y gaseosas, se produce debido a las interacciones intermoleculares (dispersión, orientación, inducción) que tiene una naturaleza electrostática. Es posible, la formación de enlaces de hidrógeno, y la contribución de este tipo de interacción en los volúmenes retenidos se reduce significativamente con la temperatura creciente.
Para la práctica analítica, es importante que a una temperatura constante, la cantidad de sustancia adsorbida en la superficie con S era proporcional a la concentración de esta sustancia en la fase de gas con M:
C. s. = kc. mETRO. (1)
esos. para que la distribución haya ocurrido de acuerdo con la isoterma lineal de la adsorción (a - constante). En este caso, cada componente se mueve a lo largo de la columna con una velocidad constante, independientemente de su concentración. La separación de sustancias se debe a diferentes velocidades de su movimiento. Por lo tanto, la selección del adsorbente, el área y la naturaleza de la superficie de los cuales determinar la selectividad (separación) a una temperatura dada, es extremadamente importante en los huecos.
El calor de la adsorción disminuye con la creciente temperatura. DH / T.de qué detección depende y, en consecuencia t. R. . Esto se utiliza en la práctica del análisis. Si los compuestos se separan muy diferentes de la volatilidad a una temperatura constante, a continuación, sustancias de bajo punto de ebullición se eluyen rápidamente, alto punto de ebullición tiene un tiempo mayor, sus picos en el cromatograma serán más bajos y más amplia, el análisis lleva mucho tiempo. Si, en el proceso de cromatografía, aumente la temperatura de la columna con una velocidad constante (programación de temperatura), se colocarán uniformemente los picos cerca del ancho en el cromatograma.
Como adsorbentes para el GI, se utilizan principalmente bullicios activos, geles de sílice, vidrio poroso, óxido de aluminio. La inhomogeneidad de la superficie de los adsorbentes activos se debe a las principales desventajas de los métodos de la GAH y la imposibilidad de determinar las moléculas polares altamente adsorbidas. Sin embargo, en adsorbentes macroporosas geométricamente y químicamente homogéneos, es posible analizar mezclas de sustancias fuerte polares. En los últimos años, los adsorbentes recientemente producen adsorbentes con una superficie más o menos homogénea, como los polímeros porosos, los geles de sílice macroporosos (satlohrom, golpeado, aerosol), gafas porosas, zeolitas.
El método más ampliamente grande de cromatografía de bombas de gas se utiliza para analizar mezclas de gases y hidrocarburos de baja ebullición que no contienen grupos funcionales activos. Las isoterminas de adsorción de tales moléculas están cerca de lineal. Por ejemplo, para la separación de 2, N 2, CO, CH 4, CO 2 es utilizado con éxito por arcilla. La temperatura de la columna está programada para reducir el tiempo de análisis reduciendo los gases de ebullición de alto nivel. En los sintas moleculares: materiales cristalinos naturales o sintéticos altamente farmacéuticos, de los cuales los poros de los cuales tienen las mismas dimensiones (0,4--1.5 nm), se pueden dividir con isótopos de hidrógeno. Los sorbentes, llamados cazadores, se utilizan para separar los hidruros metálicos (GE, como, SN, SB). El método de GA en columnas con sorbentes poliméricas porosas o tamaños moleculares de carbono es la manera más rápida y conveniente para determinar agua en materiales inorgánicos y orgánicos, por ejemplo en disolventes.
5.2 GAZA- cromatografía líquida
En la práctica analítica, se usa más a menudo el método de cromatografía de gas-líquido (GLC). Esto se debe a la extrema diversidad de fases fijas líquidas, lo que facilita elegir una fase selectiva para este análisis, con una linealidad de las isotermas de distribución en un área de concentración más amplia, que le permite trabajar con muestras grandes y fácilmente obtener reproducible columnas.
El mecanismo de distribución de componentes entre el portador y una fase líquida fija se basa en disolverlos en la fase líquida. La selectividad depende de dos factores: elasticidad de vapor de la sustancia determinada y su coeficiente de actividad en la fase líquida. Según la ley de Raoul, al disolver la elasticidad de un vapor de una sustancia sobre una solución. pag. i. directamente proporcional a su coeficiente de actividad g fracción molar NORTE. i. En solución y presión del vapor de la sustancia pura. R ° i. A esta temperatura:
p i \u003d n i p ° i (2)
Dado que la concentración del componente I-TH en la fase de vapor de equilibrio está determinada por su presión parcial, puede aceptar que
P i ~ c m, y n i ~ c s entonces
y coeficiente de selectividad:
Por lo tanto, cuanto menor sea el punto de ebullición de la sustancia (el mayor p 0 i), más débil se mantiene en la columna cromatográfica.
Si el punto de ebullición de sustancias es el mismo, entonces las diferencias en la interacción con una fase líquida fija se utilizan para separarlos: cuanto más fuerte sea la interacción, menor será el coeficiente de actividad y más retención.
Fases líquidas fijas . Para garantizar la selectividad de la columna, es importante seleccionar correctamente la fase líquida fija. Esta fase debe ser un buen disolvente para los componentes de la mezcla (si la solubilidad es pequeña, los componentes se extienden de la columna muy rápidamente), no volátil (para no evaporarse a la temperatura de funcionamiento de la columna), químicamente inerte, debe tiene una ligera viscosidad (de lo contrario el proceso de difusión se ralentiza) y cuando se aplica al soporte para formar una película uniforme está firmemente conectado con él. La capacidad de separación de la fase fija para los componentes de esta muestra debe ser máximo.
Las fases líquidas de tres tipos se distinguen: no polar (hidrocarburos saturados, etc.), moderadamente polar (ésteres, nitrilos, etc.) y polar (poliglicols, hidroxilamia, etc.).
Conocer las propiedades de una fase líquida fija y la naturaleza de sustancias separables, como una clase, estructura, es posible elegir rápidamente una fase líquida selectiva para separar esta mezcla. Debe tenerse en cuenta que el tiempo de mantenimiento de los componentes será aceptable para el análisis, si la polaridad de la fase estacionaria y la sustancia de la muestra analizada está cerca. Para sustancias disueltas con una polaridad estrecha, la orden de elución generalmente se correlaciona con las temperaturas de ebullición, y si la diferencia de temperatura es lo suficientemente grande, es posible completar la separación. Para la separación de sustancias de ebullición cercana de diferente polaridad, la fase estacionaria se usa, manteniendo selectivamente uno o más componentes debido a la interacción Dipole - Dipole. Con un aumento en la polaridad de la fase líquida, aumenta el tiempo de retención de compuestos polares.
Para aplicar uniformemente la fase líquida al portador sólido, se mezcla con un disolvente volátil, como el éter. Se agrega un portador sólido a esta solución. La mezcla se calienta, el disolvente se evapora, la fase líquida permanece en el portador. Un portador seco con una fase líquida fija aplicada de esta manera se llena de una columna, tratando de evitar la formación de vacíos. Para un embalaje uniforme a través de la columna, la corriente de gas se pasa y se golpea simultáneamente la columna para los sellos de embalaje. Luego, antes de sujetar al detector, la columna se calienta a una temperatura de 50 ° C sobre la que se supone que se debe utilizar. En este caso, puede haber pérdidas de la fase líquida, pero la columna se incluye en el modo de operación estable.
Medios de fases líquidos fijos. Los medios sólidos para dispersión de una fase líquida fija en forma de una película delgada homogénea deben ser duraderos mecánicamente con un área de superficie específica moderada (20 m 2 / g), tamaño de partícula pequeño e igual, y también ser suficientes para la adsorción en la superficie. del sólido y gaseoso etapas Era mínimo. La adsorción más baja se observa en los transportistas de cromosorba silanizada, gránulos de vidrio y fluoropac (polímero de fluorocarbono). Además, los portadores sólidos no deben responder a un aumento de la temperatura y deben hacerse fácilmente con una fase líquida. En la cromatografía de gases de los quelatos como portador sólido, los portadores de diatomitis blanca midaneed se utilizan con mayor frecuencia: sílice diatomítica, o kizelgur. La ditomitis es un dióxido de silicio y micronomórfico que contiene agua que contiene agua. Tales transportistas incluyen cromosorb W, gasohrom Q, Chromaton N, et al. Además, las bolas de vidrio y el uso de teflón.
Fases relacionadas químicamente. A menudo use portadores modificados, asociados covalentemente con una fase líquida. En este caso, la fase líquida estacionaria se mantiene firmemente en la superficie, incluso en las temperaturas de la columna más altas. Por ejemplo, el portador diatomítico se trata con un clorosilano con un sustituyente de cadena larga, que tiene una cierta polaridad. La fase fija acoplada químicamente es más eficiente.
6. Cromatografía de distribución. Cromatografía de papel (cromatografía en papel).
La cromatografía de distribución se basa en el uso de diferencias en la solubilidad de la sustancia distribuida en dos fases líquidas de contacto de contacto. Ambas fases - PF y NF son fases líquidas. Al mover el PF líquido a lo largo del líquido NF, las sustancias cromatográficas se redistribuyen continuamente entre ambas fases líquidas.
La cromatografía de distribución se refiere. chromatu de papelgráfico (o cromatografía en papel) en sus opciones habituales. En este método, en lugar de placas con una capa delgada de sorbent que se usa en TLC, según el cual se usa un papel cromatográfico especial, según el cual, impregnándolo, el PF líquido se mueve durante la cromatografía desde la línea de inicio a la línea de meta disolvente.
Distinguir fase normal y fiel cromatografía en papel.
En la realización fase normal la cromatografía en papel del líquido NF es agua, sorbed en forma de una capa delgada en las fibras y en los poros. hidrófilo papel (hasta un 25% en peso). Este agua limitada en su estructura y estado físico es muy diferente de la agua líquida convencional. En ella, los componentes de las mezclas compartidas se disuelven.
El papel de PF que se mueve a través del papel es jugado por otra fase líquida, por ejemplo, líquido orgánico con la adición de ácidos y agua. El PF orgánico líquido antes de la cromatografía está saturada con agua de modo que la PF no disuelva el golpe de agua en las fibras de papel cromatográfico hidrófilo.
El documento cromatográfico es fabricado por la industria. Debe cumplir con una serie de requisitos: prepararse a partir de variedades de algodón fibroso de alta calidad, para ser homogéneas de densidad y espesor, en la dirección de orientación de las fibras, químicamente limpio e inerte en relación con el NF y los componentes compartidos.
En una realización de fase normal, las mezclas líquidas compuestas de varios disolventes se usan con mayor frecuencia como PF. Un ejemplo clásico de tal PF es una mezcla de ácido acético, n-butanol y agua en relación volumen 1: 4: 5. Se utilizan disolventes tales como acetato de etilo, cloroformo, benceno, etc..
En la realización fielfulfazova cromatografía de papel El líquido NF es un disolvente orgánico, mientras que las soluciones de agua, acuosas o alcohólicas y mezclas de alcohol con alcoholes, actúan como un PF líquido. El proceso se lleva a cabo utilizando hidrofóbico papel cromatográfico. Se obtiene tratando (impregnando) con naftaleno, aceites de silicona, parafina, etc. Los disolventes orgánicos no polares y bajos polares están sorbemos en fibras de papel hidrófobas y penetran en sus poros, formando una capa delgada de líquido NF. El agua no se mantiene en dicho papel, no lo moja.
La técnica de la cromatografía en papel en términos generales es la misma que en el método TLC. Por lo general, se aplica un kashpo de una solución analizada que contiene una mezcla de sustancias compartidas al carril de papel cromatográfico en la línea de inicio del inicio. Después de la evaporación del disolvente, el papel debajo de la línea de inicio se sumerge en PF, colocando papel verticalmente (colgándolo). Cierre la cámara con una tapa y cromatografía hasta que el PF no llegue a la línea del frente solvente designado en papel. Después de eso, el proceso se interrumpe, el papel se seca en el aire y la detección de puntos e identificando los componentes de la mezcla.
La cromatografía en papel es similar al método TLC utilizado tanto en análisis cualitativo como cuantitativo.
Para cuantificar el contenido de uno u otro componente de la mezcla, se utilizan varios métodos:
1) proceder de la presencia de una cierta dependencia (proporcional, lineal) entre la cantidad de sustancia en el área de la mancha y los puntos (a menudo el programa de calibración es pre-construido);
2) Pese la mancha de corte con la sustancia y el mismo papel puro en el área, y luego en términos de la diferencia que encuentran una masa de la sustancia determinada;
3) Tenga en cuenta la relación entre la intensidad del color de la mancha y el contenido en él, lo que le da el color de la mancha.
En algunos casos, las sustancias contenidas en las manchas se extraen con cualquier solvente y luego analizar el extracto.
La cromatografía en papel es un método de farmacopea, que se utiliza para separar las mezclas que contienen sustancias tanto inorgánicas como orgánicas. El método está disponible, fácil de cumplir, pero en general es inferior a un método TLC más moderno, en el que se aplica una capa delgada del sorbente.
7. Cromatografía sedimentaria
El método de cromatografía de sedimentos se utiliza principalmente para la separación e identificación de iones inorgánicos que conforman las mezclas.
La esencia del método. La cromatografía de sedimentos se basa en el uso de reacciones químicas de precipitación de componentes compartidos de una mezcla con un reactivo-precipiente, que forma parte de la NF. La separación se lleva a cabo debido a la solubilidad desigual de los compuestos formados que se transfieren a la fase móvil a diferentes velocidades: sustancias menos solubles se transfieren a la PF más lento que soluble.
Puede ilustrar el uso del método en el ejemplo de la separación de iones haluro: cloruro de CL-ion,-ion-ion bromuro de iones y de iones de yoduro-ion-ion-ion, contenidas simultáneamente en el analizado solución acuosa. Para hacer esto, use una columna cromatográfica (que representa un tubo de vidrio con una grúa en la parte inferior) llena con un sorbente. Este último consiste en su aceite de aluminio, óxido de aluminio al 2 O 3 o SIO 2 de silicio, impregnado con una solución de nitrato de plata de AGNO 3 (el contenido del nitrato de plata es aproximadamente del 10% en peso de la masa del sorbente portador).
Una solución acuosa que contiene una mezcla de aniones compartidos se pasa a través de la columna cromatográfica. Estos aniones interactúan con cationes de plata AG +, formando preciputados de haluro de plata tan solubles:
AG + + I -\u003e AGIV (Amarillo)
AG + + BR -\u003e AGBRV (crema)
AG + + CL -\u003e AGCLV (blanco)
La solubilidad de los haluros de plata en el agua aumenta en la secuencia:
AGL (K ° \u003d 8.3 * 10 -17)< АgВг (К° = 5,3*10 -13) < AgCl (K°= 1,78*10 -10),
donde entre paréntesis son los valores de los productos de solubilidad a temperatura ambiente. Por lo tanto, al principio, se formará el precipitado amarillo del yoduro de plata, ya que el menos soluble en el cromatograma se observará una zona amarilla (arriba). Luego se forma el eje del bromuro de plata de plata (zona intermedia). Finalmente, se forma un precipitado blanco de cloruro de plata: la zona blanca inferior es oscura debido a la descomposición fotoquímica del cloruro de plata con la liberación de plata metálica fina.
Como resultado, se obtiene un cromatograma sedimentario primario.
Para obtener una separación más clara de las zonas, después de obtener el cromatograma primario, se pasa un disolvente limpio a través de la columna para obtener un cromatograma sedimentario secundario con una separación clara de zonas de precipitación.
En el ejemplo descrito, el precipitador fue parte de la NF, y se pasó una solución que contenía una mezcla de iones compartidos a través de la columna. Es posible, por el contrario, pasar la solución del precipitador a través de la columna en el NF que son iones cromatográficos. Al mismo tiempo, sin embargo, se forman zonas mixtas.
El esquema de la separación de CL, BR y I-IONES en la columna cromatográfica mediante el método de cromatografía sedimentaria.
7.1 Clasificación de métodos de cromatografía sedimentaria sobre la técnica del experimento.
Generalmente distinguido columna cromatografía sedimentaria realizada en columnas cromatográficas y avión Cromatografía de sedimentos implementada en papel o en una capa delgada de sorbente.
Como sorbentes en la cromatografía sedimentaria, se utilizan mezclas de medios inertes con un inspirador; sorbentes que sostienen los precipitadores en forma de iones (resinas de intercambio ión) o en forma de moléculas (carbón activado); Papel impregnado con una solución precipitante.
Los transportistas suelen elegir gel de sílice, almidón, óxidos de aluminio, calcio, sulfato de bario, resinas de intercambio iónico, etc. El portador se usa en estado dispersado fino con dimensiones de aproximadamente 0,02-0.10 mm.
Como precipitantes, se utilizan tales reactivos que forman precipitados de bajo-soluble con iones cromatográficos, por ejemplo, yoduro de sodio NAI, sulfuro de sodio Na 2 s, sulfato de plata AG 2 SO 4, ferrocianuro de potasio k 4, oxicinolina, piridina, etc.
Por lo general, cuando se utiliza el método de cromatografía de sedimentos de columna después de pasar a través de la columna de un disolvente puro, se obtienen zonas claramente separadas, cada una de las cuales contiene solo un componente (en el caso de la solubilidad de la precipitación, diferir al menos tres veces). El método se caracteriza por una buena reproducibilidad de los resultados.
En el caso de la formación de áreas incolentes de precipitación, el cromatograma se muestra o pasa a través de un desarrollador de columnas, que proporciona con precipita los productos de reacción pintados, o introduciendo inmediatamente un desarrollador en la PF o en la NF.
7.2 cromatografía de sedimentos sobre papel.
¿Considera la esencia de este método en el ejemplo del análisis de la solución acuosa que contiene una mezcla de cationes de cobre CU 2+? Iron Fe 3+ y aluminio Al 3+.
En el centro de la hoja de papel impregnada con una solución precipitante, Ferrocianuro de potasio K 4, el capilar se aplica con una solución acuosa analizada. CU 2+ y iones de hierro Fe 2+ Interactuar con iones de ferrocianuro con la formación de precipitación mal soluble:
2CU 2+ + 4-\u003e Cu 2 (Brown)
4FE 3+ + 3 4-\u003e FE4 (AZUL)
Dado que el ferrocianuro de cobre (II) es menos soluble que el ferrocianuro de hierro (III), entonces se distingue el precipitado del ferrocianuro de cobre (II), formando una zona de color marrón central. Luego se forma el precipitado azul del hierro ferrocianuro (III), que da la zona azul. Los iones de aluminio se trasladan a la periferia, dando una zona incolora, ya que no forman un ferrocianuro de aluminio pintado.
El esquema de división CU2 +, FE3 + y AL3 + por el método de cromatografía sedimentaria.
De esta manera, se obtiene el cromatograma primario, donde las zonas de precipitación se superponen parcialmente.
Luego se obtiene el cromatograma secundario. Para ello, un disolvente adecuado (en el caso en consideración es una solución acuosa de amoníaco) se aplica por el capilar al centro del cromatograma primario. El disolvente se mueve espontáneamente desde el centro del papel a la periferia, se llevó a cabo con sí misma y precipita, que se mueven a diferentes velocidades: la zona de un sedimento más soluble de hierro ferrocianuro se mueve una zona más rápida de un sedimento menos soluble del ferrocianuro de cobre. En esta etapa, debido a la diferencia en las velocidades de las zonas de desplazamiento, se produce su separación más clara.
Para abrir los iones de aluminio, formando una zona periférica incolora, una exhibición de cromatograma secundario: spray (de una solución de aerosol) de Alizhar: un reactivo orgánico que se forma con iones de aluminio productos de reacción rosa. Obtener un anillo de rosa externo.
8. Cromatografía de intercambio de iones
En la cromatografía de intercambio iónico, la separación de los componentes de la mezcla se logra mediante la interacción reversible de las sustancias ionizantes con los grupos sorbentes de iones. La preservación de la referida electrónica del sorbente está asegurada por la presencia de contraiones capaces de intercambio de iones ubicado en la proximidad a la superficie. El ion de la muestra introducida, interactuando con la carga fija del sorbente, intercambia con el contraión. Las sustancias que tienen diferentes afinidad por una carga fija se dividen en aniónicos o en catión. Los anulados tienen grupos cargados positivamente en la superficie y la sorbita de la fase móvil de aniones. Los cationarios respectivamente contienen grupos con una carga negativa, interactuando con los cationes.
Como fase móvil, se utilizan soluciones acuosas de sales ácidas, bases y disolventes del tipo de amoníaco líquido, es decir, Sistemas de disolventes que tienen un alto significado de constante dieléctrico y una gran tendencia a ionizar compuestos. Normalmente funciona con soluciones de búfer, lo que permite ajustar el valor de pH.
Cuando la separación cromatográfica de los iones de la sustancia analizada compite con los iones contenidos en el eluyente, buscando interactuar con los grupos de sorbedores cargados opuestos. Se deduce que la cromatografía de intercambio iónico se puede usar para separar los compuestos que puedan ionizarse de cualquier manera. Es posible analizar incluso las moléculas de azúcares neutros en forma de sus complejos con un ion borato.
La cromatografía de intercambio iónico es indispensable en la separación de sustancias de jugo de ustedes que no pueden ser analizadas por el GLC sin la traducción a los derivados. Tales compuestos incluyen aminoácidos, péptidos, azúcar.
La cromatografía de intercambio de iones se usa ampliamente en medicina, biología, bioquímica, para el control ambiental, al analizar el contenido de los medicamentos y sus metabolitos en la sangre y la orina, se erradica en materias primas de alimentos, así como para la separación de compuestos inorgánicos, incluyendo Radioisótopos, lantanoides, actinoides, etc.. El análisis de los biopolímeros (proteínas, ácidos nucleicos, etc.), que generalmente gastan horas o días, con la ayuda de la cromatografía de intercambio iónico se llevan a cabo en 20-40 minutos con una mejor separación. El uso de la cromatografía de intercambio iónico en biología hizo posible observar las muestras directamente en biostructuras, reduciendo la posibilidad de reagrupación o isomerización, lo que puede llevar a una interpretación inadecuada del resultado final. Es interesante usar este método para controlar los cambios que se producen con los fluidos biológicos. El uso de intercambios aniónicos débiles porosos sobre una base de gel de sílice hizo posible dividir los péptidos. El mecanismo del intercambio de iones se puede representar como las siguientes ecuaciones:
para el intercambio de aniones x - + r + y - - y - + r + x -
para intercambio catiónico x + + r - y + - y + + r - x +
En el primer caso, el ion de la muestra X está compitiendo con el ión de la Fase Movible y, para el intercambiador de iones de Ion Centers, y en la segunda a la competencia con los iones de la Fase Móvil Y + para los centros de iones son son Los cationes de la muestra X +.
Naturalmente, los iones de muestra que están interactuando débilmente con el intercambiador de iones, con esta competencia se mantendrá débilmente en la columna y se eliminarán primero de ella y, por el contrario, los iones retenidos más fuertemente eluirán de la columna. Por lo general, las interacciones secundarias de la naturaleza no iónica están surgiendo debido a la adsorción o enlaces de hidrógeno de la muestra con la parte no iónica de la matriz o debido a la solubilidad limitada de la muestra en la fase móvil.
La separación de sustancias específicas depende principalmente de la elección del sorbente más adecuado y la fase móvil. Como fase fija en la cromatografía de intercambio de iones, se utilizan resinas de intercambio iónico y geles de sílice con grupos iónicos injertados.
Resinas de intercambio de iones de poliestireno para el grano de HPLC de 10 μm y menos poseen selectividad y estabilidad, pero la estructura de malla de ellas, caracterizada por la distancia entre los nodos de malla de 1,5 nm, que es significativamente menor que el tamaño de los poros utilizados para el gel de sílice La cromatografía de adsorción (10 nm), disminuye la transferencia de masa y, por lo tanto, reduce significativamente la eficiencia. Las resinas de intercambio de iones utilizadas en HPLC son principalmente copolímeros de estireno y divinil benceno. Normalmente agrega el 8-12% de este último. Cuanto mayor sea el contenido de di-vinilbenceno, mayor será la rigidez y la resistencia del polímero, por encima de la capacidad y, como regla, selectividad y la hinchazón más pequeña.
Documentos similares
Las características generales del proceso de cromatografía. Bases físico-química de cromatografía de capa fina, clasificación de métodos de análisis. Variantes de cromatografía por estados de fase. Control de calidad de los productos alimenticios mediante método TLC, equipo.
trabajo del curso, añadido 12/27/2009
Fenómenos ocurriendo durante la cromatografía. Dos enfoques para explicar son la teoría de las placas teóricas y la teoría cinética. Gas, líquido, cromatografía de papel. Método de intercambio iónico. Casos de aplicación de la cromatografía de intercambio iónico. Gelocromatografía.
resumen, añadido 01/24/2009
El concepto y la estructura de los sorbentes de polímeros, la historia de su creación y desarrollo, valor en el proceso de cromatografía de distribución. Tipos de sorbentes poliméricos, las posibilidades de su uso en cromatografía exclusiva. Características del uso de geles duros.
resumen, añadido 07.01.2010
La emergencia y el desarrollo de la cromatografía. Clasificación de los métodos cromatográficos. Cromatografía en una fase fija sólida: gas, líquido (adsorción líquida). Cromatografía en la fase fija líquida: cromatografía de gas-líquido y gel.
resumen, añadido 01.05.2009
La esencia del método de cromatografía, la historia de su desarrollo y tipos. Ámbito de cromatografía, dispositivos o instalaciones para la separación cromatográfica y análisis de mezclas de sustancias. El esquema del cromatógrafo de gas, sus principales sistemas y el principio de operación.
resumen, añadido 09/25/2010
Conceptos básicos del método de cromatografía transmitida. La cromatografía de gases es un método universal de análisis de alta calidad y cuantitativa de mezclas complejas y un método para producir componentes individuales en su forma pura. El uso de cromatografía de gases.
trabajo del curso, añadido 01/09/2010
La esencia y el contenido de la cromatografía en el par de iones, su uso en cromatografía líquida y su extracción para extraer medicamentos y sus metabolitos de fluidos biológicos a la fase orgánica. Variantes de cromatografía de iones, características distintivas.
resumen, añadido 07.01.2010
La cromatografía de gases es uno de los métodos de investigación fisicoquímicos más prometedores, que se desarrolla rápidamente. Clasificación de los métodos cromatográficos. Varios signos característicos del proceso. La esencia de los métodos de cromatografía.
resumen, añadido 01/25/2010
La esencia de la cromatografía líquida altamente eficiente (HPLC) como método para analizar y separar las impurezas complejas. Sorbentes, coordinación y quelatos saturados; Los patrones de la influencia de la estructura del ligando sobre el comportamiento de los quelatos en las condiciones de cromatografía infectada.
resumen, añadido 11/10/2011
El concepto y las principales etapas del flujo de cromatografía de exclusión, su característica de principios y alcance de la aplicación, variedades y sus características distintivas. Características de los equipos utilizados en el proceso de cromatografía exclusiva.
Muchos descubrimientos del siglo pasado están obligados al color del científico ruso Mikhail y su método de análisis cromatográfico. ¡Una gran cantidad de investigadores destacados deben con él con sus éxitos, y muchos y el Premio Nobel!
"... Sin el trabajo de Michael, no tendremos nada que ver con todos los" pigmentos ", no habría nada que hacer ..." - Aquí está la opinión de un famoso científico inglés.
Mikhail Semenovich Color (1872-1919) - El Hijo de Italiano y el Intelectual Ruso. Nació en Italia en la ciudad de Asti, no lejos de Turín. En 1891, Mikhail se graduó del gimnasio de Ginebra y entró en la Facultad de Física y Matemáticas de la Universidad de Ginebra. Representar la disertación "Estudio de la fisiología de la célula. Los materiales para el conocimiento del movimiento del protoplasma, las membranas plasmáticas y los cloroplastos" Color en octubre de 1896 recibieron un médico del médico de las ciencias naturales. En diciembre del mismo año, viene a San Petersburgo.
Mikhail no sabía que la beca de la Universidad de Ginebra no se reconoce en Rusia. Por lo tanto, tenía que trabajar en la famosa Botany Andrei Sergeyevich Famincin, quien también estudió clorofila, se puede decir sobre los derechos de los ave. En San Petersburgo, el color se familiarizó con otros fisiólogos de botánicos y plantas excepcionales: I.P. Borodin, M.S. Voronin, a.n. Beketovo. Fue una brillante sociedad de ricos originales en ideas de pensadores y experimentadores hábiles. El color continuó su investigación de cloroplastos, preparándose al mismo tiempo para los exámenes de los nuevos maestros y para defender la tesis. Pasó el examen en 1899, y defendió la tesis de su maestría en la Universidad de Kazan el 23 de septiembre de 1901.
Desde noviembre de 1901, el color ha estado trabajando como una oficina asistente del departamento de anatomía y fisiología vegetal en la Universidad de Varsovia. En el XI Congreso de naturalistas y médicos, Mikhail Semenovich hizo el informe "Métodos y objetivos de la clorofila de investigación fisiológica", en la que se informó por primera vez sobre el método de cromatografía de adsorción.
Mikhail Semenovich ha resuelto el problema de separar pigmentos de hojas verdes, y están muy cerca por las propiedades. Además, hay otros pigmentos, muy brillantes, carotenoides en las hojas. Es gracias a los carotenoides y en el otoño amarillo, naranja, aparecen hojas carmesí. Sin embargo, mientras las clorofilas no se destruyen, era casi imposible separarlas de los carotenoides.
Cómo las notas yu.g. Chirkov, "aparentemente, la apertura del color era una reacción a los métodos existentes de métodos groseros y asesinos de su separación. Aquí hay una de las técnicas.
Primero, se extraía el extracto de alcohol de clorofila, luego sus tres horas estaban hirviendo a Guil con la adición de alcalinos fuertes (potasio cáustico). Como resultado, la clorofila se descompone en partes compuestas: pigmentos verdes y amarillos.
Pero en el proceso de fabricación de esta poción (manipulaciones casi alquímicas), la clorofila natural podría colapsar. Y luego el investigador habría tratado con piezas de pigmentos, e incluso con los productos de su transformación química ".
Sobre cómo ocurrió el gran descubrimiento, escribe S.E. Shnol: "Tomó el tubo de vidrio, lo llenó con un polvo de tiza y vierte un poco de extracto de alcohol del extracto de la hoja en la capa superior, y la capa superior de la columna de tiza era del mismo color. Y luego la MS comenzó a verter. En la parte superior en tubo con alcohol puro de tiza. Caída por gota. Otra porción del disolvente se eluyó con pigmentos de los granos de grano, que se movió hacia el tubo. Allí, las tumbas de gramos frescas se adsorbieron los pigmentos y, a su vez, les dieron nuevas porciones de El disolvente. En virtud de varias resistencia a la adsorción diferente (facilidad de la elución) se perdió con un disolvente móvil, diferentes pigmentos se movieron a lo largo de la columna de tiza a diferentes velocidades y formaron una rayas pintadas homogéneas de sustancias puras en la columna de tiza. Era hermosa Franja verde brillante, la franja de amarillo amarillo: estos son dos tipos de clorofilas y barotinoides de color amarillo brillante. M.s. llamó a esta imagen cromatograma ".
"El color mostró, - escribe a Chirkov: que cuando los pigmentos vegetales disueltos con oveja a través de una capa de sorbente poroso incoloro, los pigmentos individuales se ubican en forma de zonas pintadas: cada pigmento tiene su propio color o al menos una sombra. Polvo sorbente ( Puede ser de tiza, azúcar en polvo ...) adsorb (absorbe superficialmente: adsorbe latino significa "tragar") Diferentes pigmentos con poder desigual: algunos pueden "deslizarse" con una corriente de solución adicional, otros se detendrán más cerca. Así, la capa -El color pintado de color coloreado color llamado cromatograma, y \u200b\u200bcromatografía de métodos ".
Por lo tanto, la tarea aparentemente intratable se resolvió. El método era ingenioso simple. No es de todo similar a voluminoso, exigiendo una gran cantidad de procedimientos complejos de reactivos aplicados anteriormente.
Tal vez esta simplicidad causó el hecho de que la mayoría de los contemporáneos o no percibían este increíble descubrimiento, o, que aún está triste, se rebeló contra su autor.
Pero el tiempo se pone en su lugar. Color inventado cromatografía para estudios de clorofila. Primero asignó una sustancia llamada clorofila alfa y clorofila beta. Resultó ser adecuado para la investigación, no solo los pigmentos, sino también de mezclas incoloras, sin pintar, proteínas, carbohidratos. Durante los años sesenta de la cromatografía del siglo XX, se dedicaron varios miles de estudios. La cromatografía se ha convertido en un método universal.
"... El principio de la separación cromatográfica de sustancias, abierta por M. Color, subyace en el conjunto de varios métodos de análisis cromatográfico. Sin su uso, la mayoría de los logros en la ciencia y la técnica del siglo XX serían imposibles. .
La base de todo esto es una idea común. Ella es sencilla Esta es esencialmente la idea de la progresión geométrica. Deja que haya dos sustancias muy cerca en todas sus propiedades. Ni la deposición ni la extracción ni la adsorción se dividen en una extensión notable. Deje que una sustancia se adsorbe en la superficie, por ejemplo, carbonato de calcio (es decir, menos del 1 por ciento).
En otras palabras, su contenido en el adsorbente será de 0.99 del contenido de la otra. Tratamos al adsorbente por cualquier disolvente para que la desorción (desconexión) y la elución (enjuague) de ambas sustancias y ambas se muevan del adsorbente al solvente, y transmitimos esta solución resultante a una porción fresca del adsorbente. Luego, la proporción de la primera sustancia en la superficie del adsorbente será nuevamente de 0.99 del contenido del segundo, es decir, la parte está adsorbida, igual a 0.99 x 0.99 \u003d 0.98 de la cantidad inicial. Una vez más, llevaremos a cabo la elución y otra vez la adsorción, ahora la proporción de la primera sustancia será de 0.98 x 0.99 \u003d 0.97 del contenido del segundo. Para que el contenido de la primera sustancia sea la siguiente parte del adsorbente, solo el 1 por ciento del contenido del segundo, será necesario repetir el ciclo de la elución de absorción de aproximadamente 200 veces ...
La idea de la conversación múltiple para la separación de sustancias se puede modificar en una redistribución múltiple de la mezcla de sustancias en el sistema de disolventes no secos. Esta es la base de la cromatografía de distribución. La misma idea subyace a los métodos actuales de electroforesis cuando la mezcla de sustancias se mueve a diferentes velocidades de varios adsorbentes en el campo eléctrico.
1. INTRODUCCIÓN.
2. La aparición y desarrollo de la cromatografía.
3. Clasificación de los métodos cromatográficos.
4. Cromatografía en una fase fija sólida:
a) cromatografía de gas (adsorción de gas);
b) cromatografía líquida (adsorción líquida).
5. Cromatografía en la fase fija líquida:
a) cromatografía de gas-líquido;
b) cromatografía en gel.
6. Conclusión.
Como los rayos del espectro, los diversos componentes de la mezcla de pigmentos se distribuyen naturalmente en la columna de dióxido de carbono, lo que permite su determinación cualitativa y cuantitativa. El medicamento obtenido de esta manera llamo al cromatograma y el método propuesto: cromatográfico.
M. Color, 1906.
Introducción
Con la necesidad de dividir y analizar la mezcla de sustancias, es necesario enfrentar no solo el químico, sino también a muchos otros especialistas.
En un poderoso arsenal de métodos químicos y fisicoquímicos de separación, análisis, el estudio de la estructura y las propiedades de los compuestos químicos individuales y sus mezclas complejas, uno de los lugares principales ocupa cromatografía.
La cromatografía es un método físico-químico de separación y análisis de mezclas de gases, vapores, líquidos o solutos y la determinación de las propiedades fisicoquímicas de las sustancias individuales basadas en la distribución de los componentes compartidos de las mezclas entre las dos fases: movibles y fijos. Las sustancias que conforman la fase fija se llaman sorbentes. La fase fija puede ser sólida y líquida. La fase móvil es un flujo de líquido o gas, filtrado a través de la capa sorbente. La fase móvil realiza las funciones del disolvente y el portador de la mezcla analizada de sustancias traducidas al estado gaseoso o líquido.
Hay dos tipos de sorción: adsorción: absorción de sólidos y absorción: disolución de gases y líquidos en disolventes líquidos.
2. Ha surgidocromatografía y desarrollo y desarrollo.
La aparición de cromatografía como método científico se asocia con el nombre del destacado científico ruso Mikhail Semenovich Colors (1872 - 1919), que en 1903 abrió cromatografía durante el estudio del mecanismo para la transformación de la energía solar en pigmentos de plantas. Este año debe considerarse la fecha de creación del método cromatográfico.
SRA. El color pasó la solución de las sustancias analizadas y la fase móvil a través del pilar adsorbente ubicado en un tubo de vidrio. En este sentido, su método recibió el nombre de la cromatografía en columna. En 1938 n.a. Izmailov y M.S. Schreiber se ofreció a modificar el método de color y llevar a cabo la separación de la mezcla de sustancias en la placa cubierta con una capa delgada del adsorbente. Por lo tanto, apareció cromatografía de capa fina, lo que hace posible analizar el microcolismo de la sustancia.
En 1947. tb GAPON, E.N. GAPON y F.M. Shemyakin Por primera vez, realizó una separación cromatográfica de una mezcla de iones en solución, explicando su presencia de una reacción de intercambio entre los iones y los iones sorbentes contenidos en la solución. Por lo tanto, se abrió otra dirección de cromatografía, cromatografía de intercambio de iones. Actualmente, la cromatografía de intercambio iónico es una de las direcciones más importantes del método cromatográfico.
E.N. y G. B. Gapon en 1948 implementado expresado por M.S. La idea de la posibilidad de separación cromatográfica de una mezcla de sustancias basadas en la diferencia en la solubilidad de la precipitación soluble en materia dura. Hubo una cromatografía de sedimentos.
En 1957, M. Golay propuso aplicar un sorbente en las paredes internas del tubo capilar: cromatografía capilar. Esta variante le permite analizar el microcolismo de las mezclas multicomponentes.
En los años 60, hubo la oportunidad de sintetizar los geles iónicos y no cargados, que tienen tamaños de poros estrictamente definidos. Esto hizo posible desarrollar una opción de cromatografía, cuya esencia consiste en separar la mezcla de sustancias sobre la base de la diferencia en su capacidad para penetrar en cromatografía en gel. Este método le permite separar las mezclas de sustancias con diferente peso molecular.
Actualmente, la cromatografía ha ganado un desarrollo sustancial. Hoy en día, varios métodos de cromatografía, especialmente en combinación con otros métodos físicos y fisicoquímicos, ayudan a los investigadores e ingenieros a resolver las tareas más diferentes, a menudo muy complejas en la investigación y la técnica científicas.
3. Clasificativométodos cromatográficos
La variedad de modificaciones y variantes del método de cromatografía requiere su sistematización o clasificación.
La base de la clasificación se puede poner en varios signos, a saber:
1. El estado agregado de las fases;
2. El mecanismo de separación;
3. El método de realizar el proceso;
4. El propósito del proceso.
Clasificación por el estado agregado de las fases:
gas (fase móvil - gas), gas-líquido (fase móvil - gas, fase fija - líquido), líquido (fase móvil - líquido) cromatografía.
Clasificación por mecanismo de separación.
La cromatografía de adsorción se basa en la adsorción selectiva (absorción) de componentes individuales de la mezcla mezclada con adsorbentes apropiados. La cromatografía de adsorción se divide en líquidos (cromatografía de adsorción líquida) y gas (cromatografía de adsorción de gas).
La cromatografía de intercambio de iones se basa en el uso de los procesos de intercambio de iones que se producen entre los iones móviles del adsorbente y los iones de electrolito cuando se analizó la solución del analito a través de la columna llena con sustancia de intercambio iónico (ionite). Los ionitos son compuestos insolubles inorgánicos y orgánicos de alto peso molecular. El óxido de aluminio se usa como ionitos, permutitis, sulfouggol y una variedad de sustancias de intercambio iónico orgánico sintético: resinas de intercambio de iones.
La cromatografía sedimentaria se basa en la solubilidad diferente de la precipitación formada por los componentes de la mezcla analizada con reactivos especiales. Por ejemplo, cuando la solución de la mezcla de ng (II) y las sales PB se pasa a través de una columna con un portador preimpregnado con una solución KI, se forman 2 capas de colores: parte superior, pintada en naranja-rojo (HGI 2), y abajo, pintado en amarillo (PBI 2).
Clasificación de acuerdo con el proceso de realizar el proceso.
La cromatografía en columna es un tipo de cromatografía en la que se utiliza una columna como portador para un disolvente fijo.
La cromatografía en papel es un tipo de cromatografía, en la que las tiras u hojas de papel de filtro que no contienen impurezas minerales se utilizan como portador para un solvente fijo en lugar de un altavoz. En este caso, se aplica una caída de una solución de prueba, por ejemplo, una mezcla de soluciones de sales (III) y CO (II), se aplica al borde de las tiras de papel. El papel se suspende en una cámara cerrada (Fig. 1), bajando su borde con una gota de la solución de prueba en un recipiente con un solvente móvil, por ejemplo con alcohol N-butílico. El disolvente móvil, moviéndose a través del papel, se asiente. En este caso, cada sustancia contenida en la mezcla analizada con la tasa inherente se mueve en la misma dirección que el disolvente. Al finalizar la separación de iones, el papel se seca y luego se pulveriza con un reactivo, en este caso con una solución K 4, que forma compuestos pintados con sustancias separables (azul, con iones de hierro, verde, con iones de cobalto). Las zonas formadas con todo esto en forma de manchas pintadas le permiten establecer la presencia de componentes individuales.
La cromatografía en papel en combinación con el uso de reactivos orgánicos hace posible realizar un análisis cualitativo de mezclas complejas de cationes y aniones. En un cromatograma, con la ayuda de un reactivo, se pueden detectar varias sustancias, ya que se caracteriza por no solo la tinción correspondiente, sino también una ubicación de cierta ubicación en el cromatograma.
La cromatografía de capa fina es un tipo de cromatografía en su mecanismo de separación similar a la cromatografía en papel. La diferencia entre ellos radica en el hecho de que en lugar de hojas de papel, la separación se lleva a cabo en placas recubiertas con una capa delgada de sorbente de óxido de aluminio en polvo, celulosa, zeolitas, gel de sílice, kizelur, etc. y sosteniendo un solvente fijo. La principal ventaja de la cromatografía de capas delgadas es la facelidez del equipo, la simplicidad y la alta velocidad del experimento, suficiente claridad de la separación de la mezcla de sustancias y en la capacidad de analizar el ultramrocolismo de la sustancia.
Clasificación para el propósito del proceso cromatográfico.
La cromatografía tiene el mayor valor como un método de análisis cualitativo y cuantitativo de mezclas de sustancias (cromatografía analítica).
Cromatografía preparativa: tipo de cromatografía, en la que la separación de la mezcla de sustancias se produce con fines preparativos, es decir, Para cantidades de sustancias más o menos significativas en pura, libres de impurezas. La tarea de la cromatografía preparativa también puede concentrarse y su posterior liberación de la mezcla de sustancias contenidas en forma de microstrums a la sustancia principal.
La cromatografía no analítica es un tipo de cromatografía, que se utiliza como método de investigación científica. Se utiliza para estudiar las propiedades de los sistemas, como soluciones, cinéticas de procesos químicos, propiedades de catalizadores y adsorbentes.
Por lo tanto, la cromatografía es un método universal para analizar las mezclas de sustancias, produciendo sustancias en forma pura, así como un método para estudiar las propiedades de los sistemas.
4. Cromatógrafoarreglar en una fase fija sólida
pero)Gas (G.azo adsorbovativo) Cromatografía
Cromatografía de gases: un método cromatográfico en el que la fase móvil es el gas. La cromatografía de gas recibió la mayor solicitud de separación, análisis e investigación de sustancias y sus mezclas, moviéndose sin descomposición en un estado de vapor.
Una de las variantes de cromatografía de gases es la cromatografía de adsorción de gas: este es un método en el que una fase fija es un adsorbente sólido.
En la cromatografía de gases, ya que la fase móvil (portador de gas) utiliza gas inerte: helio, nitrógeno, argón, significativamente menor que hidrógeno y dióxido de carbono. A veces, el gas portador sirve un par de fluidos volátiles.
El proceso cromatográfico de gas generalmente se lleva a cabo en dispositivos especiales llamados cromatógrafos de gas (Fig. 3). En cada uno de ellos, hay un sistema de flujo portador de gas, un sistema de preparación e inserción de la mezcla en estudio, una columna cromatográfica con un sistema de control de temperatura, analizando el sistema (detector) y un sistema para registrar los resultados de la separación y Análisis (grabadora).
La temperatura en la cromatografía de adsorción de gas tiene una temperatura. Su función consiste principalmente en cambiar el equilibrio de la sorción en el sistema de gas, un sólido. A partir de la selección correcta de la temperatura de la columna depende, el grado de separación de los componentes de la mezcla y la eficiencia de la columna, y la tasa total de análisis. Hay algún rango de temperatura de la columna en la que el análisis cromatográfico es óptimo. Típicamente, este intervalo de temperatura se encuentra en una región cerca del punto de ebullición del compuesto químico. Cuando los puntos de ebullición de los componentes de la mezcla difieren enormemente entre ellos, apliquen la temperatura de la temperatura de la columna.
La separación de la columna cromatográfica es la operación más importante, pero preliminar de todo el proceso de análisis cromatográfico de gases. Por encima de las mezclas binarias (componente de gas portador de gas) caen en el dispositivo de detección. Aquí hay una conversión de cambios en las concentraciones de componentes a lo largo del tiempo en una señal eléctrica, registrada utilizando un sistema especial en forma de curva, llamada cromatograma. Los resultados de toda la experiencia dependen en gran medida de la elección correcta del tipo de detector, su diseño. Hay varias clasificaciones de detectores. Diferentes detectores diferenciales e integrales. Los detectores diferenciales registran el valor instantáneo de una de las características (concentración o flujo) en el tiempo. Los detectores integrales resumen la cantidad de sustancia durante un cierto período de tiempo. Los detectores también se utilizan en el principio de acción, sensibilidad y propósito: termoconductótrico, ionización, espectroscópico, espectrométrico masivo, capulométrico y muchos otros.
Aplicación de la cromatografía de adsorción de gas.
La cromatografía de adsorción de gas se utiliza en la industria química y petroquímica para analizar los productos de síntesis química y petroquímica, la composición de las fracciones de petróleo, determinando la pureza de los reactivos y el contenido de productos clave en diferentes etapas de procesos tecnológicos, etc.
Análisis de gases permanentes y hidrocarburos ligeros, incluidos los isómeros, la cromatografía de gases ocupa de 5 a 6 minutos. Anteriormente, en los analizadores de gas tradicionales, este análisis duró 5 a 6 horas. Todo esto llevó al hecho de que la cromatografía de gases comenzó a ser ampliamente utilizada no solo en los institutos de investigación y los laboratorios de control y medición, sino que también se incluyen en el sistema de automatización integral de empresas industriales.
Hoy en día, la cromatografía de gas se utiliza en la búsqueda de campos de aceite y gas, lo que permite determinar el contenido de sustancias orgánicas que indican la proximidad de los campos de aceite y gas seleccionados de muestras de suelo.
La cromatografía de gases se usa con éxito en las penalizaciones, donde se usa para establecer la identidad de muestras de manchas sanguíneas, gasolina, aceites, alimentos falsos costosos, etc. Muy a menudo, la cromatografía de gases se utiliza para determinar el contenido del alcohol en la sangre de los conductores de automóviles. Unas gotas de sangre desde el dedo lo suficiente para averiguar cuánto cuándo y qué bebida alcohólica bebió.
La cromatografía de gases le permite obtener información valiosa y única sobre la composición de los olores de alimentos, como queso, café, caviar, brandy, etc. A veces, la información recibida por el análisis cromatográfico de gases no está feliz. Por ejemplo, a menudo en productos alimenticios, es innecesario que los pesticidas o el jugo de frutas contiene tricloroetileno, lo que, al contrario de las prohibiciones, se utilizó para aumentar el grado de caroteno de las frutas, etc. Pero es esta información la que protege la salud humana.
Sin embargo, a menudo hay casos cuando las personas simplemente descuidan la información recibida. En primer lugar se refiere al fumar. Un análisis cromatográfico detallado de gas ha establecido durante mucho tiempo que los cigarrillos de humo y el cigarrillo contienen hasta 250 hidrocarburos diferentes y sus derivados, de los cuales alrededor de 50 tienen un efecto carcinogénico. Es por eso que los fumadores tienen cáncer de pulmón en 10 veces más a menudo, pero aún millones de personas continúan envenenándose, sus colegas y parientes.
La cromatografía de gases se usa ampliamente en medicina para determinar el contenido de numerosos medicamentos, determinando el nivel de ácidos grasos, colesterol, esteroides, etc. En el cuerpo del paciente. Dichos análisis proporcionan información extremadamente importante sobre el estado de la salud humana, el curso de su enfermedad, la efectividad del uso de ciertos medicamentos.
La investigación científica en metalurgia, microbiología, bioquímica, en el desarrollo de la protección de las plantas y los nuevos medicamentos, en la creación de nuevos polímeros, materiales de construcción y en muchas otras áreas diferentes de la actividad práctica humana es imposible de imaginar sin un método analítico tan poderoso como gas. cromatografía.
La cromatografía de gas se usa con éxito para determinar el contenido de compuestos aromáticos policíclicos, peligrosos para la salud humana, en el agua y en el aire, el nivel de gasolina en el aire de los planos de las estaciones de servicio, la composición de los gases de escape del automóvil en el aire, etc.
Este método se usa ampliamente como uno de los principales métodos para monitorear la pureza del entorno.
La cromatografía de gases ocupa un lugar importante en nuestras vidas, brindándonos una cantidad colosal de información. En la economía nacional y en las organizaciones de investigación, se utilizan más de 20 mil de varios cromatógrafos de gas, que son asistentes indispensables para resolver muchas tareas complejas, derivadas diariamente de investigadores e ingenieros.
b)Líquido (adsorción líquida)cromatografía
La cromatografía líquida es un grupo de variantes de cromatografía en las que la fase móvil es líquida.
Una realización de la cromatografía líquida es la cromatografía de adsorción líquida: este es un método en el que una fase fija es un adsorbente sólido.
Aunque la cromatografía líquida se abrió antes que el gas, solo en la segunda mitad del siglo XX entró en el período de desarrollo exclusivamente intensivo. Actualmente, de acuerdo con el grado de desarrollo de la teoría del proceso cromatográfico y las técnicas de diseño instrumental, de acuerdo con la eficiencia y la tasa de separación, es poco probable que renuncie al método de separación de gas cromatográfico. Al mismo tiempo, cada uno de estos dos tipos principales de cromatografía tiene su propio alcance principal. Si la cromatografía de gases es principalmente adecuada para el análisis, la separación y la investigación de productos químicos con un peso molecular de 500 a 600, luego se puede usar cromatografía líquida para sustancias con un peso molecular de varios cientos y varios millones, incluidas macromoléculas extremadamente complejas de polímeros, proteínas. y ácidos nucleicos. Al mismo tiempo, la oposición de varios métodos cromatográficos está inherentemente desprovista del sentido común, ya que los métodos cromatográficos se complementan con éxito entre sí, y a la tarea de un estudio específico, es necesario abordar de manera diferente, a saber, qué método cromatográfico Le permite resolverlo con más velocidad, informatividad y con menos costo.
Como en cromatografía de gases, los detectores se utilizan en la cromatografía líquida moderna, que puede fijar continuamente la concentración de la sustancia determinada en el flujo de fluido que fluye fuera de la columna.
El detector universal para cromatografía líquida no existe. Por lo tanto, en cada caso particular, debe seleccionarse en el Detector de la Unión más grande. Los detectores ultravioleta, refractométrica, microaccionales, detectores de ionización de refracción fueron mayores.
Detectores espectrométricos. Los detectores de este tipo son dispositivos selectivos altamente sensibles, lo que permite concentraciones de sustancias muy pequeñas en la corriente de la fase líquida. Su testimonio depende poco de las fluctuaciones de la temperatura y otros cambios aleatorios del medio. Una de las características importantes de los detectores espectrométricos es la transparencia de los disolventes más utilizados en la cromatografía de adsorción líquida en el área de trabajo de longitudes de onda.
La mayoría de las veces utilizan la absorción en UV, con menos frecuencia en la región IR. En la región UV, se utilizan electrodomésticos que operan en una amplia gama, desde 200 nm hasta la parte visible del espectro, o en ciertas longitudes de onda, con mayor frecuencia a 280 y 254 nm. Las bombillas de baja presión de mercurio (254 nm), la presión media (280 nm) y los filtros correspondientes se utilizan como fuentes de radiación.
Micro detectores de persorción. La base de los detectores de microfectos se basa en la liberación de calor durante la adsorción de la sustancia en el adsorbente, que se llena con la celda detector. Sin embargo, se mide, no el calor, sino la temperatura del adsorbente, al que se calienta como resultado de la adsorción.
Un detector de microditos es una herramienta bastante altamente sensible. Su sensibilidad depende principalmente del calor de la adsorción.
Los detectores micro perseguidos son universales, adecuados para detectar sustancias tanto orgánicas como inorgánicas. Al mismo tiempo, son difíciles de obtener cromatogramas bastante claros, especialmente con la separación incompleta de los componentes de la mezcla.
5. Cromatógrafoatia en fase fija líquida.
a) cromatografía de gas-líquido
Cromatografía de gas-líquido: un método cromatográfico de gas en el que una fase fija es un líquido joven aplicado a un vehículo sólido.
Este tipo de cromatografía se utiliza para separar los gases y vapores de líquidos.
La principal diferencia en el gas-líquido de la cromatografía de gas-adsorción es que en el primer caso, el método se basa en el uso del proceso de disolución y la posterior evaporación del gas o el vapor de la película líquida sostenida por el portador inerte sólido; En el segundo caso, el proceso de separación se basa en la adsorción y la desorción posterior de gas o vapor en la superficie del sólido: adsorbente.
El proceso cromatográfico se puede representar esquemáticamente de la siguiente manera. Se inyecta una mezcla de gases o vapores de líquidos volátiles con un flujo de gas portador en una columna llena con un portador inerte fijo, en el que se distribuye un líquido no volátil (fase fija). Los gases y pares estudiados son absorbidos por este líquido. Luego, los componentes de la mezcla compartida se desplazan de forma selectiva en un orden específico de la columna.
En la cromatografía de gas-líquido, se usan una serie de detectores que reaccionan específicamente a cualquier sustancia orgánica o en sustancias orgánicas con un grupo funcional específico. Estos incluyen detectores de ionización, detectores de captura electrónicos, térmicos, espectrofotométricos y algunos otros detectores.
Detector de ionización de llama (PID). El trabajo de la PID se basa en el hecho de que las sustancias orgánicas que caen en la llama del quemador de hidrógeno están sujetas a la ionización, como resultado de lo cual la ionización es simultáneamente una ionización, que es simultáneamente una cámara de ionización, que es proporcional a El número de partículas cargadas.
PID es sensible solo a compuestos orgánicos y no es sensible o muy sensible a los gases como los óxidos de aire, azufre y carbono, sulfuro de hidrógeno, amoníaco, carbono, vapor de agua y a varios otros compuestos inorgánicos. La insensibilidad del PID al aire le permite aplicarlo para determinar la contaminación del aire por varias sustancias orgánicas.
Cuando se trabaja con el PID, se usa 3 gas: portador de gas (helio o nitrógeno), hidrógeno y aire. Los 3 gases deben tener un alto grado de pureza.
Detector de argón. En el detector de argón, la ionización es causada por la colisión de las moléculas de la sustancia determinada con átomos de argón metástibles que resultan de los efectos de la radiación radiactiva.
Detector térmico. El principio del detector de termoonía es que las sales de metal alcalino, que se evaporan en el quemador de llama, se reaccionan selectivamente con los compuestos que contienen halógenos o fósforo. En ausencia de tales compuestos en la cámara de ionización del detector, se establece un equilibrio de átomos de metal alcalino. La presencia de átomos de fosforne debido a su reacción con átomos de metal alcalino viola este equilibrio y causa la aparición en la cámara de corriente iónica.
Dado que el detector térmico tiene la mayor sensibilidad a las conexiones que contienen fósforo, recibió el nombre del fosfato. Este detector se utiliza principalmente para analizar pesticidas fosforodinorgánicos, insecticidas y una serie de compuestos biológicamente activos.
b)Gel cromategra.fIA
Cromatografía en gel (filtración del gel): método de separación de mezclas de sustancias con diferentes pesos moleculares al filtrar la solución analizada a través de geles celulares reticulados transversales.
La separación de la mezcla de sustancias ocurre en el caso de que las dimensiones de las moléculas de estas sustancias sean diferentes, y el diámetro de los granos de gel es constante y solo las moléculas pueden pasar, cuyas dimensiones son más pequeñas que el diámetro de la Poros de gel. Al filtrar la solución de una mezcla de la mezcla, las moléculas más pequeñas penetradas en los poros del gel, se retrasan en el disolvente contenidas en estos poros, y se mueven a lo largo de la capa de gel más lenta que las moléculas grandes que no son capaces de penetrar en los poros. Por lo tanto, la cromatografía en gel le permite separar la mezcla de sustancias dependiendo del tamaño y el peso molecular de las partículas de estas sustancias. Este método de separación es bastante simple, rápido y, lo que es más importante, le permite separar las mezclas de sustancias en condiciones de limo que otros métodos cromatográficos.
Si los gránulos de gel llenan la columna y luego vierte una solución de varias sustancias con un peso molecular diferente en él, cuando la solución se mueve a lo largo de la capa de gel en la columna, se llevará a cabo esta mezcla.
El período inicial de la experiencia: aplicar la solución de la mezcla analizada en la capa de gel en la columna. La segunda etapa: gel no interfiere con la difusión de moléculas pequeñas en los poros, las moléculas más grandes permanecen en solución que rodea los gránulos de gel. Cuando se lava con una capa de gel con un disolvente puro, las moléculas grandes comienzan a moverse a una velocidad cercana a la velocidad del movimiento solvente, mientras que las moléculas pequeñas deben primero predefinir de la edad interna del gel en el volumen entre los granos y como un El resultado de esto se retrasa y se lava con el solvente más tarde. Se produce una mezcla de sustancias de acuerdo con su peso molecular. Las sustancias de lavado de la columna ocurren para reducir su peso molecular.
El uso de cromatografía en gel.
El propósito principal de la cromatografía en gel es la separación de mezclas de altos compuestos moleculares y la determinación de la distribución de masa molecular de los polímeros.
Al mismo tiempo, se usa una cromatografía igualmente en gel para separar la mezcla de sustancias de peso molecular medio e incluso conexiones de peso molecular bajo. En este caso, es importante que la cromatografía en gel hace posible separarse a temperaturas de la habitación, lo que lo distingue favorablemente de la cromatografía de gas-líquido que requiere calentamiento para transferir las sustancias analizadas a la fase de vapor.
La separación de la mezcla de sustancias por cromatografía en gel es posible y cuando los pesos moleculares de las sustancias analizadas son muy cercanas o incluso iguales. En este caso, se usa la interacción de los solutos con gel. Esta interacción puede ser tan significativa, lo que reduce las diferencias en los tamaños de las moléculas. Si la naturaleza de la interacción con el gel para diferentes sustancias es no idas, esta diferencia se puede usar para separar la mezcla de intereses.
Un ejemplo es el uso de cromatografía en gel para el diagnóstico de enfermedades de la tiroides. El diagnóstico se establece mediante el número de yodo definido durante el análisis.
Los ejemplos anteriores del uso de cromatografía en gel muestran sus amplias oportunidades para resolver una amplia variedad de tareas analíticas.
Conclusión
Como método científico de aprendizaje que nos rodea, la cromatografía se desarrolla y mejora constantemente. Hoy en día se aplica tan a menudo y tan ampliamente en la investigación científica, la medicina, la biología molecular, la bioquímica, la tecnología y la economía nacional, que es muy difícil de encontrar el área de conocimiento en la que se utilizaría la cromatografía.
La cromatografía como método de estudio con sus capacidades excepcionales es un factor poderoso en el conocimiento y la transformación de un mundo de complicación en los intereses de crear condiciones de hábitat humano aceptables en nuestro planeta.
Con p y con a punto deL y t e r y t u r s
1. IVAZOV B.V. Introducción a la cromatografía. - M.: Mayor. Sk., 1983 - s. 8-18, 48-68, 88-233.
2. Kreshkov a.p. Conceptos básicos de la química analítica. Bases teóricas. Análisis cualitativo, el primer libro, Ed.4-E, recreación. M., "Química", 1976 - p. 119-125.
3. Sakodynsky K.I., Orekhov B.I. Cromatografía en ciencia y tecnología. - M.: Conocimiento, 1982 - p. 3-20, 28-38, 58-59.