Как да стигнем от етан хлорхетан в органична химия. Как да се получи хлоретан от етилов алкохол като от хлоретан за получаване на етанол
Химична формула Етилов алкохол (етанол) - C2H5ON. И веществото е хлоретан, използвано като хладилен агент и за анестезия за медицински цели, има C2H5SL формула. Тези вещества са близки в състав, само в първия случай, хидроксилната група е прикрепена към етилов радикал на С2Н5 и във втория йон хлор. Възможно е да се получи химически начин като етанол от хлоретан и хлороантан от етанол.
Инструкция
Съществуват редица начини за получаване на химическа трансформация на хлорхетан от етилов алкохол. Например, възможно е да се претърпи контейнер с етанол със силно нагряване в присъствието на концентрирана сярна киселина. И тогава образуваният газ е етилен, за да се комбинира с газообразен хлорид. Ето диаграмата на първия етап на реакцията: C2H5ON \u003d C2H4 + Н20.
Получената вода се абсорбира от концентрирана сярна киселина, която е много хигроскопична. Газообразен етилен се сглобява в друг контейнер, свързан към реакционната колба, използвайки стъклен адаптер.
При взаимодействието на получения етилен с газообразен хлорид се образува хлороетан. Ето схемата на втория етап на реакцията: C2H4 + NSL \u003d C2H5SL.
Тази реакция се появява в присъствието на катализатор - желязо три хлорид. Между другото, в индустрията, хлорхетан се получава по този начин (разбира се, без да се използва етилов алкохол като първоначален суровина).
Възможно е да се получи хлороантейн, като се използва реакцията на взаимодействие на етилов алкохол с пет хлорид фосфор. След смесване на тези вещества, реакционната смес се прехвърля във вода и с разделяща фуния, органичната част (хлорохетана) се отделя от неорганичната част поради факта, че хлорьоатът е много слабо смесен с вода. Реакцията протича както следва: C2H5ON + PCL5 \u003d C2H5SL + HCI + POCL3.
Има и друг популярен лабораторен метод за производство на хлоретан от етилов алкохол. Когато взаимодействието на етанол с тионил хлорид се получава хлорхетан, солна киселина и газообразен серен диоксид. Възможно е да се отдели органичната фаза от неорганиката, както в предишния пример, с дивизионна фуния. Реакцията е при такава схема: C2H5ON + SOC1 \u003d C2H5Cl + HCI + SO2.
Във втория случай реакцията е напълно нерентабилна в икономически смисъл и е само практически интерес.
Хлороетанът е запалим прилеп, който има особена миризма и безцветен цвят. Хлороетанът много често се използва в медицинската практика за анестезия или инхалационна анестезия. Това е доста мощно наркотично лекарство, благодарение на което анестезията се среща много бързо, буквално в рамките на няколко минути. Основният недостатък на това химическо вещество, е задухът на действие, т.е. след анестезия, пробуждането се случва след 20 минути, така че може да се използва само с краткосрочни хирургични интервенции. Може да се използва и като локално аналгетично средство за дерматит, спортни наранявания, натъртвания, ухапване от насекоми, възпаление и др.
В органична химия Има различни видове химични реакции:
1. Допълване (елиминиране)
Това са химични реакции, в резултат на което се образуват молекули от няколко нови вещества от изходната молекула. Много важни сред елиминационните реакции има термично разделяне на въглерод.
2. Присъединяване
В резултат на тези реакции няколко молекули реагират вещества са свързани в едно. то основна характеристика Реакции на приставката.
3. Замяна
При извършване на тези реакции се заменя един атом или група атоми към друг атом или друга група атома.
4. Пренареждане (изомеризация)
В резултат на тези реакции от молекулите на едно вещество се образуват молекули на други вещества.
Как от етилен получава хлорхетан
В този случай ще използваме реакцията на добавянето - хидро-зареждане (Halo-ген водороден закрепване). Така, хлороантетан от етилен може да бъде получен от следната реакция:
C2H4 + HCI \u003d C2H5Cl
Как да получите етанол от хлороетан
Сега трябва да използваме химическа реакция - замяна с алкали, в резултат на което получаваме алкохол и сол:
C2H5CI + NaOH \u003d C2H5OH + NaCl
Как да получите хлорхетан
За да се получи хлороантхане от етан, ние използваме обичайния халогенид на алкани. Само, трябва да помните едно важно условие, реакцията трябва да се извърши в присъствието на светлина. Тук химическо уравнениеТази реакция.
За да разберем как да стигнете от етан хлорхетан, първо анализирайте характеристиките на етан.
Кратко описание на етан
Този въглеводород има C2H6 формула. Карбоните в нейната молекула са в SP3 хибридно състояние. Това се отразява във физическото и. \\ T химични свойства Това вещество. При нормални условия етанът е газообразна субстанция чрез слабо разтворима във вода. Както всички останали представители на класа Алканов, Итън има богати прости връзки. Това се отразява в химичните свойства на този въглеводород. Не е в състояние да се присъедини към реакцията, е допустимо само радикално заместване.
Особеност
Разберете как да стигнете от етан хлорхетан. За да направите това, е необходимо да се реагира между етана и хлора в присъствието на квантова светлина (повишена температура). Благодарение на Gomolitical счупване на връзката се образуват хлорни радикали. За образованието изисква определени енергийни разходи.
Тя може да бъде закупена по различни начини. Термичната пиролиза може да се разглежда като един от варианта на образуването на радикали. За да се получи хлоретан от етан, уравнението се записва при температура от около 500 0 S. на енергията, която ще бъде подчертана, достатъчно за счупване на връзки. Вторият метод за образуване на активни радикали е използването на ултравиолетова радиация.

Механизъм за радикална замяна
Помислете как от етана да получите хлорхетан. Той приема механизма на халогените на SR-действие с алкани. В газовата фаза, по време на реакцията на етана с хлор, се появява хлорното дисоциация под действието на UV. Този етап се нарича иницииране, то се характеризира с появата на активни частици от хлорни радикали. Получените частици атакуват етановата молекула, образувайки хлорен водород, както и етилов радикал C2H5.
Ще продължим разговора как да стигнем от този хлорхетан. На следващия етап етил радикалът влиза във взаимодействие с хлорната молекула, образувайки енчелорид и друг хлорен радикал. Той е този, който е в състояние да реагира да реагира, продължавайки цикъла верижна реакция. Този етап се нарича нарастваща верига. Броят на активните радикали на този етап на взаимодействие не се променя и се запазва изцяло. Тъй като завършването на цикъла третият етап от реакцията се нарича повреда на веригата. Това предполага сблъсъци на свободни частици, което води до реакционни продукти.

Приложение
Отговорът на въпроса как да се получи от етан хлорхетан. Да се \u200b\u200bсъсредоточим върху прилагането. Полученият хлороетил е сериозно наркотично вещество. Използва се като лекарство в хирургическите операции. Достатъчно е два до три секунди, за да се сведе до минимум двигателната активност.
Като основна липса на това вещество, ние отбелязваме възможността за предозиране. Дори незначително увеличение на допустимата норма причинява сериозни проблеми за човешкото тяло. В днешно време в някои случаи хлоретан се използва в някои случаи като наркотично вещество.
В повече от Тя е търсена като местен агент за краткосрочна облекчение на повърхността. Намирането на кожата, веществото се изпарява, настъпва се чувствителността му, което води до възможността за рязане, т.е. извършване на малки повърхностни операции.
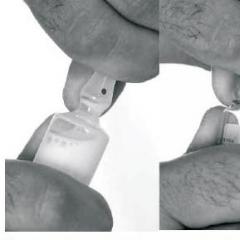
Това вещество се използва и за намаляване на сърбеж на кожата, третиране на термични изгаряния, невромаизити, криотерапия на възпалението. Ампулата първо се загрява в дланта на дланта, след което струята върху кожата е насочена. За терапевтични цели процедурата се провежда веднъж дневно в продължение на 7-10 дни.
Халогенни производни на въглеводороди - продукти за редуциране на водородни атоми в въглеводороди на един или повече халогенни атоми.
Повечето халогенни производствени въглеводороди (халоалкили) са много реактивни връзки. Най-големите стойности за връзките на този клас имат реакции на заместване и разцепване. Химичните свойства на халогеналкил се определят първо от цялата комбинация от С - Х (x \u003d F, С1, br, i). Свързването на С - Х в халолилала се характеризира с повишена полярност. Това се обяснява с по-голямата електрическа загуба на халогенен атом в сравнение с въглерода, с който е свързан.
Изместването на електронната плътност настъпва към халогенен атом (-I ефект). Такова преразпределение на електронната плътност води до факта, че на халогенен атом възниква частичен отрицателен заряд () и на въглеродния атом - частично положително ( +):
В резултат на това -свързването на С - Х става поляризирано. Намалената електронна плътност върху въглеродния атом и определя високо, за разлика от ограничаващите въглеводороди, реакционния капацитет на халогенни производни, които лесно влизат в реакцията на нуклеофилно заместване (s) и разцепване (елиминиране) (Е).
Лабораторна работа
Цел на работа:изследване на методите за получаване и химични свойства на халогенни производни на въглеводороди.
Реагенти и оборудване:2N.NAOH; H2S04 конц.; 0,2N.AGNO 3; I 2 в разтвор; хлорбензол; етанол; NaCl (телевизор); Хлорал хидрат (крист).
статив с епруветки; държач за изпитвани тръби; Кожни очила; Алкохол, микроскоп.
Опит 3.1 Създаване на хлоретан от етанол
Сатриотични кристали на натриев хлорид се изливат в епруветката от около 3 mm и се добавят 3-4 капки етилов алкохол. Така че цялата сол се навлажнява с алкохол. След това добавете 3-4 капки сярна киселина и нагрявани над алкохолния пламък не се допуска твърде бързо изолиране на хлороводород. За да се контролира прогресът на образуването на хлорхетан, дупката на тестовата епруветка към пламъка на алкохола и запалва (хлороетан изгаря с образуването на характерни пръстени на зелено). След първоначалното отопление, веднага щом бъде забелязан поне слаб зелен хлоретан, нагряването се спира. Необходимо е да се напишат уравненията на реакциите.
Забележка.Не е необходимо да се загрява тестовата тръба без нужда, тъй като се различава значително количество хлороводород. Поради тази причина не трябва да се опитвате да идентифицирате миризмата на хлорхетан.
Насладете се на 3.2Отложна хлороформ от хлорохидрат
3-4 хлорохидрат кристал се поставят в тръбата, се прибавят 6-8 капки 2N. NaOHS са леко нагрят от течност, която вече е пушена при стайна температура. Какво става? Трябва да обърнете внимание на миризмата на получената течност, сравнявайки го с миризмата на хлороформ от колбата. Необходимо е да се напишат уравненията на реакциите.
Опит 3.3production на етанол йодоформ
2 капки етанол се поставят в тръбата, 3 капки йоден разтвор в калиев йодист и 3 капки 2N. NaOH. С слабо отопление, (понякога дори от топлина) се появява бял факел с характерен много устойчив мирис на йодоформи. Когато мути се разтвори, към топъл разтвор се добавят още 3-5 капки от йодния разтвор. Изчакайте 2-3 минути преди образуването на кристали. След това, с помощта на пипети, те вземат 2 капки течност с кристали от йодоформи от дъното на тръбата с кристали към микроскопа и скицират формата на получените кристали в списанието. Напишете уравненията на реакциите.
Забележка. Загрейте сместа от йод с алкохол и алкали за кипене, но не се заварявайте, тъй като образуването на йодоформ ще бъде открито.
Опит 3.4. Сравнителна мобилност на халоген в бензеновото ядро

а) Итън от метан може да бъде получен на два етапа. Когато се образува хлорографски метан, хлорометан:
Когато хлорометанът взаимодейства с натриев етан (реакция на Würtz):
От етанол в два етапа можете да получите етанол. При хлоро-етано се образува хлорхетан:
При действие по хлоретан водно решение Образува се алкалният атом върху хидроксилната група и етанол.
Итън от етанол може да бъде получен и на два етапа. При нагряване етанол със сярна киселина се появява дехидратация и се образува етилен:
b) При нагряване на етанол със сярна киселина се появява дехидратация и се образува етилен:
При хидрогениране на етилен върху катализатора се образува етанка:
При хлоро-етано се образува хлорхетан:
Може да се получи от хлорхетан в два етапа оцетен алдехид. При действието на хлорхетан воден алкален разтвор се образува етанол.
Когато се нагрява, етанолът се окислява чрез меден оксид в оцетен алдехид:

в) бутадиен може да бъде получен директно от етилов алкохол при нагряване в присъствието на катализатор, докато се появява едновременно дехидрогениране (водородно разцепване) и дехидратация (почистване на вода):
г) със силно нагряване на калциев карбонат с въглерод, се образува калциев карбид:
При действие върху калциев карбид се получава ацетилен:
Етилов алкохол от ацетилен може да бъде получен на два етапа. Когато се образува хидрогениране на ацетилен в присъствието на катализатора, се образува етилен.