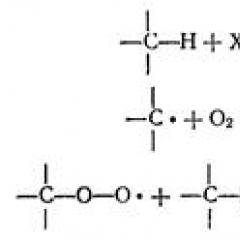
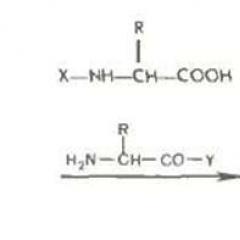
واکنش واکنش لیگاند ها. مجتمع های واکنش پذیری
شیمی عمومی: کتاب درسی / A. V. Zhulkhan؛ اد. V. A. Popkov، A.V. Zhoglovna. - 2012. - 400 p: IL.
فصل 7. ترکیبات پیچیده
فصل 7. ترکیبات پیچیده
عناصر جامع سازمان دهندگان زندگی هستند.
K. B. Yatimirsky
ترکیبات پیچیده طبقه بندی گسترده تر و متنوع تر از ترکیبات هستند. در موجودات زنده، ترکیبات پیچیده فلزات بیوژنیک با پروتئین ها، اسیدهای آمینه، ریزه های پورفی، اسیدهای نوکلئیک، کربوهیدرات، ترکیبات ماکروسیکلیک وجود دارد. مهمترین فرآیندهای فعالیت حیاتی با مشارکت ترکیبات پیچیده ادامه می یابد. برخی از آنها (هموگلوبین، کلروفیل، هموسینین، ویتامین B 12، و غیره) نقش مهمی در فرایندهای بیوشیمیایی ایفا می کنند. بسیاری از داروها حاوی مجتمع های فلزات هستند. به عنوان مثال، انسولین (مجتمع روی)، ویتامین B 12 (مجتمع کبالت)، پلاتین (پیچیده پلاتین) و غیره
7.1 نظریه هماهنگی A. verner
ساخت ترکیبات پیچیده
تعامل ذرات هماهنگی متقابل ذرات را مشاهده می کند که می تواند به عنوان یک فرآیند تشکیل پیچیده تعریف شود. به عنوان مثال، فرایند هیدراتاسیون یون ها به پایان می رسد با تشکیل Aquacompleks. واکنش های پیچیده همراه با انتقال جفت های الکترونیکی همراه است و منجر به تشکیل یا تخریب ترکیبات بالاتر، ترکیبات پیچیده (هماهنگی) می شود. یکی از ویژگی های ترکیبات پیچیده، حضور یک پیوند هماهنگی ناشی از مکانیسم گیرنده اهدا کننده است:
ترکیبات پیچیده ترکیباتی هستند که هر دو در حالت بلورین و در محلول، ویژگی دارند
که حضور یک اتم مرکزی احاطه شده توسط لیگاندها است. ترکیبات پیچیده را می توان به عنوان ترکیبات پیچیده ای از نظم بالاتر متشکل از مولکول های ساده ای که قادر به وجود مستقل در محلول است، در نظر گرفته شود.

با توجه به نظریه هماهنگی ورنر در اتصال پیچیده متمایز است درونی؛ داخلیو حوزه های خارجیاتم مرکزی با لیگاندهای اطراف آن، حوزه درونی این مجموعه را تشکیل می دهد. این معمولا در براکت های مربع به پایان می رسد. هر چیز دیگری در ترکیب پیچیده یک کره خارجی است و فراتر از براکت های مربع نوشته شده است. تعداد مشخصی از لیگاند ها در اطراف اتم مرکزی بیان شده است که تعیین می شود. شماره هماهنگی(CC). تعداد لیگاندهای هماهنگ شده اغلب برابر 6 یا 4 است. لیگاند یک مکان هماهنگی در نزدیکی اتم مرکزی را اشغال می کند. هنگامی که هماهنگی، خواص هر دو لیگاند و اتم مرکزی تغییر می کنند. اغلب لیگاندهای هماهنگ را نمی توان با استفاده از واکنش های شیمیایی مشخصه آنها در یک کشور آزاد شناسایی کرد. ذرات مرتبط با قوی تر از حوزه داخلی نامیده می شود مجتمع (یونی پیچیده).نیروهای جاذبه بین اتم مرکزی و لیگاند ها عمل می کنند (یک پیوند کووالانسی برای تبادل و (یا) مکانیسم گیرنده اهدا کننده تشکیل شده است)، بین لیگاندها - نیروهای انفجاری. اگر اتهام حوزه داخلی 0 باشد، حوزه هماهنگی خارجی وجود ندارد.
اتم مرکزی (عامل پیچیده)- اتم یا یون، که موقعیت مرکزی را در ترکیب پیچیده اشغال می کند. نقش عامل پیچیده اغلب توسط ذرات دارای مداری آزاد و یک بار مثبت مثبت هسته انجام می شود و بنابراین می تواند گیرنده های الکترون باشد. اینها کاتیون عناصر انتقال هستند. قوی ترین مجتمع ها عناصر گروه های IB و VIIIB هستند. به ندرت به عنوان پیچیده است
retributors اتمهای خنثی از عناصر D و اتم های غیر فلزی در مقادیر مختلف اکسیداسیون هستند. تعداد اوربیتال های اتمی آزاد ارائه شده توسط عامل پیچیده، تعداد هماهنگی آن را تعیین می کند. مقدار تعداد هماهنگی بستگی به عوامل بسیاری دارد، اما معمولا برابر با شارژ بهینه سازی یک عامل الکلینگ است:

لیگاند- یون ها یا مولکول هایی که به طور مستقیم به عامل پیچیده مرتبط هستند و اهدا کنندگان جفت های الکترونیکی هستند. این فایل های الکترونیکی دارای جفت های الکترونیکی رایگان و تلفن همراه می توانند اهداکنندگان الکترونها باشند، به عنوان مثال:
ترکیبات P-leams خواص پیچیده ای را نشان می دهند و در یک ارتباط جامع به عنوان لیگاندها عمل می کنند. لیگاند ممکن است اتم ها و مولکول ها (پروتئین، اسیدهای آمینه، اسیدهای نوکلئیک، کربوهیدرات) باشد. با توجه به تعداد اتصالات تشکیل شده توسط لیگاندها با یک مربی پیچیده، لیگاندها به لیگاندهای مونو، دی و پلی اتیل تقسیم می شوند.لیگاندهای بالا (مولکول ها و آنیون ها) مونودن تاتات هستند، زیرا آنها اهدا کنندگان یک جفت الکترونیکی هستند. لیگاند های بنیادی شامل مولکول ها یا یون های حاوی دو گروه کاربردی هستند که قادر به اهداکننده دو جفت الکترونیکی هستند:

لیگاند های پلی اتیلن شامل لیگاند اسید اتیل سدیم اتیل سدیم 10 دندان است:

تعداد مکان های اشغال شده توسط هر لیگاند در حوزه داخلی یک ترکیب جامع نامیده می شود ظرفیت هماهنگی (دندانپزشکی) لیگاند.این تعدادی از جفت های الکترونیکی لیگاند تعیین می شود که در شکل گیری ارتباطات هماهنگی با اتم مرکزی دخیل هستند.
علاوه بر ترکیبات پیچیده، شیمی هماهنگ، نمک های دوگانه را پوشش می دهد، کریستال هیدرات ها در یک محلول آبی به قطعات کامپوزیتی تجزیه می شوند که در حالت جامد در بسیاری از موارد به همان شیوه ای پیچیده می شود، اما ناپایدار است.
پایدار ترین و متنوع ترین مجتمع های ترکیب شده و توابع انجام شده توسط D-Elements تشکیل شده است. ترکیبات جامع عناصر انتقال بسیار مهم هستند: آهن، منگنز، تیتانیوم، کبالت، مس، روی و مولیبدن. S-b-biogenics (Na، K، Mg، CA) ترکیبات جامع را فقط با لیگاندهای یک ساختار چرخه ای خاص تشکیل می دهند، همچنین به عنوان یک عامل پیچیده صحبت می کنند. بخش اصلی r-Elements (N، P، S، O) بخش فعال ذرات تشکیل دهنده پیچیده (لیگاند)، از جمله Bioligands است. این شامل اهمیت بیولوژیکی است.
در نتیجه، توانایی پیچیدگی، مالکیت عمومی عناصر شیمیایی سیستم دوره ای است، این توانایی به ترتیب زیر کاهش می یابد: f.> d.> پ.> s
7.2. تعیین اتهام ترکیب اصلی ذرات اصلی
اتهام حوزه درونی ترکیب مجتمع، مقدار جبری اتهامات ذرات تشکیل شده است. به عنوان مثال، ارزش مجموعه مجتمع این مجموعه به شرح زیر تعیین می شود. شارژ آلومینیوم یونی +3، کل شارژ شش هیدروکسید -6. در نتیجه، اتهام این مجموعه برابر با (+3) + (-6) \u003d -3 و فرمول مجموعه 3- است. اتهام یک یون یکپارچه به صورت عددی برابر با اتهام کل حوزه خارجی است و با علامت او مخالف است. به عنوان مثال، اتهام کره بیرونی K 3 + 3 است. در نتیجه، اتهام یون پیچیده -3 است. اتهام تئاتر مجتمع برابر با اندازه است و در مقابل نشانه ای از میزان جبری اتهامات تمام ذرات دیگر ترکیب پیچیده است. از اینجا، در K 3، اتهام یون آهن +3 است، زیرا کل اتهام کل ذرات دیگر ترکیب پیچیده (+3) + (-6) \u003d -3 است.
7.3. nomenclature ترکیبات پیچیده
پایه های nomenclature در آثار کلاسیک ورنر طراحی شده اند. مطابق با آنها، در ترکیب پیچیده، کاتیون اول به نام، و سپس آنیون است. اگر اتصال نوع غیر الکتریکی نوع، سپس آن را در یک کلمه نامیده می شود. نام یون مجتمع به یک کلمه نوشته شده است.
لیگاند خنثی همانند مولکول نامیده می شود، و آنیون های لیگاند ها در انتهای "O" اضافه می شوند. برای یک مولکول آب هماهنگ شده، تعیین "Aqua" استفاده می شود. برای اشاره به تعداد لیگاندهای یکسان در حوزه درونی این مجموعه به عنوان یک کنسول قبل از نام لیگاند، عدد یونانی دی، سه، تترا، پنتا، هگزا- و غیره استفاده می شود. Confix Mononux مصرف می کند لیگاندها به ترتیب حروف الفبا ذکر شده اند. نام لیگاند به عنوان یک کل در نظر گرفته شده است. پس از نام لیگاند، نام اتم مرکزی نشان دهنده درجه اکسیداسیون است که توسط اعداد رومی در پرانتز نشان داده شده است. کلمه ammin (با دو "M") در رابطه با آمونیاک نوشته شده است. برای همه آمین های دیگر، تنها یک "M" استفاده می شود.
C1 3 - hexamincobalt (III) کلرید.
C1 3 - Aquapentamicobalt (III) کلرید.
CL 2 - pentamethylamminchlorocobalt (III) کلرید.
Diammindibromoptiny (II).
اگر یون یکپارچه یک آنیون باشد، نام لاتین آن پایان "AM" است.
(NH 4) 2 - آمونیوم تتراکلروپالدات (II).
K - پتاسیم پنتبرومامامین پلاتین (IV).
K 2 - پتاسیم تتراتودودندانوبالتات (II).
نام لیگاند پیچیده معمولا در پرانتز به پایان می رسد.
NO 3 - dichloro-di- (ethylenediamine) نیترات کبالت (III).
BR - Bromo-tris- (triphenylphosphin) Platinum (II) برومید.
در مواردی که لیگاند دو یونهای مرکزی را متصل می کند، نامه یونانی قبل از نام آن استفاده می شودμ.

چنین لیگاند ها نامیده می شوند پلو آخرین لیست
7.4 پیوند شیمیایی و ساختار ترکیبات پیچیده
در شکل گیری ترکیبات پیچیده، تعاملات اهدا کننده گیرنده لیگاند و اتم مرکزی نقش مهمی ایفا می کنند. اهدا کننده جفت الکترونیکی معمولا لیگاند است. یک پذیرنده یک اتم مرکزی است که دارای مداری آزاد است. این اتصال با دوام است و زمانی که مجتمع حل می شود، شکست نمی خورد (Neoio-noun)، و آن را نامیده می شود هماهنگی
همراه با پیوندها، π-bonds برای یک مکانیزم کمک کننده اهدا کننده تشکیل شده است. در عین حال، اهدا کننده به یک یون فلز می پردازد، الکترونهای D زوجه خود را با لیگاند می برد، که دارای مدارهای خالی قابل ملاحظه ای است. چنین اتصالات به نام DATION نامیده می شود. آنها شکل می گیرند:
الف) با توجه به همپوشانی از جای خالی فلزات P-orbitals با فلز D یا BETIAL، که الکترونهایی که به σ- ارتباطات وارد نشده اند وجود دارد؛
ب) هنگام همپوشانی لیگاند خالی D-Orbital با فلز D-Orbital پر شده است.
اندازه گیری قدرت آن، میزان همپوشانی از اوربیتال های لیگان و اتم مرکزی است. جهت اوراق قرضه اتم مرکزی هندسه این مجموعه را تعیین می کند. برای توضیح تمرکز پیوندها، بازنمایی هیبریداسیون اوربیتال های اتمی اتم مرکزی استفاده می شود. اوربیتال های ترکیبی از اتم مرکزی نتیجه مخلوط کردن اوربیتال های اتمی ناهموار هستند، به عنوان یک نتیجه، فرم و انرژی تغییرات مداری به طور متقابل تغییر می کند و Orbi-Tali با همان شکل و انرژی شکل می گیرد. تعداد اوربیتال های هیبریدی همیشه برابر با تعداد منبع است. ابرهای هیبریدی در یک اتم در حداکثر فاصله از یکدیگر قرار دارند (جدول 7.1).
جدول 7.1انواع هیبریداسیون اربیتال های اتمی از تشکیل پیچیده - LA و هندسه برخی از ترکیبات پیچیده

ساختار فضایی مجتمع با نوع هیبریداسیون مدار والنس و تعداد جفت های الکترونیکی آسیب پذیر موجود در سطح انرژی ارزش آن تعیین می شود.
اثربخشی تعامل اهدا کننده گیرنده لیگاند و عامل پیچیده، و در نتیجه، قدرت رابطه بین آنها (پایداری پیچیده) توسط قطبش پذیری آنها تعیین می شود، I.E. توانایی تبدیل پوسته های الکترونیکی خود تحت نفوذ خارجی. بر این اساس، واکنشگرها به آن تقسیم می شوند "سخت"،یا dowololarizable و "نرم" -سبک وزن قابل حمل است. قطبیت اتم، مولکول یا یون بستگی به اندازه آنها و تعداد لایه های الکترونیکی دارد. کوچکتر شعاع و الکترونها در ذرات کمتر قطبی شده است. کوچکتر شعاع و الکترونهای کمتر در ذرات، بدتر از آن قطبی است.
اسیدهای سفت و سخت با اتم های الکتریکی منفی O، N، F Ligands (پایه های سفت و سخت) مجتمع های قوی (سفت و سخت) و اسید های نرم با اتم های اهدا کننده P، S و I از لیگاند هایی که دارای الکترونگامی کم و قطبش پذیری بالا، مجتمع های با دوام (نرم) هستند، تشکیل می دهند. ما در اینجا شاهد تظاهرات اصل کلی "شبیه به مانند" هستیم.
یون های سدیم، پتاسیم به علت سفتی آنها عملا مجتمع های پایدار را با biosubstrates تشکیل نمی دهند و در محیط فیزیولوژیکی به شکل Aquacomplexes هستند. یون های Ca 2 + و Mg 2 + فرم های بسیار پایدار را با پروتئین ها تشکیل می دهند و بنابراین در محیط های فیزیولوژیکی هر دو در یون و در حالت مرتبط هستند.
یون های D عناصر با مجتمع های با دوام Biozubstrats (پروتئین) تشکیل می شوند. و اسید نرم Cd، Pb، Hg بسیار سمی هستند. آنها مجتمع های با دوام را با پروتئین های حاوی گروه های Sulf-Hydrogen R-S تشکیل می دهند:
سمی سیانید یون. لیگاند نرم به طور فعالانه با D-metals در مجتمع های با بیوسوبسترات ها ارتباط برقرار می کند، فعال کردن آن.
7.5. جداسازی ترکیبات پیچیده. پایداری مجتمع ها. مجتمع های ناخوشایند و بی اثر
هنگامی که در آب ترکیبات پیچیده حل می شود، آنها معمولا به یون های داخلی و داخلی، شبیه به الکترولیت های قوی تجزیه می شوند، زیرا این یون ها به طور یونیک، به طور عمده نیروهای الکترواستاتیک مرتبط هستند. این به عنوان جداسازی اولیه ترکیبات پیچیده تخمین زده می شود.
جداسازی ثانویه ترکیب پیچیده، فروپاشی حوزه داخلی به اجزای اجزای آن است. این فرایند به وسیله نوع الکترولیت های ضعیف حاصل می شود، زیرا ذرات حوزه داخلی به طور غیر یونیک (پیوند کووالانتی) همراه هستند. جداسازی در طبیعت پله شده است:

برای مشخصه کیفی پایداری حوزه داخلی ترکیب پیچیده، ثابت ثابت استفاده می شود، که توضیحات کامل را توصیف می کند، به نام آن، نامیده می شود ثابت مجتمع عمر(kn). برای آنیون پیچیده - بیان ثابت از موقع، فرم را تشکیل می دهد:

مقدار kN کوچکتر است، پایدار تر، حوزه داخلی ترکیب پیچیده است، I.E. کمتر آن را در محلول آبی جدا می کند. به تازگی، به جای KN، مقدار ثابت پایداری (KU) ارزش ها، بازگشت KN است. ارزش Ku بیشتر، پیچیده تر است.
ثابت های پایداری امکان پیش بینی مسیر فرآیندهای تبادل لیگاند را فراهم می کنند.
در یک محلول آبی، یون فلزی به شکل Aquacomplexes وجود دارد: 2 + - Hexaakvoryzo (II)، 2 + - Tetraakvmed (II). هنگام نوشتن فرمول یون های هیدراته، مولکول های آب هماهنگ شده از پوسته هیدراته نشان نمی دهد، اما به این معنی است. تشکیل یک مجموعه بین یون فلز و در هر لیگاند ما به عنوان واکنش جایگزینی مولکول آب در حوزه هماهنگی داخلی توسط این لیگاند در نظر می گیریم.
واکنش های تبادل لیگاند به وسیله مکانیسم واکنش ها s n -typ ادامه می یابد. مثلا:
مقادیر ثابت های پایداری نشان داده شده در جدول 7.2 نشان می دهد که با توجه به فرایند پیچیده، اتصال قوی یون ها در محلول های آبی رخ می دهد، که نشان دهنده اثربخشی استفاده از این نوع واکنش برای یون های اتصال، به ویژه لیگاندهای پلییدات است.
جدول 7.2پایداری مجتمع های زیرکونیا

در مقایسه با واکنش های متابولیسم یونیک، تشکیل ترکیبات پیچیده اغلب یک فرآیند تقریبی نیست. به عنوان مثال، با تعامل آهن (III) با اسید نیتریمکتریلن اسید فسفونیک، تعادل در 4 روز نصب شده است. برای ویژگی های جنبشی مجتمع ها، مفاهیم استفاده می شود - لاغر(به سرعت واکنش پذیر) و بی اثر(به آرامی واکنش پذیر). مجتمع های لخت، در پیشنهاد شهر Taub، به طور مساوی توسط لیگاندها به مدت 1 دقیقه در دمای اتاق مبادله می شود و غلظت محلول 0.1 متر است. لازم است به وضوح مفاهیم ترمودینامیکی را تشخیص دهیم [با دوام (پایدار) / مجتمع های غیر امن (ناپایدار) و سینتیک [بی اثر و لخت].
در مجتمع های لخت، جایگزینی لیگاندها به سرعت رخ می دهد و به سرعت تعادل را ایجاد می کند. در مجتمع های بی اثر، جایگزینی لیگاندها به آرامی جریان می یابد.
بنابراین، مجتمع بی اثر 2 + در یک محیط اسیدی، ترمودینامیکی ناپایدار است: ثابت رد شده 10 -6 است، و مجتمع Labile 2- بسیار پایدار است: ثابت پایداری 10 -30 است. قابلیت تغذیه مجتمع های Taube با ساختار الکترونیکی اتم مرکزی مرتبط می شود. بی اثر مجتمع ها به طور عمده، یون ها با یک پوسته D-Untinated مشخص می شود. این نیرو شامل مجتمع CO، CR است. مجتمع های سیانید بسیاری از کاتیون ها با سطح خارجی S 2 P 6 Labils.
7.6. خواص شیمیایی مجتمع ها
فرایندهای پیچیده تقریبا بر خواص تمام ذرات تشکیل پیچیده تاثیر می گذارد. بالاتر از قدرت اوراق قرضه لیگاند و عامل پیچیده، به میزان کمتر، خواص اتم مرکزی و لیگاند ها در محلول ظاهر می شود و بیشتر به طور قابل توجهی ویژگی های پیچیده پیچیده است.
ترکیبات پیچیده نشان می دهد فعالیت های شیمیایی و بیولوژیکی به عنوان یک نتیجه از هماهنگی اشباع اتم مرکزی (Orbitals رایگان وجود دارد) و در دسترس بودن جفت های الکترونیکی رایگان لیگاند. در این مورد، این مجموعه دارای خواص الکترو فیلتر و نوکلئوفیلی به غیر از خواص اتم مرکزی و لیگاند ها است.
لازم است تا تاثیر بر فعالیت شیمیایی و بیولوژیکی ساختار پوسته هیدراته پیچیده را در نظر بگیریم. روند آموزش و پرورش
این مجتمع بر خواص اصلی اسید یک ترکیب جامع تاثیر می گذارد. شکل گیری اسیدهای پیچیده به ترتیب با افزایش نیروی اسید یا پایه همراه است. بنابراین، در شکل گیری اسیدهای پیچیده از انرژی اتصال ساده با یون های H +، اسید اسید در حال رشد است. اگر یون در حوزه بیرونی قرار گیرد، اتصال بین کاتیون پیچیده و یون هیدروکسید کره خارجی کاهش می یابد و خواص اصلی این مجموعه در حال افزایش است. به عنوان مثال، هیدروکسید مس Cu (OH) 2 یک پایه ضعیف و سخت محلول است. تحت عمل آمونیاک، آمونیاک مس (OH) 2 تشکیل شده است. تراکم شارژ 2 + نسبت به Cu 2 + کاهش می یابد، اتصال با یون های آن ضعیف شده و (OH) 2 مانند یک پایه قوی رفتار می کند. خواص اسید-پایه لیگاند های مرتبط با عامل پیچیده معمولا به شدت از خواص اساسی اسید آنها در یک کشور آزاد ظاهر می شود. به عنوان مثال، هموگلوبین (Hb) یا Oxygemoglobin (HBO 2) دارای خواص اسیدی با توجه به گروه های کربوکسیل آزاد پروتئین-گلوبین، که لیگاند NNB ↔ H + + Hb است. در عین حال، آنیون هموگلوبین به علت گروه آمینو پروتئین گلوبین، خواص اساسی را نشان می دهد و بنابراین CO 2 اکسید اسید را تشکیل می دهد تا یک کربناماموژلوبین آنیون را تشکیل دهد (NBSO 2 -): CO 2 + Hb - ↔ NBSO 2 -.
مجتمع ها خواص بازآفرینی را نشان می دهند به دلیل تغییرات Redox از تعلیم و تربیت مجتمع، درجه اکسیداسیون پایدار را تشکیل می دهند. فرایند مجتمع به میزان قابل توجهی بر ارزش های پتانسیل کاهش دهنده عناصر D تاثیر می گذارد. اگر فرم کاهش یافته از کاتیون ها یک مجتمع پایدار تر با این لیگاند را از فرم اکسید شده آن ترکیب کند، مقدار بالقوه افزایش می یابد. کاهش میزان پتانسیل زمانی رخ می دهد که یک مجتمع پایدار تر یک فرم اکسید شده را تشکیل می دهد.به عنوان مثال، تحت عمل اکسیداسیون: نیترات، نیترات، NO 2، H 2 O 2 هموگلوبین به عنوان یک نتیجه از اکسیداسیون اتم مرکزی به متیموگلوبین تبدیل می شود.
ششم اوربیتال در شکل گیری Oxymemoglobin استفاده می شود. همان مدار در شکل گیری ارتباط با مونوکسید کربن دخیل است. در نتیجه، یک مجتمع ماکروسیکلیک با آهن - کربوکسیگلوبین تشکیل شده است. این مجتمع 200 برابر پایدار تر از مجتمع آهن با اکسیژن در heme است.

شکل. 7.1تحولات شیمیایی هموگلوبین در بدن انسان. طرح از کتاب: Slyzarev v.I. اصول شیمی زنده، 2000
شکل گیری یونهای پیچیده بر فعالیت کاتالیزوری یون ها از عوامل پیچیده تاثیر می گذارد. در برخی موارد، فعالیت افزایش می یابد. این به دلیل تشکیل سیستم های ساختاری بزرگ در یک راه حل است که قادر به شرکت در ایجاد محصولات متوسط \u200b\u200bو کاهش انرژی فعال شدن واکنش است. به عنوان مثال، اگر KN 2 O 2 افزودن Cu 2+ یا NH 3، فرآیند تجزیه تسریع نیست. در حضور مجتمع 2 +، که در یک محیط قلیایی تشکیل شده است، تجزیه پراکسید هیدروژن 40 میلی ثانیه را افزایش می دهد.
بنابراین، در هموگلوبین، می توان خواص ترکیبات پیچیده را در نظر بگیریم: اسید مرکزی، مجتمع و اکسیداتیو و بازیابی.
7.7. طبقه بندی ترکیبات پیچیده
چندین سیستم طبقه بندی برای ترکیبات پیچیده وجود دارد که بر اساس اصول مختلف هستند.
1. برنامه های کاربردی یک اتصال جامع به یک کلاس خاص از ترکیبات:
اسیدهای پیچیده H 2؛
پایه های پیچیده آه؛
نمک های مجتمع K 4.
2. با ماهیت لیگاند: Akvakompleks، آمونیا، آککسید ها (به عنوان لیگاند ها، آنیون های اسید های مختلف، K 4، مجتمع های هیدروکسیل (به عنوان لیگاند ها - گروه های هیدروکسیل، K 3)؛ مجتمع هایی با لیگاندهای ماکروسیکلیک، که در آن اتم مرکزی قرار دارد .
3. در علامت شارژ مجتمع: کاتیونی - کاتیونی پیچیده در ترکیب پیچیده CL 3؛ آنیون آنیونی پیچیده در ترکیب پیچیده k؛ خنثی - اتهام این مجتمع 0. ترکیب جامع از حوزه خارجی، به عنوان مثال. این فرمول آماده سازی ضد تومور است.
4. توسط ساختار داخلی مجتمع:
الف) بسته به تعداد اتم های عامل پیچیده: تک هسته ای- مجموعه ای از ذرات پیچیده شامل یک اتم از عامل پیچیده، به عنوان مثال، CL 3؛ چند هسته ای- به عنوان بخشی از یک ذره پیچیده، چند اتم از کامپوزیت COM - مجتمع Ironoprotein:

ب) بسته به تعداد انواع لیگاندها، مجتمع ها را تشخیص می دهد: همگن (یک درجه)،حاوی یک نوع لیگاند، به عنوان مثال 2 + و ناهمگن (جامد)- دو نوع لیگاند یا بیشتر، به عنوان مثال PT (NH 3) 2 CL 2. این مجموعه شامل Ligal-Dying NH 3 و CL است. برای ترکیبات پیچیده حاوی لیگاندهای مختلف در حوزه داخلی، آن را با ایزومریسم هندسی مشخص می شود، زمانی که با ترکیب مشابهی از حوزه داخلی لیگاندها در آن، نسبت به یکدیگر متفاوت است.

ایزومرهای هندسی ترکیبات پیچیده نه تنها در خواص فیزیکی و شیمیایی، بلکه فعالیت های بیولوژیکی نیز متفاوت است. Cis-Isomer PT (NH 3) 2 CL 2 فعالیت ضد تومور را اعلام کرده و Trans-Isomer - NO؛
ب) بسته به پروتئین لیگاندهای تشکیل مجتمع های مونوریتر، گروه ها را می توان اختصاص داد:
مجتمع های تک هسته ای با لیگاندهای یکنواخت، به عنوان مثال 3+؛
مجتمع های تک هسته ای با لیگاندهای پلی اتیلن. ترکیبات پیچیده با لیگاند های پلی اتیلن تماس بگیرید ترکیبات کلات؛
د) شکل های چرخه ای و آسیکلیک ترکیبات پیچیده.
7.8. مجتمع های chelate مجتمع ها درک مطلب
ساختارهای چرخه ای که به عنوان یک نتیجه از اضافه کردن یون فلز به دو اتم اهدا کننده تشکیل شده یا بیشتر متعلق به یک مولکول از عامل تشکیل دهنده کلات نامیده می شود ترکیبات کلاتبه عنوان مثال، Glycinate مس:

در آنها، عامل مجتمع به نظر می رسد در داخل لیگاند، تحت پوشش اوراق قرضه به عنوان culbs، به طوری که آنها، با چیزهای دیگر برابر است، ثبات بالاتر از ترکیبات که حاوی چرخه نیست. پایدار ترین چرخه های متشکل از پنج یا شش لینک است.این قانون برای اولین بار توسط L.A فرموله شده است. چوان تفاوت
پایداری پیچیده کلات و پایداری آنالوگ غیر سیکل آن نامیده می شود اثر کلات
به عنوان یک عامل تشکیل دهنده ی شیمیایی، لیگاندهای پلی مدیا خدمت می کنند که شامل 2 نوع گروه بندی می شوند:
1) گروه هایی که قادر به تشکیل اوراق قرضه قطبی کووالانتی به علت واکنش های تبادل (اهدا کنندگان پروتون ها، پذیرش جفت الکترونیکی) -ch 2 Soam، -ch 2 PO (OH) 2، -Ch 2 SO 2 OH، - گروه های اسید (مراکز )
2) اهدا کنندگان جفت الکترونیکی: ≡NN،\u003e NH،\u003e C \u003d O، -S-، -OH، گروه های اصلی (مراکز) هستند.
اگر چنین لیگاند ها با حوزه هماهنگی داخلی مجتمع اشباع شوند و به طور کامل شارژ یون فلز را خنثی کنند، سپس ترکیبات نامیده می شوند intracomplexبه عنوان مثال، گلیسینت مس. هیچ حوزه خارجی در این مجموعه وجود ندارد.
یک گروه بزرگ از مواد ارگانیک حاوی مراکز پایه و اسید در مولکول نامیده می شود مجتمعاینها اسیدهای پلیپی هستند. ترکیبات Chelate که توسط ترکیبات با ترکیبات فلزی ارتباط برقرار می کنند، نامیده می شود cOMPایتن ها،به عنوان مثال، ترکیبات منیزیم با اسید اتیلندیامینتتراک اسید اسید:
در یک محلول آبی، این مجموعه در شکل آنیون وجود دارد.
این مجموعه ها و کابینت ها یک مدل ساده از ترکیبات پیچیده تر موجودات زنده هستند: اسیدهای آمینه، پلیپپتید، پروتئین، اسیدهای نوکلئیک، آنزیم ها، ویتامین ها و بسیاری از ترکیبات اندوژن دیگر.
در حال حاضر، طیف گسترده ای از کانکال های مصنوعی با گروه های کاربردی مختلف در دسترس است. فرمول های مجتمع اصلی در زیر ارائه شده است:


کامپیوترها تحت شرایط خاص می توانند جفت های الکترونیکی حاشیه ای (چندین) را فراهم کنند تا یک پیوند هماهنگی را با یک یون فلزی (S-، P- یا D-Element) تشکیل دهند. به عنوان یک نتیجه، ترکیبات ثابت از نوع Chelate با چرخه های 4، 5، 6 یا 8 عضو تشکیل شده است. این واکنش در فاصله زمانی pH گسترده می شود. بسته به PH، ماهیت عامل پیچیده، نسبت آن با لیگاند توسط کپسول های قدرت و حلالیت مختلف تشکیل شده است. شیمی درمانی مجتمع های مجتمع را می توان با معادلات بر روی نمونه ای از نمک سدیم EDTA (Na 2 H 2 Y) نشان داد که در محلول آبی محلول می شود: Na 2 H 2 Y → 2NA + + H 2 Y 2 و یون H 2 Y 2- با توجه به اکسیداسیون کاتیون فلز، با یک مجموعه پیچیده از مجتمع، اغلب یک یون فلزی (1: 1) را تعامل می کند. واکنش به صورت کمی (CR\u003e 10 9) ادامه می یابد.
کانکتون ها و کپسول ها در طیف گسترده ای از خواص آمفوتریک pH نشان می دهند، توانایی شرکت در واکنش های اکسیداسیون، پیچیدگی، ترکیبات تشکیل شده با خواص مختلف، بسته به درجه اکسیداسیون فلز، اشباع هماهنگی آن، خواص الکتروفیل و نوکلئوفیلی دارند. همه این ها توانایی اتصال به تعداد زیادی از ذرات را تعیین می کند که به تعداد کمی از واکنشگرها اجازه می دهد تا وظایف بزرگی و متنوع را حل کند.
یکی دیگر از مزایای غیر قابل انکار از کریستال ها و کپسول ها، یک مسمومیت کوچک و توانایی تبدیل ذرات سمی است.
در کم سمی یا حتی بیولوژیکی فعال. محصولات تخریب کانکون ها در بدن و بی ضرر انباشته نمی شوند. سومین ویژگی COMPRECTONATES احتمال استفاده آنها به عنوان منبع عناصر کمیاب است.
افزایش هضم پذیری ناشی از این واقعیت است که عنصر ردیابی در یک فرم فعال زیست شناختی معرفی شده و دارای نفوذ پذیری غشای بالا است.
7.9. مجتمع های فلزات فسفریک - یک شکل موثر تبدیل میکرو و کلان به یک حالت فعال بیولوژیکی و یک مدل تحقیق بیولوژیکی عناصر شیمیایی
مفهوم فعالیت بیولوژیکیطیف گسترده ای از پدیده ها را پوشش می دهد. از نقطه نظر اثرات شیمیایی تحت مواد فعال زیست شناختی (BAV)، معمول است برای درک مواد که می تواند بر روی سیستم های بیولوژیکی عمل کند، تنظیم معیشت آنها.
توانایی تفسیر به عنوان توانایی برای آشکار فعالیت های بیولوژیکی. مقررات ممکن است خود را در اثر تحریک، ظلم و ستم، توسعه اثرات خاص آشکار سازد. تظاهرات شدید فعالیت بیولوژیکی است عمل زیست محیطیهنگامی که قرار گرفتن در معرض مواد بیوسید، دومی می میرد. در غلظت های پایین تر، در اغلب موارد، بیوسیدها موجودات جامد نیستند، بلکه یک اثر تحریک کننده است.
در حال حاضر تعداد زیادی از این مواد شناخته شده است. با این وجود، در بسیاری از موارد، استفاده از مشهور BAV استفاده می شود کافی نیست، اغلب با بهره وری، دور از حداکثر، و برنامه اغلب منجر به عوارض جانبی می شود که می تواند توسط معرفی اصلاح کننده در BAV حذف شود.
ترکیبات حاوی فسفر حاوی ترکیبات با خواص مختلف، بسته به طبیعت، درجه اکسیداسیون فلز، اشباع هماهنگی، ترکیب و ساختار پوسته هیدرات. همه اینها تعدادی پوشش پیچیده NAT را تعیین می کند، توانایی منحصر به فرد آنها از عمل زیرزمینی
اثر یون مشترک و استفاده گسترده ای در پزشکی، زیست شناسی، محیط زیست و در بخش های مختلف اقتصاد ملی فراهم می کند.
هنگامی که هماهنگ کردن یون فلز از جامد، تراکم الکترونی توزیع شده است. با توجه به مشارکت جفت الکترونیکی رادیویی با تعامل گیرنده اهدا کننده، تراکم الکترونیکی لیگاند (مجتمع N) به اتم مرکزی رخ می دهد. کاهش شارژ منفی در لیگاند باعث کاهش تحریک کولمب از واکنش ها می شود. بنابراین، لیگاند هماهنگ شده برای حمله واکنش های نوکلئوفیلی قابل دسترسی است که بیش از حد تراکم الکترونیکی در مرکز واکنش دارد. جابجایی تراکم الکترون از چهره به یون فلز منجر به افزایش نسبی در بار مثبت اتم کربن می شود و بنابراین، به کاهش حمله خود با یک واکنش نوکلئوفیلی، یون هیدروکسیل، کاهش می یابد. مجتمع هیدروکسی شده در میان آنزیم هایی که فرایندهای متابولیسم را در سیستم های بیولوژیکی کاتالیز می کنند، یکی از مکان های مرکزی در مکانیزم عمل آنزیمی و سم زدایی بدن را اشغال می کند. به عنوان یک نتیجه از تعامل چند جانبه آنزیم با بستر، جهت گیری رخ می دهد، ارائه نزدیک شدن به روابط گروه های فعال در مرکز فعال و ترجمه واکنش به حالت داخل مولکولی، قبل از واکنش و تشکیل حالت انتقال آغاز شده است، که عملکرد FQM آنزیمی را تضمین می کند.تغییرات سازگاری ممکن است در مولکول های آنزیمی رخ دهد. هماهنگی شرایط اضافی برای تعامل مجدد بین یون مرکزی و لیگاند ایجاد می کند، زیرا اتصال فوری بین عامل اکسید کننده و عامل کاهش دهنده، که تضمین انتقال الکترون ها را تضمین می کند، ایجاد می شود. برای مجموعه ای از فلزات انتقال، FQM را می توان با انتقال الکترون-نوع L-M، M-L، M-L-M مشخص کرد، که در آن اوربیتال هر دو فلز (M) و لیگاندها (L) درگیر هستند، که به ترتیب با اوراق قرضه اهدا کننده گیرنده مرتبط هستند. مجتمع ها می توانند به عنوان یک پل که برای آن الکترونهای مجتمع های چند هسته ای بین اتم های مرکزی یک یا چند عنصر مختلف در درجه های مختلف اکسیداسیون استفاده می شود، استفاده می شود (الکترونیک انتقال الکترون و پروتون ها).این مجتمع ها ویژگی های توانبخشی مجتمع های فلزات را تعیین می کنند که به آنها اجازه می دهد تا خواص آنتی اکسیدان بالا، سازگاری، توابع هوموتاتیک را نشان دهند.
بنابراین، این مجتمع ها عناصر ردی را به یک فرم فعال بیولوژیکی تبدیل می کنند که برای بدن موجود است. آنها پایدار هستند
ذرات اشباع شده بیشتر هماهنگ شده، قادر به نابودی زیستی، و در نتیجه، فرم های کم سمی. این مجموعه ها در نقض میکروارگانیسم هومیوستا فراتر از ارگانیسم مطلوب هستند. یون های انتقال در فرم Complactonate در بدن به عنوان عامل تعیین حساسیت بالا سلول ها به میکرولیوم ها با مشارکت آنها در ایجاد گرادیان غلظت بالا، پتانسیل غشایی. مولفه های انتقال فلزات FQM دارای خواص بیولوژیکی هستند.
حضور مراکز اسید و اصلی در ترکیب PCM خواص آمفتری و مشارکت آنها در حفظ تعادل پایه اسید (ایزوگید) را فراهم می کند.
با افزایش تعداد گروه های فسفون در ترکیب مجتمع، ترکیب و شرایط برای تشکیل مجتمع های محلول و ضعیف محلول تغییر می کند. افزایش تعداد گروه های فسفون، تشکیل مجتمع های محلول کم را در یک فاصله pH گسترده تر می کند، منطقه ای را در ناحیه اسیدی تغییر می دهد. تجزیه مجتمع ها در pH بیش از 9 اتفاق می افتد.
مطالعه فرایندهای پیچیده با فرایندهای پخت و پز امکان ایجاد روش های سنتز بیولوژیک را فراهم می آورد:
محرک های رشد فعالیت طولانی مدت در فرم کلوئیدی-شیمیایی، هموگلوبین های چند گانه تیتانیوم و آهن هستند؛
محرک های رشد در یک فرم محلول در آب. این ترکیبات تیتانیوم غیر ترکیبی مبتنی بر کریستون ها و لیگاند معدنی است؛
مهار کننده های رشد - مجتمع های حاوی فسفر از عناصر S.
اثر بیولوژیکی داروهای سنتز شده بر رشد و توسعه در یک آزمایش مزمن بر روی گیاهان، حیوانات و یک فرد مورد مطالعه قرار گرفته است.
بیگانه سازی- این یک جهت علمی جدید است که اجازه می دهد تا جهت و شدت فرآیندهای بیوشیمیایی را تنظیم کنید، که می تواند به طور گسترده ای در پزشکی، دامداری و تولید محصول استفاده شود. این امر با توسعه راه هایی برای بازگرداندن عملکرد فیزیولوژیکی بدن به منظور جلوگیری و درمان بیماری ها و بیماری های سنی همراه است. مجتمع ها و ترکیبات پیچیده بر اساس آنها می تواند به امیدوار کننده ترکیبات فعال زیست شناختی نسبت داده شود. مطالعه عمل بیولوژیکی آنها در آزمایش مزمن نشان داد که شیمی به دست پزشکان،
پرورش دهندگان دامداری، کشاورزان و زیست شناسان عامل جدیدی هستند که اجازه می دهد تا به طور فعال بر سلول زنده تأثیر بگذارد، شرایط قدرت، رشد و توسعه موجودات زنده را تنظیم کند.
بررسی سمیت کیتون های مورد استفاده و کپسول ها، عدم وجود کامل اثرات داروها بر ارگان های تشکیل خون، فشار خون، تحریک پذیری، میزان تنفس را نشان داد: هیچ تغییری در عملکرد کبد مشاهده نشد، اثر سم شناسی بر مورفولوژی بافت ها و اندام ها نشان ندادند. OEDF نمک پتاسیم سمیت در دوز، 5-10 برابر بیشتر از درمانی (10-20 میلی گرم بر کیلوگرم) در طول مطالعه برای 181 روز ندارد. در نتیجه، ترکیبات متعلق به ترکیبات کم سمی هستند. آنها به عنوان داروهای دارویی برای مبارزه با بیماری های ویروسی مورد استفاده قرار می گیرند، مسمومیت با فلزات سنگین و عناصر رادیواکتیو، نقض فلزات کلسیم، در بیماری های اندمیک و نقض تعادل عنصر ردیابی در بدن است. مجتمع های حاوی فسفر و دیجیتال به فتوولیسم نمی رسند.
آلودگی پیشرونده محیط زیست با فلزات سنگین - محصولات فعالیت اقتصادی انسانی یک عامل زیست محیطی همیشه موثر است. آنها می توانند در بدن انباشته شوند. بیش از حد و ضعف آنها باعث مسمومیت بدن می شود.
مجتمع های فلزی، حفظ در بدن اثر شیمیایی بر لیگاند (مجتمع) و ضروری برای حفظ هوموستاز فلزی است. فلزات سنگین گنجانده شده به میزان مشخصی در بدن خنثی می شوند و توانایی جذب کم باعث جلوگیری از انتقال فلزات در امتداد زنجیرهای تروفیک می شود، به عنوان یک نتیجه، منجر به یک "سیستم بیومین" معانی اثر سمی آنها می شود که به ویژه درست برای منطقه اورال. به عنوان مثال، یون سرب آزاد به سموم تیئول اشاره می کند و یک مجموعه سرب با دوام با اتیلنیمینتراسیت اسید کم اکسیدوکسیک است. بنابراین، سم زدایی گیاهان و حیوانات، استفاده از کیتون های فلزات است. این بر اساس دو اصل ترمودینامیکی است: توانایی آنها برای تشکیل اوراق قرضه قوی با ذرات سمی، تبدیل آنها به اتصالات ضعیف یا مقاوم در محلول آبی؛ ناتوانی آنها برای نابود کردن بیوماپل های درونی. در این رابطه، ما آن را یک جهت مهم برای مبارزه با زیست محیطی و تولید محصولات سازگار با محیط زیست - این درمان پیچیده گیاهان و حیوانات در نظر می گیریم.
بررسي تأثير درمان گياهان گياهان فلزات گوناگون با تکنولوژي کشت كاري پيشنهادي انجام شده است.
سیب زمینی در ترکیب میکروارگانیسم سیب زمینی. نمونه های نظرسنجی شامل 105-116 میلی گرم بر کیلوگرم آهن، 16-20 میلی گرم بر کیلوگرم منگنز، 13-18 میلی گرم بر کیلوگرم مس و 11-15 میلی گرم بر کیلوگرم روی بود. نسبت و محتوای عناصر ردیابی برای بافت های گیاهی معمول است. غده ها رشد کرده اند و بدون استفاده از کیتون های فلزات تقریبا همان ترکیب عنصری هستند. استفاده از Shela-COM شرایط را برای انباشت فلزات سنگین در غده ها ایجاد نمی کند. این مجموعه ها به میزان کمتری نسبت به یون های فلزی توسط خاک جذب می شوند، که مقاوم در برابر اثرات میکروبیولوژیک آن است که به مدت طولانی در راه حل خاک نگهداری می شود. اثر 3-4 سال. آنها به خوبی با آفت کش های مختلف ترکیب شده اند. فلز در مجتمع دارای سمیت پایین است. کپسول های حاوی فسفر حاوی غشای مخاطی چشم ها تحریک نمی شوند و به پوست آسیب نمی رسانند. خواص حساس سازی شناسایی نشده است، خواص تجمعی کانکال های تیتانیوم بیان نشده است، و برخی از آنها بسیار ضعیف بیان شده اند. ضریب تجمعی 0.9-3.0 است که نشان دهنده یک خطر بالقوه بالقوه مسمومیت مزمن با داروها است.
پایه مجتمع های حاوی فسفر، پیوند فسفور (C-P) است که در سیستم های بیولوژیکی یافت می شود. این بخشی از رادپیدها فسفو، فسفونوگلیکان ها و فسفوپروپروتئین های غشای سلولی است. لیپیدهای حاوی ترکیبات آمینو فسفونیک مقاوم به هیدرولیز آنزیمی هستند، اطمینان از ثبات، و بنابراین، عملکرد طبیعی غشاهای سلول بیرونی. آنالوگ های مصنوعی پیرو فسفات ها - فون های دیفرانسیل (R-C-P-P) یا (R-C-C-P) در دوزهای بزرگ، تبادل کلسیم را نقض می کنند و در آن به طور کوچک آن را عادی می کنند. دیفسفونات ها در هیپرلیپمی موثر هستند و امیدوار کننده از موقعیت های فارماکولوژی هستند.
diffosphosphonates، شامل پین های P-C-P، عناصر ساختاری بیوسيستم ها هستند. آنها از لحاظ زیست شناختی موثر هستند و آنالوگ های پیرو فسفات هستند. نشان داده شده است که دی فسفونات ها ابزار موثر درمان بیماری های مختلف هستند. دی فسفونات ها مهار کننده های فعال کانی سازی و جذب استخوان هستند. این مجتمع ها عناصر ردی را به شکل بیولوژیکی فعال تبدیل می کنند که برای بدن موجود است، هماهنگی پایدار تر و ذرات اشباع شده را تشکیل می دهند، قادر به نابودی زیستی، و در نتیجه، فرم های کم سمی نیستند. آنها حساسیت بالا سلول ها را به عناصر ردیابی می رسانند، که در شکل گیری گرادیان غلظت بالا شرکت می کنند. قادر به شرکت در تشکیل ترکیبات چند هسته ای از تیتانیوم هتروانیوم
نوع - الکترونها و پروتون های انتقال مجتمع های انتقال، شرکت در تولید بیولوژیک فرآیندهای متابولیک، مقاومت ارگانیسم، توانایی تشکیل اتصالات با ذرات سمی، تبدیل آنها به مجتمع های غیر قابل حل یا محلول، پایدار و غیر مخرب، پایدار و غیر مخرب. بنابراین، استفاده از آنها برای سم زدایی، از بین بردن از بدن، به دست آوردن محصولات سازگار با محیط زیست (پخت و پز)، و همچنین در صنعت برای بازسازی و استفاده از زباله های صنعتی اسیدهای معدنی و نمک های فلزات انتقال بسیار امیدوار کننده است.
7.10. تبادل لیگاند و تبادل فلزی
تعادل chelatotherapy
اگر لیگاندهای متعددی با یک یون فلزی یا چند یونهای فلزی با یک لیگاند وجود داشته باشند که قادر به تشکیل ترکیبات پیچیده هستند، فرایندهای رقابتی مشاهده می شود: در اولین مورد، تعادل تبادل لیگاند رقابت بین لیگاندهای یون های فلزی، در مورد دوم، تعادل مبادله فلزی است رقابت بین یون ها است. فلز برای لیگاند. غلبه بر فرآیند تشکیل جامد جامد خواهد بود. به عنوان مثال، در محلول، یون ها وجود دارد: منیزیم، روی، آهن (III)، مس، کروم (II)، آهن (II) و منگنز (II). هنگامی که به این محلول مقدار کمی از مقدار کمی از اتیل اتیلنیمین ژنیته اسید (EDTA) معرفی شد، رقابت بین یونهای فلزی و اتصال به مجتمع آهن (III) رخ می دهد، زیرا این مجموعه با دوام ترین از EDTA را تشکیل می دهد.
بدن به طور مداوم در تعامل بیومتر (MB) و Biolygandov (LB)، آموزش و تخریب زیست سازهای حیاتی (MBLB) رخ می دهد:
در بدن انسان، حیوانات و گیاهان مکانیسم های مختلفی برای حفاظت و حمایت از این تعادل از Xenobiotics های مختلف (مواد بیگانه) وجود دارد، از جمله یونهای فلزات سنگین. یون های فلزات سنگین که با این مجموعه ارتباط ندارند، و هیدروکسیکوپلز آنها ذرات سمی (MT) هستند. در این موارد، همراه با داربست های طبیعی، یک تعادل جدید ممکن است رخ دهد، با تشکیل مجتمع های خارجی با دوام های حاوی فلزات سموم (MTLB) یا لیگاندهای سمی (MBLT) که انجام نمی دهند
توابع بیولوژیکی مورد نیاز اگر به بدن ذرات سمی خارجی وارد شوید، تعادل ترکیبی بوجود می آید و به عنوان یک نتیجه، صلاحیت فرآیندها. غالب این فرآیند است که منجر به تشکیل اتصال جامد جامد می شود:

اختلالات هوموستاز فلزی نامنظم باعث نقض فرآیند متابولیسم می شود، فعالیت آنزیم ها را مهار می کند، متابولیت های مهم مانند ATP، غشای سلولی را از بین می برد، شیب غلظت در سلول ها را مختل می کند. بنابراین، سیستم های حفاظتی مصنوعی ایجاد می شوند. محل مناسب در این روش توسط Chelate Therapy (پیچیده و درمان) اشغال شده است.
Chelatotherapy حذف ذرات سمی از بدن است، بر اساس کالبد شکافی از عناصر S. آماده سازی مورد استفاده برای از بین بردن ذرات سمی موجود در بدن، سم زدایی نامیده می شود(ال جی). ترکیب ذرات سمی از مجتمع های فلزات فلزات (LG) یون های سمی فلزی (MT) را به فرم های مرتبط غیر سمی (MTLG) تبدیل می کند که مناسب برای عایق و نفوذ از طریق غشاء، حمل و نقل و حذف از بدن است. آنها در بدن یک اثر کلات را به عنوان یک لیگاند (پیچیده) و یون فلز حفظ می کنند. آن را فراهم می کند هوموستاز فلزی نامناسب بدن. بنابراین، استفاده از کریسمس در پزشکی، دامداری، تولید محصول، سم زدایی بدن را تضمین می کند.
اصول اصلی ترمودینامیکی درمانی Chelate را می توان در دو موقعیت فرموله کرد.
I. سم زدایی (LG) باید به طور موثر اتصال یون های سمی (MT، LT)، ترکیبات تازه تشکیل شده (MTLG) باید قوی تر از آنچه که در بدن وجود داشت، قوی تر باشد:
دوم سم زدایی نباید ترکیبات جامع حیاتی (MBLB) را نابود کند؛ ترکیباتی که می توانند در اثر متقابل آنزیم آلودگی و بیومکتال (MBLG) تشکیل شوند، باید نسبت به موجود در بدن کمتر با دوام باشند:
7.11. استفاده از contribons و confactons در پزشکی
مولکول های کلاسیک عملا شکسته یا هر گونه تغییر در یک محیط زیست بیولوژیکی نیست، که ویژگی های مهم داروسازی آنهاست. این مجتمع ها در لیپیدها حل نشده اند و به خوبی محلول در آب هستند، به طوری که آنها از طریق غشاهای سلولی نفوذ یا نفوذ نمی کنند و بنابراین: 1) با روده تولید نمی شوند؛ 2) جذب عوامل com-sharpulating تنها در تزریق آنها رخ می دهد (تنها پنی سیلین داخلی گرفته می شود)؛ 3) در مجتمع های بدن به وسیله مزیت در فضای خارج سلولی گردش می کنند؛ 4) حذف بدن عمدتا از طریق کلیه ها انجام می شود. این روند به سرعت رخ می دهد.
مواد که اثرات اثرات سموم بر روی ساختارهای بیولوژیکی را از بین می برند و از طریق واکنش های شیمیایی به دست می آید پادزهر
یکی از اولین پادزهر، که در Chelatotherapy اعمال شد، ضد روانکاری بریتانیا (توپ) است. Unitiol در حال حاضر استفاده می شود:
این دارو به طور موثر آرسنیک، جیوه، کروم و بیسموت را از بدن نشان می دهد. به طور گسترده ای مورد استفاده در مسمومیت روی، کادمیوم، مجتمع های سرب و جیوه و مجتمع های جیوه. استفاده از آنها بر اساس تشکیل مجتمع های با دوام تر با یونهای فلزی نسبت به مجتمع های یون های مشابه با گروه های حاوی گوگرد پروتئین، اسیدهای آمینه و کربوهیدرات ها است. آماده سازی مبتنی بر EDTA برای حذف سرب استفاده می شود. مقدمه ای بر بدن در دوزهای بزرگ مواد مخدر خطرناک است، زیرا آنها یون های کلسیم را متصل می کنند، که منجر به نقض بسیاری از توابع می شود. بنابراین، استفاده کنید تیتاسین(Sana 2 EDTA)، که برای حذف سرب، کادمیوم، جیوه، یتیم، سرییم و سایر فلزات نادر و کبالت استفاده می شود.

از زمان استفاده از اولین استفاده درمانی تتاسین در سال 1952، این دارو به طور گسترده ای در کلینیک بیماری های شغلی مورد استفاده قرار گرفت و همچنان یک پادزهر ضروری باقی می ماند. مکانیسم عمل تتاسین بسیار جالب است. به علت تشکیل پیوند های با دوام با اکسیژن و EDTA، یونی-سموم، یون های کلسیم هماهنگ شده از تتااسین را جابجا می کنند. یون کلسیم، به نوبه خود، دو یونهای سادیوم باقی مانده را جابجا می کند:

ThetaCine به شکل 5-10٪ راه حل به بدن معرفی شده است، اساس آن Saline است. بنابراین، پس از 1.5 ساعت پس از تزریق داخل صفاقی، 15٪ تجویز دوز تتااسین در بدن باقی می ماند، پس از 6 ساعت - 3٪، و پس از 2 روز - تنها 0.5٪. دارو به طور موثر و به سرعت، هنگام استفاده از روش استنشاق تجویز تتااسین. این به سرعت جذب می شود و برای مدت طولانی گردش می کند. علاوه بر این، تکتسین هنگام محافظت در برابر گانگرن گاز استفاده می شود. این مانع از یون های روی و کبالت، که فعال کننده آنزیم لسیتیناز است که گانگرن گاز توکسین است.
اتصال تتسین سمی به یک مجتمع کلات کوچک و با دوام تر، که از بین نمی رود و به راحتی از طریق کلیه ها دفع می شود، آن را از بین می برد، آن را دفع ادرار و تغذیه معدنی متعادل فراهم می کند. نزدیک به ساختار و ترکیب برای
پاراتام Edta یک نمک سدیم کلسیم از اسید دی اتیلن-پنتاکوس (SANA 3 DTP) است - پنتاتینو نمک سدیم پودر فسفونیک اسید دی اتیلن (Na 6 DTPF) - trimph Qing.پنتازین به طور عمده در مسمومیت با ترکیبات آهن، کادمیوم و سرب، و همچنین حذف رادیونوکلئید (تکنسیوم، پلوتونیوم، اورانیوم) استفاده می شود.

نمک سدیم اتیلندیامینیدیزوپروپیل فسفونیک اسید (SANA 2 EDTF) پر زحمتبا موفقیت برای از بین بردن جیوه، سرب، بریل، منگنز، actinoids و سایر فلزات از بدن استفاده می شود. مجتمع های کامل برای حذف برخی از آنیون های سمی بسیار موثر هستند. به عنوان مثال، کبالت (II) اتیلن Diametetracetate، تشکیل یک ترکیب مخلوط لیگاند با CN، می تواند به عنوان یک پادزهر در طول مسمومیت سیانید توصیه می شود. اصل مشابهی، روش های حذف مواد آلی سمی را شامل می شود، از جمله آفت کش ها حاوی گروه های کاربردی با اتم های اهدا کننده قادر به تعامل با فلز Complexonate.
آماده سازی موثر است سست کننده(اسید dimercastric، dimercaptosuccinic acid، hemet). این کاملا تقریبا تمام سموم (Hg، As، Pb، Cd) را متصل می کند، اما از بدن یونهای عناصر بیوژنیک (Cu، Fe، Zn، CO) حاصل می شود، بنابراین تقریبا هیچ کاربردی ندارد.
کاندوم های حاوی فسفر مهار کننده های قدرتمند تشکیل کریستال فسفات ها و اگزالات کلسیم هستند. به عنوان یک داروی ضد عفونی کننده در درمان اورولیثیها، Xidihon پیشنهاد شده است - Caliyevo سدیم سدیم OEDF. دی اکسید کربن، علاوه بر این، در حداقل دوز، افزایش کلسیم را به بافت استخوان، جلوگیری از خروجی پاتولوژیک از استخوان ها افزایش می دهد. OEDF و سایر دیفسفونات ها از انواع مختلف پوکی استخوان جلوگیری می کنند، از جمله استئولوژیستروزی کلیوی، دوره ای
تخریب، همچنین تخریب استخوان های پیوند شده در حیوانات. اثر ضد دریایی EDF نیز شرح داده شده است.
در ایالات متحده، تعدادی از دی فونسفونات ها، به ویژه EDF، به عنوان آماده سازی دارویی برای درمان انسان و حیوانات مبتلا به سرطان استخوان متاستاز پیشنهاد شد. تنظیم نفوذپذیری غشا، دی فسفونات ها به حمل و نقل داروهای ضد تومور به سلول کمک می کنند و از این رو درمان موثر بیماری های مختلف انکولوژیکی.
یکی از مشکلات واقعی پزشکی مدرن، وظیفه تشخیص اکسپرس بیماری های مختلف است. در این جنبه، منافع بدون شک یک کلاس جدید از داروهای حاوی کاتیون هایی است که قادر به انجام توابع پروب - رادیواکتیو مغناطیسی و تگ های فلورسنت هستند. رادیوایزوتا از برخی فلزات به عنوان اجزای اصلی آماده سازی رادیوگرافی استفاده می شود. کالبد شکافی از این ایزوتوپ های مجتمع ها اجازه می دهد تا امکان پذیرش سم شناسی خود را برای بدن افزایش دهد، حمل و نقل خود را تسهیل می کند و اطمینان حاصل از انتخاب غلظت در بدن خاصی در محدودیت های خاص را تضمین می کند.
مثالهای فوق تمام اشکال مختلف استفاده از کپسول های پزشکی را از بین نمی برد. بنابراین، نمک Diekal از منیزیم اتیلنمینامنتاتیت برای تنظیم محتوای مایع در بافت ها در طی آسیب شناسی استفاده می شود. EDTA در ترکیب تعلیق های ضد انعقادی مورد استفاده در جداسازی پلاسمای خون، به عنوان یک تثبیت کننده تریفسفات آدنوزین در تعیین گلوکز خون، هنگام روشن شدن و ذخیره لنزهای تماسی استفاده می شود. دیفسفونات ها به طور گسترده ای در درمان بیماری های روماتوئید مورد استفاده قرار می گیرند. آنها به طور خاص به عنوان عوامل ضد دارویی در ترکیب با عوامل ضد التهابی موثر هستند.
7.12. مجتمع های ترکیبات ماکروسیکلیک
در میان ترکیبات پیچیده طبیعی، Macrocomplexes بر اساس پلیپپتید های چرخه ای حاوی حفره های داخلی از اندازه های خاص اشغال شده است، که در آن چند گروه حاوی اکسیژن وجود دارد که می تواند کاتالیز های آن را متصل کند، از جمله سدیم و پتاسیم، ابعاد آن مربوط به اندازه است از حفره. چنین مواد در حالی که در زیست شناسی

شکل. 7.2.مجتمع Valinomycin با یون K +
مواد، اطمینان از حمل و نقل یون ها از طریق غشاها و به همین ترتیب نامیده می شود یونپورهابه عنوان مثال، roliniumicin یون پتاسیم را از طریق غشا حمل می کند (شکل 7.2).
با کمک یک پلیپپتید دیگر - gramicidine a.کاتیون های سدیم توسط مکانیسم رله حمل می شوند. این پلیپپتید به "لوله" تبدیل می شود، سطح داخلی آن توسط گروه های حاوی اکسیژن اغراق می شود. در نتیجه، معلوم می شود
یک کانال هیدروفیلی بسیار طولانی با یک بخش متقابل خاص مربوط به اندازه یون سدیم است. یون سدیم، وارد کانال هیدروفیلی از یک طرف، از یک به گروه های اکسیژن دیگر، مانند رله در کانال هدایت یونی منتقل می شود.
بنابراین، مولکول پلیپپتید چرخه ای دارای یک حفره داخل مولکولی است که می تواند یک بستر بستر، هندسه بر روی اصل کلیدی و قفل وارد کند. حفره چنین گیرنده های داخلی توسط مراکز فعال (Endorecepto-Rami) محافظت می شود. بسته به ماهیت یون فلز، تعامل غیر ویروسی ممکن است رخ دهد (الکترواستاتیک، تشکیل پیوند هیدروژن، نیروهای ون د ولز) با فلزات قلیایی و کووالانتی با فلزات قلیایی زمین. در نتیجه، آنها شکل می گیرند supramolecu- همکاران پیچیده متشکل از دو ذره یا بیشتر توسط نیروهای بین مولکولی برگزار می شود.
شایع ترین در بیابان های ماکروسیت های tetradentate، پورفینها و corrinoids نزدیک به آنها هستند.یک چرخه جغرافیایی طرح ریزی می تواند در فرم زیر نشان داده شود (شکل 7.3)، جایی که قوس ها به معنی همان نوع زنجیره کربن هستند که اتم های نیتروژن اهدا کننده را به یک چرخه بسته متصل می کنند؛ R 1، R 2، R 3، P 4-radicals هیدروژن؛ M N + - یون فلز: در chlorophyll یون Mg 2+، در hemoglobin یون Fe 2+، در hemocianin یون Cu 2+، در ویتامین B 12 (kobalamin) یون از 3+.
اتم های نیتروژن اهدا کننده در گوشه های مربع قرار دارند (نشان داده شده توسط خط نقطه نقطه). آنها در فضا به شدت هماهنگ شده اند. از این رو
porphyrins و Corrinoids تشکیل مجتمع های جامد با کاتیون عناصر مختلف و حتی فلزات قلیایی زمین. اساسا این صرف نظر از دندانپزشکی لیگاند، پیوند شیمیایی و ساختار مجتمع توسط اتم های اهدا کننده تعیین می شود.به عنوان مثال، مجتمع های مس با NH 3، اتیلندیامین و پور فیرین دارای ساختار مربع مشابه و پیکربندی الکترونیکی مشابه هستند. اما لیگاندهای پلی اتیلن با یونهای فلزی بسیار قوی تر از لیگاند های تک سلولی هستند

شکل. 7.3.Macrocycle Tetradentate
با همان اتم های اهدا کننده. قدرت مجتمع های اتیلندیامین توسط 8 تا 10 سفارش بیشتر از قدرت فلزات مشابه با آمونیاک است.
مجتمع های بیولوژیک یون های فلزی با پروتئین ها نامیده می شوند bioclathers -مجتمع های یون های فلزی با ترکیبات ماکروسیکلیک (شکل 7.4).

شکل. 7.4یک نمایش اساسی از ساختار زیستی زیستی از اندازه های خاصی از مجتمع های پروتئینی با یونهای D-Elements. انواع تعاملات یک مولکول پروتئینی. M N + - مرکز فعال یون فلز
در داخل bioclaster حفره وجود دارد. این شامل فلز است، که با اتم های اهدا کننده گروه های اتصال ارتباط برقرار می کند: این، SH -، COO -، -NH 2، پروتئین ها، اسیدهای آمینه است. معروف ترین مزارع فلزی
تغییرات (Carboangeerase، Xanthine Oxidase، Cytochrome)، زیست محیطی هستند که حفره هایی که مراکز آنزیم حاوی Zn، Mo، Fe را تشکیل می دهند، تشکیل می دهند.
7.13. مجتمع های چند هسته ای
مجتمع های heterovalent و heteroanore
مجتمع هایی که شامل چندین اتم مرکزی یک یا چند عنصر مختلف هستند چند هسته ایاحتمال تشکیل مجتمع های چند هسته ای با توانایی برخی از لیگاند ها به دو یا سه یونهای فلزات متصل می شود. چنین لیگاند ها نامیده می شوند پل کردنبه ترتیب پلگمرک ها نامیده می شوند. ذهن ها نیز ممکن است و پل های مناتومیک، به عنوان مثال:

آنها از جفت های ضروری الکترونیکی متعلق به یک اتم استفاده می کنند. نقش پل ها می توانند انجام دهند لیگاندهای چند اتمی.در چنین پل ها، جفت های الکترونیکی مخلوط متعلق به اتم های مختلف استفاده می شود. لیگاند پلی اتمی.

A.A. Greenberg و F.M. فیلیلین ها ترکیبات بریده کننده ترکیب را مورد بررسی قرار دادند که در آن لیگاند ترکیبات پیچیده ای از همان فلز را متصل می کند، اما در درجه های مختلف اکسیداسیون. تاوب آنها را فرا خواند مجتمع های انتقال الکتروناین واکنش انتقال الکترون را بین اتم های مرکزی فلزات مختلف بررسی کرد. مطالعات سیستماتیک از سینتیک و مکانیسم واکنش های بازدارنده منجر به نتیجه گیری می شود که انتقال یک الکترون بین دو مجتمع از
این از طریق پل لیگاند تشکیل شده است. تبادل الکترون بین 2 + و 2 + از طریق تشکیل مجتمع پل میانبر رخ می دهد (شکل 7.5). انتقال الکترون از طریق لیگاند پل کلرید رخ می دهد و با تشکیل مجتمع های 2 + پایان می یابد؛ 2 +

شکل. 7.5.انتقال الکترون در یک مجموعه چند هسته ای متوسط
طیف گسترده ای از مجتمع های پلیدیدی از طریق استفاده از لیگاندهای آلی حاوی چندین گروه اهدا کننده به دست آمد. شرایط تشکیل آنها محل گروه های اهدا کننده در یک لیگاند است که اجازه نمی دهد که چرخه های کلات را ببندید. مواردی وجود ندارد که لیگاند توانایی بستن چرخه چلت را داشته باشد و در عین حال به عنوان یک پل متعلق به عمل عمل کند.
شروع کنونی انتقال الکترون، فلزات انتقال است که چندین درجه اکسیداسیون پایدار را نشان می دهد. این به تیتانیوم، آهن و یون های مس می دهد. خواص کامل حامل های الکترونی. ترکیبی از گزینه های تشکیل مجتمع های HETERO-TANDY (GVK) و هتروونیکور (GIK) بر اساس TI و FE در شکل نشان داده شده است. 7.6.
واکنش

واکنش (1) نامیده می شود واکنش متقابلدر واکنش های متابولیک، واسطه ها مجتمع های ناهموار خواهند بود. تمام مجتمع های تئوری های احتمالی واقعا در محلول در شرایط خاصی تشکیل شده اند که توسط فیزیکی و شیمیایی مختلف اثبات شده است

شکل. 7.6.تشکیل مجتمع های ناهموار مجتمع های heteroanore حاوی Ti و Fe
مواد و روش ها. برای انجام انتقال الکترون ها، واکنشگرها باید در انرژی های دولت باشند. این الزام به عنوان اصل فرانک کاندون نامیده می شود. انتقال الکترون می تواند بین اتم های یک عنصر انتقال در درجه های مختلف اکسیداسیون GVK یا عناصر مختلف گایاک، ماهیت متالوکن، که متفاوت است، رخ دهد. این ترکیبات را می توان به عنوان مجتمع انتقال الکترون ها تعریف کرد. آنها حامل های مناسب الکترون ها و پروتون ها در سیستم های بیولوژیکی هستند. ضمیمه و بازگشت الکترون باعث می شود که تنها به پیکربندی الکترونیکی فلز، بدون تغییر ساختار جزء آلی پیچیده تغییر کند.تمام این عناصر دارای چندین درجه اکسیداسیون پایدار (Ti +3 و +4؛ Fe +2 و +3؛ Cu +1 و +2) هستند. به نظر ما، این سیستم ها توسط طبیعت ارائه می شود، نقش منحصر به فردی از اطمینان از برگشت پذیری فرایندهای بیوشیمیایی با حداقل هزینه های انرژی ارائه می شود. واکنش برگشت پذیر شامل واکنش هایی است که دارای ثابت های ترمودینامیکی و ترمو شیمیایی از 10 تا 3 تا 10 3 و با مقدار کمی ΔG O و o o.فرآیندهای در این شرایط، مواد اولیه و محصولات واکنش می تواند در غلظت های متناسب باشد. هنگامی که آنها در برخی از محدوده تغییر می کنند، آسان است برای رسیدن به معکوس شدن روند، بنابراین، در سیستم های بیولوژیکی، بسیاری از فرآیندها نوسان (موج) است. سیستم های Redox که دارای جفت های بالا هستند، با طیف گسترده ای از پتانسیل ها همپوشانی دارند، که به آنها اجازه می دهد تا به تعاملات وارد شوند، همراه با تغییرات متوسط \u200b\u200bΔ g O.و °, با بسیاری از بسترها.
احتمال تشکیل GVK و GIK به طور قابل توجهی افزایش می یابد زمانی که راه حل حاوی لیگاندهای بالقوه متعادل است، I.E. مولکول ها یا یون ها (اسیدهای آمینه، اسید هیدروکسیک، کریستال ها و غیره)، قادر به اتصال دو مرکز متالو در یک بار هستند. احتمال حذف یک الکترون در GVK موجب کاهش کل انرژی مجتمع می شود.
مجموعه ای واقع گرایانه از گزینه های ممکن برای تشکیل GVK و GIK، که در آن ماهیت مراکز فلزی متفاوت است، قابل مشاهده در شکل. 7.6. شرح مفصلی از تشکیل GVK و GAIK و نقش آنها در سیستم های بیوشیمیایی در آثار A.N. Glebova (1997). زوج های Redox باید به صورت ساختاری به یکدیگر تنظیم شوند، سپس انتقال امکان پذیر می شود. انتخاب اجزای راه حل، شما می توانید فاصله ای را که از آن الکترون از عامل کاهش دهنده به اکسید کننده منتقل می شود، افزایش دهید. با حرکت سازگار با ذرات، انتقال الکترون می تواند در فاصله های طولانی در طول مکانیسم موج رخ دهد. به عنوان یک "راهرو" می تواند یک زنجیره پروتئین هیدراته و دیگران باشد. احتمال انتقال الکترون با فاصله تا 100A. طول "راهرو" را می توان با افزودنی ها (یون های فلزی قلیایی، الکترولیت های پس زمینه) افزایش داد. این فرصت های بزرگی را در زمینه مدیریت ترکیب و خواص GVK و GAIK باز می کند. در راه حل ها، آنها نقش نوع "جعبه سیاه" را با الکترونها و پروتون ها بازی می کنند. بسته به شرایط، می تواند آنها را به اجزای دیگر بدهد یا "سهام" آن را دوباره پر کند. برگشت پذیری واکنش ها با مشارکت آنها اجازه می دهد تا چندین بار برای شرکت در فرایندهای چرخه ای شرکت کنند. الکترون ها از یک مرکز فلز به دیگری می روند، بین آنها نوسان می کنند. مولکول پیچیده باقی می ماند نامتقارن است و می تواند در فرایندهای اکسیداتیو و توانبخشی شرکت کند. GVK و GYAK به طور فعال در فرایندهای ارتعاشی در محیط های بیولوژیکی دخیل هستند. این نوع واکنش واکنش نوسانات نامیده می شود.آنها در کاتالیزوری آنزیمی، سنتز پروتئین ها و سایر فرآیندهای بیوشیمیایی مرتبط با پدیده های بیولوژیکی یافت می شوند. این شامل فرایندهای دوره ای متابولیسم سلولی، امواج فعالیت در بافت قلب، در بافت مغزی و فرآیندهای رخ می دهد که در سطح سیستم های محیطی رخ می دهد. یک گام مهم متابولیسم، شکاف هیدروژن از مواد مغذی است. اتم های هیدروژن به حالت یونی تبدیل می شوند و الکترونها جدا از آنها زنجیره تنفسی را وارد می کنند و انرژی خود را به شکل گیری ATP می دهند. همانطور که ما نصب کرده ایم، مجتمع های تیتانیوم حامل های فعال نیستند نه تنها الکترون، بلکه همچنین پروتون ها. توانایی یون های تیتانیوم برای تحقق نقش آن در مرکز فعال آنزیم های نوع کاتالاز، پراکسیداز و سیتوکروموز با توانایی بالایی آن در پیچیدگی، تشکیل یک هندسه یون هماهنگ شده، تشکیل GVK چند هسته ای و GIK ترکیبات مختلف تعیین می شود و خواص در pH تابع، غلظت عنصر انتقال Ti و اجزای ارگانیک پیچیده، نسبت مولر آنها. این توانایی در بهبود انتخابی پیچیده ظاهر می شود
در ارتباط با زیربناها، محصولات فرآیندهای متابولیک، فعال سازی لینک ها در یک مجتمع (آنزیم) و یک بستر با هماهنگی و تغییر در فرم یک بستر مطابق با خواسته های استرشیت مرکز فعال.
تحول الکتروشیمیایی در بدن مرتبط با انتقال الکترونها با تغییر درجه اکسیداسیون ذرات و وقوع پتانسیل اکسیداسیون و کاهش پتانسیل در محلول همراه است. نقش بزرگی در این تحولات متعلق به مجتمع های چند هسته ای GVK و GIK است. آنها تنظیم کننده های فعال فرایندهای رادیکال آزاد هستند، سیستم استفاده از اشکال فعال اکسیژن، پراکسید هیدروژن، عوامل اکسید کننده، رادیکال ها و در اکسیداسیون زیربنایی ها و همچنین حفظ هوموستاز آنتی اکسیدانی، در حفاظت از بدن از استرس اکسیداتیو دخیل هستند .عمل آنزیمی آنها بر روی بیوسيستم ها مشابه آنزیم ها (مادران سیتوکرو، سوپراکسیدیسموتاز، کاتالاز، پراکسیداز، گلوتاتیون ردوکتاز، دیا هیدروژناز) است. همه اینها نشان می دهد خواص آنتی اکسیدانی بالا از عناصر انتقالی مجرایان.
7.14. سوالات و وظایف خود تست آموزش برای کلاس ها و امتحانات
1. مفهوم ترکیبات پیچیده. تفاوت آنها از نمک های دوگانه چیست و چه چیزی مشترک دارند؟
2. بر اساس نام آنها فرمول ترکیبات پیچیده را به دست آورید: آمونیوم دی هیدروکوت تترالوپوتین (IV)، Triammmingrinitro Balt (III)، آنها را مشخص کنید؛ حوزه هماهنگی داخلی و خارجی را مشخص کنید؛ یون مرکزی و درجه اکسیداسیون آن: لیگاندها، تعداد آنها و دندانپزشکی؛ ماهیت اتصالات. معادله انحلال را در محلول آبی و بیان برای ثابت پایداری بنویسید.
3. خواص کلی ترکیبات پیچیده، جداسازی، پایداری مجتمع ها، خواص شیمیایی مجتمع ها.
4. چگونه واکنش پذیری مجتمع ها با موقعیت های ترمودینامیکی و جنبشی مشخص می شود؟
5. چه اسیدهای آمینه بیشتر از تترامینینو مس (II) با دوام بیشتری دارند و کمتر با دوام هستند؟
6. نمونه های نمونه ای از مجتمع های ماکروسیکسیک تشکیل شده توسط یون های فلزی قلیایی؛ یونهای عناصر D.
7. چه نشانه ای از این مجموعه ها به chelate اشاره می کنند؟ نمونه هایی از ترکیبات پیچیده کلات و غیر تخمیر شده را ارائه دهید.
8. در مثال مس Glycinat، مفهوم اتصالات intracomplex را ارائه دهید. یک فرمول ساختاری از ترکیبات منیزیم را با اسید اتیلندیامینتلتراسیت اسید در فرم سدیم بنویسید.
9. برنامه ریزی یک قطعه معطر طرح دار از هر گونه پیچیده پلیدیر.
10. تعریف مجتمع های چند هسته ای، heteroanore و hetero-tape را بگذارید. نقش فلزات انتقال در شکل گیری آنها. نقش بیولوژیکی داده های اجزاء.
11. چه نوع مواد شیمیایی در یکپارچه با یکپارچگی یافت می شود؟
12. انتقال انواع اصلی هیبریداسیون اربیتال های اتمی، که ممکن است در اتم مرکزی در این مجموعه رخ دهد. هندسه این مجموعه بسته به نوع هیبریداسیون چیست؟
13. چه چیزی از ساختار الکترونیکی اتمهای عناصر S-، P- و D-Blocks برای مقایسه توانایی پیچیدگی و مکان آنها در شیمی مجتمع ها می آید.
14. تعریف مجتمع ها و کابینت ها را بگذارید. نمونه هایی از بیشتر مورد استفاده در زیست شناسی و پزشکی را ارائه دهید. اصول ترمودینامیکی را که در آن Chelatotherapy مستقر است، برسانید. استفاده از ciractons برای خنثی سازی و از بین بردن Xenobiotics از بدن.
15. موارد اصلی اختلال فلزات و هوموتازای انسانی را در بدن انسان شناسایی کنید.
16. برای نمونه هایی از ترکیبات زیستی حاوی آهن، کبالت، روی.
17. نمونه هایی از فرایندهای رقابتی با مشارکت هموگلوبین.
18.ROL یون های فلزی در آنزیم ها.
19. ممکن است چرا برای کبالت در مجتمع های لیگاند های پیچیده (پلییداتت) مقاوم در برابر اکسیداسیون +3، و در نمکهای معمولی مانند هالید، سولفات، نیترات، درجه اکسیداسیون +2؟
20. مس با درجه اکسیداسیون +1 و +2 مشخص می شود. آیا می توان واکنش های کاتالیز با انتقال الکترون را افزایش داد؟
21. آیا روی واکنش های Redox را کاتالیز می کند؟
22. مکانیسم عمل جیوه به عنوان سم چیست؟
23. برای اسید و پایه در واکنش:
Agno 3 + 2nh 3 \u003d No 3.
24. تمرین کنید که چرا نمک سدیم سدیم هیدروکسی متیلیدندند تکنیک اسید به عنوان دارو دارویی استفاده می شود و نه OEDF.
25.cax با یون های فلزی شامل اتصالات زیستی، الکترون ها در بدن حمل می شوند؟
7.15. وظایف تست
1. درجه اکسیداسیون اتم مرکزی در یون مجتمع 2- مساوی با:
a) -4؛
ب) +2؛
در 2؛
د) +4.
2. قوی ترین یون پیچیده:
a) 2-، kn \u003d 8،5х10 -15؛
ب) 2-، kn \u003d 1.5x10 -30؛
ج) 2-، kn \u003d 4x10 -42؛
د) 2-، kn \u003d 1x10 -21.
3. این راه حل شامل 0.1 مول از ترکیب PTCL 4 4NH 3 است. پاسخ به AGNO 3، آن را 0.2 میلی مول از رسوب AgCl تشکیل می دهد. فرمول هماهنگی اولیه مواد اولیه را حذف کنید:
a) cl؛
ب) CL 3؛
ج) CL 2؛
د) CL 4.
4. فرم های پیچیده ای که در نتیجه تشکیل شده است sP 3 D 2- برابری؟
1) Tetrahedra؛
2) مربع؛
4) تریپونال بیپیامید؛
5) خطی.
5. وانت فرمول برای ترکیب پنتیمیاماموکولالت (III) سولفات:
a) na 3 ;
6) [SL 2 (NH 3) 4] CL؛
ج) K 2 [CO (SCN) 4]؛
د) بنابراین 4؛
الف) [co (n 2 O) 6] C1 3.
6. چه لیگاندهای پلی اتیلن هستند؟
الف) C1 -؛
ب) H 2 O؛
ج) ethylenediamine؛
د) nh 3؛
الف) SCN -.
7. عوامل پیچیده عبارتند از:
الف) اهدا کنندگان اتم از جفت های الکترونیکی؛
ج) اتم ها و یون ها پذیرفته شده از جفت های الکترونیکی؛
د) یون های اتم و اهدا کننده جفت های الکترونیکی.
8. کوچکترین عناصر توانمند سازی پیچیده تشکیل دهنده:
مانند؛ ج) d؛
ب) پ؛ د) F.
9. لیگاند ها عبارتند از:
الف) مولکول های اهدا کننده جفت الکترونیکی؛
ب) جفت های گیرنده الکترونیکی جفت؛
ج) مولکول ها و اهداکنندگان یون از جفت های الکترونیکی؛
د) مولکول ها و یونها - گیرنده های جفت الکترونیکی.
10. ارتباطات در حوزه هماهنگی داخلی مجتمع:
الف) تبادل کووالانسی؛
ب) پذیرش اهدا کننده کووالانسی؛
ج) یونیک؛
د) هیدروژن.
11. بهترین ترکیبات خواهد بود:
ترکیبات جامع ساختار آنها بر اساس نظریه هماهنگی A. Verner. یونی پیچیده، هزینه او. کاتیونی، آنیونی، مجتمع های خنثی. nomenclature، نمونه ها.



واکنش واکنش لیگاند ها. ثابت یون مجتمع ناپایدار، پایداری پایدار.

 نسبت غلظت یون های شکسته به مقدار بی سابقه نسبت به غلظت یون های بی سابقه ای است.
نسبت غلظت یون های شکسته به مقدار بی سابقه نسبت به غلظت یون های بی سابقه ای است.
به دهان \u003d 1 / به لانه (معکوس)
 تفکیک ثانویه -فروپاشی حوزه داخلی پیچیده به اجزای اجزاء.
تفکیک ثانویه -فروپاشی حوزه داخلی پیچیده به اجزای اجزاء.

43. پذیرش لیگاند یا برای عامل پیچیده: جایگزینی تعادل متعادل و ترکیبی از لیگاند ها. ثابت کل تعادل همبستگی ترکیبی از لیگاندها.
به عنوان یک نتیجه از رقابت، پروتون یک مجتمع نسبتا دوام را از بین می برد، تشکیل یک اختلال ضعیف - آب.
CL + NIS0 4 + 4NH 3 ^ S0 4 + AGCL I
این یک نمونه از یک رقابت لیگاند برای عامل پیچیده است، با تشکیل یک مجتمع با دوام تر (KH + 9.3-1 (G 8؛ KH [M (W 3) 6] 2+ \u003d 1.9-Yu-9) و ترکیب استخدامی AGCL - K S \u003d 1.8 10 "10
نمایندگی بر ساختار مزارع فلزی و سایر ترکیبات زیستی (هموگلوبین، سیتوکروم، کوبالامین). اصول فیزیکی شیمیایی هموگلوبین حمل و نقل اکسیژن





کابالیمین ویتامین B 12. آنها گروهی از مواد فعال زیست شناختی کبالت را به نام کوبالامین ها نامیده اند. این در واقع شامل سیانو کوبالامین، هیدروکسی کوبالومین و دو سور ویتامین B12: متیلکووبالامین و 5-deoxyadenosylcobalamine.
گاهی اوقات به معنای باریک، ویتامین B 12 به نام Cyanocobalamine نامیده می شود، زیرا دقیقا در این فرم به بدن انسان، مقدار اصلی ویتامین B 12 دریافت می شود، بدون از دست دادن این واقعیت که مترادف با B 12 و چندین نفر نیست ترکیبات همچنین دارای فعالیت B 12 - ویتامین هستند. ویتامین B12 همچنین عامل بیرونی قلعه نامیده می شود.
B 12 دارای پیچیده ترین ساختار شیمیایی در مقایسه با سایر ویتامین ها است، اساس آن Corrinoecolo است. Corrin در بسیاری از موارد شبیه به پورفیرین (ساختار شیمیایی پیچیده، که بخشی از HEM، کلروفیل icotochromes) است، اما متفاوت از پورفیرین در این واقعیت است که دو دوره پیروزی در Corrod به طور مستقیم متصل می شوند و نه پل متیلن. در مرکز ساختار رومی، یون کبالت است. چهار پیوند هماهنگی کبالت با اتم های نیتروژن تشکیل شده است. یک رابطه هماهنگی دیگر کبالت را با یک نوکلئوتید Coinmetythylbenzimidazole متصل می کند. دومی، ششمین پیوند هماهنگی کبالت باقی می ماند: این برای این ارتباط است که یک گروه سیانو، یک گروه هیدروکسیل، یک متیل یا 5 "-DEoxyadenosal باقی مانده، با تشکیل چهار نوع از ویتامین B 12، به ترتیب پیوست شده است . اتصال کربن کربن کربن در ساختار Cyanocobalamin - تنها نمونه شناخته شده طبیعت شناخته شده از Covernent Bond Carbon-Carbon.
واکنش اصلی جایگزینی در محلول های آبی مبادله مولکول های آب است (22) - برای تعداد زیادی از یونهای فلزی مورد مطالعه قرار گرفت (شکل 34). تبادل مولکول های آب از حوزه هماهنگی یون فلز با جرم اصلی مولکول های آب به عنوان یک حلال، برای اکثر فلزات به سرعت ادامه می یابد، و بنابراین سرعت چنین واکنش به طور عمده توسط آرامش انجام شد. این روش شامل نقض تعادل سیستم است، به عنوان مثال افزایش شدید دما. در شرایط جدید (درجه حرارت بالاتر)، سیستم دیگر در تعادل نیست. سپس میزان استقرار تعادل را اندازه گیری کنید. اگر شما می توانید دمای راه حل را تغییر دهید 10 -8 ثانیهسپس شما می توانید سرعت واکنش را اندازه گیری کنید که نیاز به زمان بیشتری برای تکمیل آن دارد 10 -8 ثانیه.
همچنین ممکن است میزان جایگزینی مولکول های آب هماهنگ شده در یون های مختلف فلزی با لیگاندها را اندازه گیری کند، بنابراین 2- 4، S 2 O 3 2-، EDTA و غیره (26). سرعت چنین واکنش
این بستگی به غلظت یون فلز هیدراته دارد و به غلظت لیگاند ورودی بستگی ندارد، که اجازه می دهد اولین معادله سفارش برای توصیف این سیستم ها (27). در بسیاری از موارد، میزان واکنش (27) برای این یون فلز به ماهیت لیگاند ورودی (L) بستگی ندارد، چه مولکول های H 2 O یا یون ها، 4-2، S 2 O 3 2- یا EDTA .
این مشاهدات، و همچنین این واقعیت که غلظت لیگاند ورودی در معادله سرعت این فرایند گنجانده نشده است، نشان می دهد که این واکنش ها به وسیله مکانیسم که در آن مرحله آهسته است، شکستن اتصال بین یون و آب فلزی است . اتصال به دست آمده به احتمال زیاد به سرعت به سرعت هماهنگ کردن لیگاند های نزدیک است.
در بخش. 4 این فصل نشان داده شده است که یون های هیدراته شده بالاتر از جمله Al 3+ و SC 3+، مولکول های آب مبادله کندتر از m 2+ و یون های M +؛ این باعث می شود که فرض کنیم که در مرحله تعیین سرعت کل فرآیند، پارگی اتصالات نقش مهمی ایفا می کند. نتیجه گیری های به دست آمده در این مطالعات نهایی نیست، اما آنها دلیلی را به فکر می کنند که در واکنش جایگزینی یونهای فلزات هیدراته شده، فرایندهای S N 1 مهم هستند.
احتمالا بیشتر ترکیبات پیچیده مورد مطالعه آمین های کبالت (III) هستند. پایداری آنها، سهولت آماده سازی و واکنش های آهسته در حال حاضر با آنها، آنها را به ویژه برای مطالعات جنبشی راحت می کند. از آنجا که مطالعات این مجتمع ها به طور انحصاری در محلول های آبی انجام می شود، در ابتدا واکنش این مجتمع ها را با مولکول های حلال - آب بررسی می کنند. مشخص شد که به طور کلی مولکول های آمونیاک یا آمین، که توسط یون CO (III) هماهنگ شده اند، به آرامی توسط مولکول های آب جایگزین می شوند که معمولا جایگزینی لیگاندهای دیگر و نه آمین ها را در نظر می گیرند.
سرعت واکنش نوع (28) مورد بررسی قرار گرفت و مشخص شد که ابتدا در مورد مجتمع کبالت (X یکی از آنیون های ممکن است) بود.
از آنجا که در محلول های آبی، غلظت H 2 O همیشه برابر است 55.5 مترتعیین تأثیر تغییرات در غلظت مولکول های آب بر میزان واکنش غیرممکن است. معادلات سرعت (29) و (30) برای یک محلول آبی به صورت آزمایشی قابل تشخیص نیستند، زیرا به سادگی با k "\u003d k" برابر است. در نتیجه، معادله سرعت واکنش نمی توان گفت که آیا H 2 O در مرحله تعیین سرعت روند شرکت می کنند. پاسخ به این سوال این است که آیا این واکنش زیر مکانیزم S N 2 با جایگزینی یون X در مولکول H 2 O یا مکانیسم SN 1 است که برای اولین بار از ترکیبات جدا شده است، به دنبال افزودن H 2 O است مولکول، باید با استفاده از سایر داده های تجربی بدست آید.
راه حل های این کار را می توان با دو نوع آزمایش به دست آورد. سرعت هیدرولیز (جایگزینی یک یون CL - بر روی مولکول آب) ترانس- + تقریبا 10 3 برابر سرعت هیدرولیز 2+. افزایش اتهام این مجموعه منجر به افزایش روابط فلزی - لیگاند، و در نتیجه، به ترمز قطع این اتصالات. همچنین باید توجه داشته باشید جذب لیگاندهای ورودی و تسهیل جریان واکنش واکنش. از آنجا که کاهش سرعت به عنوان اتهام افزایش پیچیده تشخیص داده می شود، پس در این مورد به نظر می رسد یک فرآیند متفاوتی بیشتر (S n 1).
راه دیگری از شواهد بر اساس مطالعه هیدرولیز یک سری از مجتمع های مشابه است ترانس- + در این مجتمع ها، مولکول اتیلندیامین با دیامین های مشابه جایگزین شد که در آن اتم های هیدروژن در اتم کربن در گروه CH 3 جایگزین شدند. مجتمع هایی حاوی دیامین های جایگزین واکنش سریع تر از مجتمع اتیلن دیامین را نشان می دهند. جایگزینی اتم های هیدروژن بر روی گروه CH 3 افزایش حجم لیگاند را افزایش می دهد، که باعث می شود که یک لیگاند دیگر به اتم فلزی حمله کند. این موانع استریل واکنش را با توجه به مکانیزم S N 2 کاهش می دهد. حضور اتم حجم لیگاند فله در نزدیکی اتم فلزی به فرآیند متفاوتی کمک می کند، زیرا حذف یکی از لیگاند ها انباشت آنها را در اتم فلزی کاهش می دهد. افزایش مشاهده شده در میزان هیدرولیز مجتمع ها با لیگاندهای فله، اثبات خوبی از جریان واکنش از طریق مکانیسم S N 1 است.
بنابراین، به عنوان یک نتیجه از مطالعات متعدد از ترکیبات اسید آمین اسید (II)، معلوم شد که جایگزینی agroups اسید مولکول های آب یک فرآیند متفاوتی در طبیعت است. اتصال اتم کبالت - لیگاند قبل از شروع مولکول های آب شروع به ورود به مجموعه می شود. در مجتمع هایی که شارژ 2+ و بالاتر دارند، کاشی ارتباطات کبالت - لیگاند بسیار دشوار است و ورود مولکول های آب شروع به نقش مهمی می کند.
مشخص شد که جایگزینی گروه اسید اسید (X -) در مجتمع کبالت (III) به گروه دیگری نسبت به مولکول H 2 O (31) در ابتدا از طریق جایگزینی مولکول آن عبور می کند
حلال - آب با جایگزینی بعدی برای گروه جدید Y (32).
بنابراین، در بسیاری از واکنش های با مجتمع های کبالت (III)، میزان واکنش (31) برابر با میزان هیدرولیز است (28). فقط هیدروکسیل یون از سایر واکنش ها متفاوت است و با توجه به واکنش پذیری با Ammines CO (III). این به سرعت به مجتمع های آموسی کبالت (III) واکنش می دهد (تقریبا 10 6 برابر سریعتر از آب) با نوع واکنش هیدرولیز پایه (33).
مشخص شد که این واکنش اولین مرتبه نسبت به لیگاند جایگزینی آه - (34). کل روش واکنش دوم واکنش و جریان غیر معمول سریع واکنش نشان می دهد که یون OH یک واکنش نوکلئوفیلی فوق العاده موثر با توجه به مجتمع های CO (III) است و واکنش از طریق مکانیسم S N 2 از طریق تشکیل یک اتصال متوسط \u200b\u200bادامه می یابد.
با این حال، این ویژگی OH نیز می تواند توسط مکانیسم دیگری توضیح داده شود [معادلات (35)، (36)]. در واکنش (35) مجتمع 2+ مانند اسید (با توجه به Brenets) رفتار می کند، به مجموعه ای پیچیده +، که است امیدیو- (حاوی)-به ترکیب - پایه مربوط به اسید 2+.
واکنش پس از آن، از طریق مکانیزم S N 1 (36) جریان می یابد تا پنج هماهنگ مختصری را تشکیل دهد، بیشتر واکنش نشان می دهد با مولکول های حلال، که منجر به محصول واکنش نهایی می شود (37). این مکانیزم واکنش با نرخ پاسخ دوم مرتبه سازگار است و مربوط به مکانیزم S n 1. از زمان واکنش در مرحله تعیین میزان شامل پایه ای که در مجتمع اولیه تشکیل شده است، شامل این مکانیزم تعیین شده است. 1SV
برای تعیین اینکه کدام یک از این مکانیزم ها بهترین توصیف مشاهدات تجربی است، بسیار دشوار است. با این حال، شواهد قانع کننده ای وجود دارد که فرضیه S N 1CB را تایید می کند. بهترین استدلال ها به نفع این مکانیسم عبارتند از: مجتمع های هشت ضلعی CO (III) در همه واکنش ها در مکانیزم های متفاوتی SN 1 واکنش نشان می دهند، و هیچ استدلالی قانع کننده ای وجود ندارد، چرا یون OH - باید روند SN 2. را تعیین کند ثابت شده است که هیدروکسیل یون یک واکنش دهنده نوکلئوفیلی ضعیف در واکنش های PT (II) است و بنابراین واکنش غیر معمول آن با توجه به CO (III) به نظر می رسد غیر منطقی است. واکنش های ترکیبات کبالت (III) در رسانه های غیر آبی به عنوان اثبات عالی تشکیل ترکیبات متوسط \u200b\u200bپنج مختصات ارائه شده توسط مکانیسم S N 1 SV استفاده می شود.
اثبات نهایی این واقعیت است که، در غیاب CO (III)، اتصالات N-H در CO (III) واکنش نشان می دهد با یونهای آن -. البته، البته، دلیل آن را باور می کند که برای سرعت واکنش خواص اساسی اسید پیچیده، مهم تر از خواص نوکلئوفیلی است. این واکنش هیدرولیز اصلی شرکت های آمین (III) یک تصویر از آن است واقعیت این است که داده های جنبشی اغلب می توانند نه تنها به یک روش تفسیر شوند و یک یا چند مکانیزم احتمالی را از بین ببرند، شما باید یک آزمایش نسبتا نازک داشته باشید.
در حال حاضر، واکنش جایگزینی تعداد زیادی از ترکیبات هشت ضلعی مورد بررسی قرار گرفته است. اگر ما مکانیسم های واکنش آنها را در نظر بگیریم، فرآیند متفکرانه اغلب یافت می شود. این نتیجه غیر منتظره نیست، زیرا شش لیگاند فضای کوچکی را در اطراف اتم مرکزی ترک می کنند تا گروه های دیگر را به آن متصل کنند. این تنها به چند نمونه شناخته شده است زمانی که وقوع یک ترکیب متوسط \u200b\u200bهفت مختصات ثابت شده است یا تاثیر لیگاند معرفی شده شناسایی شده است. بنابراین، S n 2، مکانیزم را نمی توان به طور کامل به عنوان مسیر احتمالی واکنش جایگزینی در مجتمع های هشت ضلعی رد کرد.
مقدمه ای بر کار
ارتباط کار. مجتمع های پورفیرین با فلزات در درجه های بالا اکسیداسیون می تواند پایه ها را بسیار کارآمد تر از مجتمع های M 2+ هماهنگ کند و ترکیبات هماهنگی مخلوط را تشکیل می دهد که در اولین حوزه هماهنگی اتم فلزی مرکزی همراه با لیگاند ماکروسیکلیک، غیر سیکل سیکل است ، و گاهی مولکول های هماهنگ شده. مسائل مربوط به سازگاری لیگاند ها در چنین مجتمع ها بسیار مهم هستند، زیرا دقیقا به صورت مجتمع های مخلوط پورفیرین، توابع بیولوژیکی خود را انجام می دهند. علاوه بر این، واکنش افزودنی برگشت پذیر (انتقال) مولکول های پایه مشخص شده توسط ثابت های تعادل متوسط \u200b\u200bبالا می تواند به طور موفقیت آمیز برای جداسازی مخلوط ایزومرهای ارگانیک، برای تجزیه و تحلیل کمی، برای اهداف محیط زیست و پزشکی استفاده شود. بنابراین، مطالعات ویژگی های کمی و استئوکیومتری تعادل تعادل اضافی بر روی فلزات (MR) و جایگزینی لیگاندهای ساده در آنها نه تنها از دیدگاه دانش نظری از خواص متالوفیررین به عنوان ترکیبات پیچیده مفید است همچنین برای حل وظیفه عملی پیدا کردن گیرنده ها و حامل مولکول های کوچک یا یونهای کوچک. تا به امروز، مطالعات سیستماتیک برای یونهای فلزی بالا عبور عملا وجود ندارد.
هدف از کار. این مقاله به مطالعه واکنش های مجتمع های مخلوط پورفیرین مخلوط از کاتیون های بالایی از فلزات Zr IV، HF IV، MO V و WV با استفاده از BioVActive N-Bases: Imidazole (IM)، پیریدین (PY)، پیریدین اختصاص داده شده است (PYZ)، بنزیمیدازول (BZIM)، پایداری مشخص و خواص نوری مجتمع های مولکولی، توجیه مکانیسم های واکنش گام به گام.
تازگی علمی. روشهای تیتراسیون اسپکتروفتومتری اصلاح شده، سینتیک شیمیایی، جذب الکترون و نوسان و 1 ساعته طیف سنجی NMR ابتدا توسط ویژگی های ترمودینامیکی و مکانیزم های استئوشیومتریک واکنش های N-base با متالوپورفرین ها با یک حوزه هماهنگی مخلوط (X) N-2 MTRR (X) به دست آمد - AcidOligand CL -، OH -، O 2-، TRP - Tetraphenylpirin Dyanion). ثابت شده است که در اکثریت قریب به اتفاق از موارد، فرایندهای تشکیل سوپرومولکول ها متالوفرروفرین - پایه جریان گام به گام و شامل چندین واکنش ابتدایی برگشت ناپذیر و آهسته غیر قابل برگشت از هماهنگی مولکول های پایه و جایگزینی اسیدولینگان ها است. برای هر یک از مراحل واکنش های گام، استوکیومتری، ثابت های تعادل یا سرعت، دستورات واکنش های آهسته بر پایه، محصولات فکری مشخص شده (UV، طیف های قابل مشاهده برای محصولات متوسط \u200b\u200bو UV، قابل مشاهده و IR - برای پایان). برای اولین بار، معادلات همبستگی برای پیش بینی پایداری مجتمع های سوپرمولکول با سایر پایگاه ها به دست آمد. معادلات در عملیات برای بحث در مورد مکانیزم جایگزینی دقیق مورد استفاده قرار می گیرند، در مولکول های پایه در مولکول های پایه قرار دارند. خواص MR شرح داده شده است، که باعث می شود که چشم انداز استفاده برای تشخیص، جداسازی و تجزیه و تحلیل کمی از پایگاه های فعال بیولوژیکی، مانند پایداری نسبتا بالا از مجتمع های سوپرمولکولار، پاسخ نوری واضح و سریع، آستانه حساسیت کم، بار دوم، باعث شود.
اهمیت عملی کار. نتایج کمی و اثبات مکانیسم های استوکیومتریک واکنش های پیچیده مولکولی برای شیمی هماهنگی لیگاند های ماکروتر اکسیوئیک ضروری است. این پایان نامه نشان داده شده است که مجتمع های حاوی پورفیرین مخلوط حساسیت بالا و انتخابی برای پایگاه های آلی زیست فعال را نشان می دهد، در عرض چند ثانیه یا چند دقیقه پاسخ نوری را برای تشخیص عملی واکنش های با پایگاه های Bases، اجزای مواد مخدر و محصولات غذایی مناسب می دهد برای استفاده به عنوان اجزای سنسورهای پایه در محیط زیست، صنایع غذایی، پزشکی و کشاورزی توصیه می شود.
تأیید کار. نتایج کار گزارش شده و مورد بحث قرار گرفت:
کنفرانس بین المللی IX در مورد حل و جمع آوری پیچیدگی در راه حل ها، Ples، 2004؛ سمپوزیوم XII برای تعامل بین مولکولی و سازگاری مولکول ها، Pushchino، 2004؛ XXV، XXVI و جلسات علمی XXVI و XXIX از سمینار روسیه در شیمی پرفیرین ها و آنالوگ های آنها، ایوانوو، 2004 و 2006؛ دبیرستان دانشمندان جوان کشورهای مستقل مشترک المنافع کشورهای مستقل مشترک المنافع در شیمی پورفیرین ها و ترکیبات مرتبط، سنت پترزبورگ، 2005؛ هشتمین دانشکده علمی VIII - کنفرانس های شیمی آلی، کازان، 2005؛ کنفرانس علمی همه روسیه "ترکیبات طبیعی ماکروسیکلیک و آنالوگ های مصنوعی آنها"، Syktyvkar، 2007؛ کنفرانس بین المللی XVI در مورد ترمودینامیک شیمیایی در روسیه، Suzdal، 2007؛ XXIII بین المللی کنفرانس Chughaev در مورد شیمی هماهنگی، اودسا، 2007؛ کنفرانس بین المللی Porphyrins و Phtalocyanines ISPP-5، 2008؛ 38 کنفرانس بین المللی شیمی هماهنگی، اسرائیل، 2008.
واکنش های شیمیایی مشروط مجتمع ها به تبادل، اکسیداتیو، توانبخشی، ایزومریزاسیون و لیگاندهای هماهنگ تقسیم می شوند.
جداسازی اولیه مجتمع ها بر روی حوزه داخلی و بیرونی، جریان مبادله یونهای هزینه را تعیین می کند:
x m + mnay \u003d y m + mnax.
اجزای حوزه داخلی مجتمع ها همچنین می توانند در فرآیندهای متابولیک با مشارکت هر دو لیگاند و عامل پیچیده شرکت کنند. برای مشخص کردن واکنش های جایگزینی لیگاند ها یا یون فلز مرکزی، تعیین و اصطلاحات پیشنهاد شده توسط K. inslold برای واکنش ترکیبات آلی استفاده می شود (شکل 42)، nucleophilicS n. و الکتروفیلS جایگزینی:
z + y \u003d z + x s n
Z + M "\u003d Z + M S E.
با توجه به مکانیزم واکنش، جایگزینی تقسیم می شود (شکل 43) به انجمنی (s n 1 و s e 1 ) و discociative (s n 2 و s e 2 )، در انتقال با یک تعداد هماهنگی بزرگ و کاهش یافته متفاوت است.
تخصیص مکانیزم واکنش به وابستگی یا متفکرانه دشوار است به طور تجربی به کار بر روی دستیابی به وظیفه شناسایی متوسط \u200b\u200bبا کاهش یا افزایش تعداد هماهنگی. در این راستا، اغلب مکانیزم واکنش بر اساس داده های غیر مستقیم بر اثر غلظت واکنش های واکنش بر میزان واکنش، تغییر ساختار هندسی محصول واکنش و غیره مورد قضاوت قرار می گیرد.
برای مشخص کردن میزان واکنش واکنش های لیگاند های مجتمع، برنده جایزه نوبل 1983 G. Taube (شکل 44) پیشنهاد کرد که از اصطلاح "Labile" و "بی اثر" استفاده کند، بسته به زمان واکنش واکنش لیگاندها کمتر از 1 دقیقه. اصطلاحات مورد نظر یا بی اثر، مشخصه سینتیک واکنش های واکنش های لیگاند هستند و نباید با ویژگی های ترمودینامیکی پایداری یا عدم پذیرش مجتمع ها اشتباه گرفته شود.
لایحه یا بی اثر مجتمع ها بستگی به ماهیت یونی عامل پیچیده و لیگاند دارد. در توافق با تئوری میدان لیگاند:
1. مجتمع های اکتبر 3.d. فلزات انتقال با توزیع ولنس (n -1) d الکترونها بر روی سیگما* (به عنوان مثال ) Breakdown Mo Labils.
4- (T 2G 6 E G 1) + H 2 O= 3- + CN -.
علاوه بر این، کمتر انرژی تثبیت میدان کریستال پیچیده، قابلیت تغذیه بیشتر است.
2. مجتمع های اکتبر 3.d. فلزات انتقال با سیگما آزاد* پاره شدن اوربیتال ها و توزیع یکنواخت از والنس (n -1) D الکترونها توسط T 2 G Orbitals (T 2 G 3، T 2 G 6) بی اثر هستند.
[CO III (CN) 6] 3- (T 2 G 6 E G 0) + H 2 O \u003d
[CR III (CN) 6] 3- (T 2 G 3 E G 0) + H 2 O \u003d
3. مربع مسطح و هشت ضلعی 4d و 5 د فلزات انتقال که الکترونها را روی سیگما ندارند* شکست INERT.
2+ + H 2 O \u003d
2+ + H 2 O \u003d
تأثیر ماهیت لیگاندهای بر میزان واکنش های واکنش لیگاند ها در چارچوب "نفوذ متقابل لیگاندها" در نظر گرفته می شود. یک مورد خاص از مدل نفوذ متقابل لیگاند ها، فرموله شده در سال 1926 I.I. Chernyaev مفهوم نفوذ ترانس (شکل 45) - "قابلیت تغذیه لیگاند در مجتمع بستگی به ماهیت لیگاند ترانس واقع دارد" - و ارائه تعدادی از تأثیرات ترانس لیگاند:CO، CN -، C 2 H 4\u003e PR 3، H -\u003e CH 3 -، SC (NH 2) 2\u003e C 6 H 5 -، شماره 2 -، I -، SCN -\u003e BR -، CL -\u003e PY ، NH 3، OH -، H 2 O.
مفهوم نفوذ ترانزیت باعث شد تا قوانین تجربی را اثبات کند:
1. حکمرانی - تحت عمل آمونیاک یا آمین ها در tetrachlopla-tinat (دوم ) پتاسیم همیشه Dichlodiamineplatin CIS-Configuration:
2 - + 2NH 3 \u003d CIS - + 2CL -.
از آنجا که واکنش به دو مرحله ادامه می یابد و لیگاند کلرید دارای نفوذ بزرگ ترانس است، جایگزینی لیگاند کلرید دوم بر روی آمونیاک با تشکیل CIS رخ می دهدPT (NH 3) 2 CL 2]:
2- + NH 3 \u003d -
NH 3 \u003d CIS -.
2. قانون Hiergensen - تحت عمل اسید هیدروژنیک بر روی کلرید تتامامامنا پلاتین (دوم ) یا ترکیبات مشابه به دست آمده Dichlorod-Amminplatin Trans-configuration:
[PT (NH 3) 4] 2+ + 2 HCL \u003d TRANS- [PT (NH 3) 2 CL 2] + 2 NH 4 CL.
مطابق با تعدادی از نفوذ ترانسفورماتور لیگاندها، جایگزینی مولکول آمونیاک دوم در لیگاند کلرید منجر به تشکیل ترانسفورماتور می شودPT (NH 3) 2 CL 2].
3. واکنش Tiomea Kurnakova - محصولات مختلف واکنش Tiomo-Chevina با اندازه گیری های هندسی [PT (NH 3) 2 CL 2] و CIS- [PT (NH 3) 2 CL 2]:
سیس - + 4thio \u003d 2+ + 2Cl - + 2NH 3.
ماهیت متفاوتی از محصولات واکنش با تأثیر بالایی از تیتووین همراه است. مرحله اول واکنش ها جایگزینی لیگاندهای کلرید تئودیشیمیایی با تشکیل ترانس و CIS- [PT (NH 3) 2 (Thio) 2] 2+:
trans- [PT (NH 3) 2 CL 2] + 2 Thio \u003d Trans- [PT (NH 3) 2 (Thio) 2] 2+
cIS - + 2Thio \u003d CIS - 2+.
در CIS- [PT (NH 3) 2 (Thio ) 2] 2+ دو مولکول آمونیاک در موقعیت ترانس به Thiouvine تحت تعویض بیشتر قرار می گیرند، که منجر به آموزش می شود 2+ :
سیس - 2+ + 2Thio \u003d 2+ + 2NH 3.
در Trans- [PT (NH 3) 2 (Thio ) 2] 2+ دو مولکول آمونیاک با یک نفوذ کوچک کوچک در موقعیت ترانس به یکدیگر قرار دارند و بنابراین توسط ThioCheaver جایگزین نمی شوند.
قوانین نفوذ نفوذ توسط I.I. Chernyaev هنگام مطالعه واکنش های جایگزینی لیگاند در مجتمع های پلاتین مسطح (دوم ) در آینده، نشان داده شد که تأثیر گذار از لیگاند ها نیز در مجتمع های دیگر فلزات وجود دارد (PT (IV)، PD (II)، CO (III)، CR (III)، RH (III)، IR (III) )) و یک ساختار هندسی دیگر. درست است، ردیف های تاثیر گذار از لیگاند ها برای فلزات مختلف تا حدودی متفاوت است.
لازم به ذکر است که نفوذ ترانس است اثر جنبشی- تاثیر گذار بزرگتر دارای این لیگاند است، با سرعت بیشتری، لیگاند دیگری دیگر با توجه به آن در موقعیت ترانس جایگزین می شود.
همراه با اثر جنبشی نفوذ ترانس، در وسطجامه قرن A.A. Greenberg و Yu.N. Cuccushkin وابستگی به نفوذ ترانزیت لیگاند را نصب کردL. از لیگاند واقع در CIS موقعیت بهL. . بنابراین، مطالعه میزان واکنش جایگزینیcl - آمونیاک در مجتمع های پلاتین (II):
[PTCL 4] 2- + NH 3 \u003d [PTNH 3 CL 3] - + CL - K \u003d 0.42 10 4 لیتر / مول از جانب
[PTNH 3 CL 3] - + NH 3 \u003d CIS- [PT (NH 3) 2 CL 2] + CL - K \u003d 1.14 10 4 لیتر / مول از جانب
trans- [PT (NH 3) 2 CL 2] + NH 3 \u003d [PT (NH 3) 3 CL] + + CL - K \u003d 2.90 10 4 لیتر / مول از جانب
این نشان داد که حضور CIS به لیگاند جایگزین کلرید یک و دو مولکول آمونیاک منجر به افزایش ترتیبی در میزان واکنش می شود. این اثر جنبشی نامیده شد نفوذ CIS. در حال حاضر، هر دو اثر جنبشی از نفوذ ماهیت لیگاند بر میزان واکنش های واکنش لیگاند ها (نفوذ و نفوذ CIS) در مفهوم عمومی ترکیب می شوند نفوذ متقابل لیگاند ها.
اثبات تئوری اثر تاثیر متقابل لیگاند ها با توسعه ایده های مربوط به اوراق قرضه شیمیایی در ترکیبات پیچیده مرتبط است. در 30 ثانیهجامه قرن A.A. Greenberg و B.V. Nekrasov Trans تحت تاثیر قرار گرفته به عنوان بخشی از مدل قطبش:
1. نفوذ ترانس برای مجتمع ها، یون مرکزی فلز است که دارای قطب پذیری بزرگ است.
2. فعالیت ترانزیت لیگاند ها توسط انرژی قطبش متقابل لیگاند و یون فلز تعیین می شود. برای این یون فلزی، تأثیر گذار لیگاند توسط قطبش پذیری آن و فاصله ی یون مرکزی تعیین می شود.
مدل قطبش با داده های تجربی برای مجتمع های لیگاند های ساده آنیونی، مانند یون های هالید سازگار است.
در سال 1943. گرینبرگ این فرضیه را مطرح کرد که فعالیت ترانس لیگاند ها با خواص بهبود آنها همراه است. جابجایی تراکم الکترون از لیگاند ترانس فعال به فلز باعث کاهش بار موثر یون فلز می شود که منجر به تضعیف پیوند شیمیایی با لیگاند ترانس می شود.
توسعه ارسال ها در مورد نفوذ ترانس با فعالیت ترانس بزرگ لیگاندها بر اساس مولکول های آلی غیر اشباع مانند اتیلن در [PT (C 2 H 4) CL 3 ] - به گفته چاتا و سفارشات (شکل 46)، این به دلیل آن استpiتعامل داوطلبانه این لیگاندهای با فلز و مکانیسم وابسته واکنش های واکنش لیگاند های ترانس واقع شده است. هماهنگی به یون فلز حمله به فلزZ. منجر به تشکیل پنج هم مختصات واسطه های دوجانبه تریژن تریژن سهگانه می شود، و پس از آن شکاف سریع لیگاند ترک X را تشکیل می دهد. شکل گیری چنین میانجی کمک می کندpiپیوند فلزی لیگاند مرگبار لیگاندY. کاهش تراکم الکترونی فلز و کاهش انرژی فعال سازی حالت انتقال و پس از آن جایگزینی سریع لیگاند X.
همچنین پ. پذیرنده (C 2 H 4، CN -، CO ...) لیگاندهای تشکیل یک پیوند شیمیایی فلزی لیگاند، دارای نفوذ بالایی بالاs. لیگاندهای اهدا کننده:H -، CH 3 -، C 2 H 5 - ... تأثیر گذار از این لیگاند ها توسط تعامل اهدا کننده گیرنده لیگاند X با فلز تعیین می شود، تراکم الکتریکی آن را کاهش می دهد و اتصال فلز را با لیگاند خروجی تضعیف می کندY.
بنابراین، موقعیت لیگاند ها در یک سری فعالیت ترانس توسط عمل مشترک سیگما تعیین می شود اهداء اول pi خواص لیگاند - سیگمااهداء اول piخواص پذیرش لیگاند نفوذ خود را افزایش می دهد، در حالی کهpi اهدا کننده - تضعیف کدامیک از این اجزاء از فلزات لیگاند تعامل غالب در نفوذ ترانس بر اساس محاسبات کوانتومی شیمیایی ساختار الکترونیکی وضعیت انتقال واکنش است.