Vývoj chromatografie. Chromatografia ako metóda výskumu
Chromatografia je ruský vedecká, botanika a fyzikálnumochemista Michail Semenovičská farba.
Objav chromatografie sa vzťahuje na čas dokončenia práce na diplomovej práci v Petrohrade (1900 - 1902) a prvé obdobie práce vo Varšave (1902 - 1903). Skúmanie pigmentov rastlín, farba prešla roztokom zmesi veľmi málo líši sa vo farbe pigmentov cez trubicu naplnenú adsorbentným práškovým uhličitanom vápenatým a potom sa potom premyje adsorbent s čistým rozpúšťadlom. Samostatné zložky zmesi boli rozdelené a tvorené farebnými pruhmi. Podľa modernej terminológie sa farba objavila vývojový variant chromatografie (vyvíjanie kvapalnej adsorpčnej chromatografie). Hlavné výsledky výskumu o vývoji chromatografie, ktoré vytvorili ho. Farba načrtnutá v knihe "Chromophyls v rastlinnom a živočíšnom svete" (1910), čo je jeho doktorandská dizertačná práca. Chromatografia plynu sedimentárna iónová výmena
Farba široko používa chromatografickú metódu nielen na separáciu zmesi a vytvorenie IT multicomponency, ale aj pre kvantitatívnu analýzu, na tento účel rozbil sklenený stĺpec a narezal adsorpčnú kolónu na vrstvy. Farba vyvinula zariadenie na kvapalinovú chromatografiu, pričom prvýkrát vykonala chromatografické procesy za zníženého tlaku (čerpanie) a pri určitom pretlaku vyvinuté odporúčania na prípravu účinných stĺpcov. Okrem toho predstavil mnoho základných pojmov a podmienok novej metódy, ako napríklad "chromatografia", "prejav", "posunutie", "chromatogram" atď.
Chromatografia sa najprv použila veľmi zriedka, jeho skryté obdobie trvalo asi 20 rokov, počas ktorého sa objavil len veľmi malý počet správ o rôznych aplikáciách metódy. A len v roku 1931, R. Kunu (Nemecko) A. Winterstein (Nemecko) a E. LEDTERRE (Francúzsko), ktorí pracovali v chemickom laboratóriu (LED R. KUN), Ústavu cisára Wilhelma na lekárskom výskume v Heidelbergu, Podarilo sa prideliť tento spôsob A - a B-karotén zo surového karoténu a tým demonštrovať hodnotu farebného otvoru.
Dôležitým stupňom vývoja chromatografie bol objav sovietskych vedcov N.A. Izmailov a M.S. Schreiber metóda chromatografie v tenkej vrstve (1938), ktorá umožňuje analýzu mikrokolizmom látky.
Ďalším dôležitým krokom bol objav A. Martin a R. Sing (Anglicko) variantu kvapalnej distribučnej chromatografie na príklade separácie acetylových derivátov aminokyselín na kolóne naplnenej silikagélom, nasýteným vodou, s použitím chloroformu ako rozpúšťadlo (1940). Zároveň sa poznamenalo, že ako mobilná fáza môže byť použitá nielen kvapalina, ale aj plyn. O niekoľko rokov neskôr boli títo vedci navrhnutí na oddelenie derivátov aminokyselín na zvlhčenú vodou s butanolom ako mobilnej fázy. Implementovali tiež prvý dvojrozmerný separačný systém. Na otvorenie distribučnej verzie chromatografie, Martin a Sping dostal Nobelovu cenu v chémii. (1952). Ďalej, Martin a A. James vykonávali variant rozvodnej chromatografie plynu, čím sa oddelila zmes na zmiešanej sorbente z DS-550 silikónovej a kyseliny stearovej (1952 - 1953). Od tejto doby bol najintenzívnejší vývoj získaný plynovou chromatografiou.
Jedným z variantov plynovej chromatografie je chromantografia, v ktorej sa má zlepšiť separáciu plynnej zmesi súčasne s pohybom pohyblivého fázového plynu, ovplyvňuje sorbent a oddelenú zmes s pohyblivou teplotou s určitým gradientom ( AA Zhukhovitsky a Sotr., 1951).
Znateľným príspevkom k rozvoju chromatografickej metódy predstavil mesto Schwab (Nemecko), ktorý bol zakladateľom ionomeničovej chromatografie (1937 - 1940). Dostala ďalší rozvoj v dielach sovietskych vedcov E.N. Gapona a TB GAPONA, ktorá uskutočnila chromatografickú separáciu zmesi iónov v roztoku (spolu s FM Shemyakin, 1947), a tiež vykonaná myšlienka možnosti chromatografickej separácie zmesi látok na základe rozdielu v rozpustnosti rozpustnosti (sedimentárna chromatografia, 1948).
Moderná etapa vo vývoji ionomeničovej chromatografie začala v roku 1975 po práci mesta Smallla, T. Stevens a W. Bauman (USA), v ktorom navrhli novú analytickú metódu nazvanú iónovou chromatografiou (možnosť pre vysoko efektívne iónový výmenný chromatografia s kondaktometrickou detekciou).
Vytvorenie spoločnosti "Perkin-Elmer" M. Golley (USA) kapilárneho variantu chromatografie (1956), v ktorom sa sorbent aplikuje na vnútorné steny kapilárnej trubice, čo umožňuje analyzovať mikrokolizmus viaczložkových zmesí.
Koncom 60. rokov. Zvýšený záujem o tekutú chromatografiu. Tam bola vysoko účinná kvapalinová chromatografia (HPLC). To bolo uľahčené vytvorením vysoko citlivých detektorov, nových selektívnych polymérových sorbentov, nových zariadení, ktoré umožní pracovať pri vysokých tlakoch. V súčasnosti HPLC zaujíma vedúcu pozíciu medzi inými chromatografickými metódami a implementovaný v rôznych verziách.
Chromatografia je spôsob separácie a stanovenie látok založených na distribúcii zložiek medzi oboma fázami-podšívkami a fixovanými. Pevná (stacionárna) fáza slúži na pevnú poréznu látku (často nazývanú sorbent) alebo kvapalný film aplikovaný na pevnú látku. Mobilná fáza je kvapalina alebo plyn prúdi cez pevnú fázu, niekedy pod tlakom. Zložky zmesi zmesi (jadro) spolu s pohyblivou fázou sa pohybujú pozdĺž stacionárnej fázy. Zvyčajne sa umiestni do sklenenej alebo kovovej trubice, nazývanej kolónu. V závislosti od interakčnej sily s sorbentovým povrchom (v dôsledku adsorpcie alebo akýmkoľvek iným mechanizmom) sa zložky pohybujú pozdĺž kolóny pri rôznych rýchlostiach. Niektoré komponenty zostanú v hornej vrstve sorbentu, iní, v menšej miere interakcii s sorbentom, budú v spodnej časti kolóny a niektoré opustia stĺpec spolu s pohyblivou fázou (takéto komponenty sú neplatené, a Ich doba chovu určuje reproduktory "mŕtveho času").
Vyskytuje sa teda rýchle oddelenie zložitých zmesí komponentov.
História Otvorenie:
Narodenie chromatografie
Vo večerných hodinách tohto dňa, na stretnutí biologického oddelenia Varšavskej spoločnosti prírodovedcov, asistent oddelenia anatómie a fyziológie rastlín Mikhail Semenoviča urobil správu "v novej kategórii adsorpčných javov a na použitie z nich na biochemickú analýzu. "
Bohužiaľ, M.S. Tsvet, byť na tvorbe botaniky, neocenila chemický analytický aspekt jeho otvorenia ako správne, a málo publikoval svoju prácu v chemických časopisoch. Následne to boli chemici, ktoré ocenili skutočnú škálu navrhovaných M.S. Farba chromatografickej metódy, ktorá sa stala najbežnejšou metódou analytickej chémie.
Treba zdôrazniť nasledujúce podrobnosti chromatografických metód: \\ t
1. Separácia je dynamická a akty sorpčného desorpcie zdieľaných zložiek sa opakujú. To spôsobuje výrazne vyššiu účinnosť chromatografických
oddelenie v porovnaní so statickými sorpčnými metódami a
extrakcie.
2. Počas oddelenia sa používajú rôzne druhy interakcie sorbátov a stacionárnych fáz: z čisto fyzickej na hemosorpciu.
To spôsobuje možnosť selektívneho oddelenia širokého rozsahu
3. Na oddelených látkach môžete aplikovať rôzne ďalšie polia (gravitačné, elektrické, magnetické atď.), Ktoré meniace podmienky separácie, rozširujú možnosti chromatografie.
4. Chromatografia je hybridný spôsob, ktorý kombinuje simultánnu separáciu a definíciu niekoľkých zložiek.
5. Chromatografia vám umožňuje riešiť analytické úlohy (separácia, identifikácia, definícia) a preparatívne (čistenie, výber, koncentrácia). Riešenie týchto úloh je možné kombinovať vykonaním v režime "Online".
Početné metódy sú klasifikované agregovaným stavom fáz, separačného mechanizmu a technikou separácie.
Chromatografické metódy sa líšia metódou vykonávania
separačný proces na prednej strane, rozhodujúci a eluent.
Iónová chromatografia
Iónová chromatografia je vysoko účinná kvapalinová chromatografia na oddeľovanie katiónov a aniónov na iónomeniče
nízka kapacita. Rozšírená iónová chromatografia
kvôli počtu jej výhod:
- schopnosť určiť veľký počet anorganických a
organické ióny, ako aj súčasne definujú katióny a
- Vysoká citlivosť stanovenia (až 1 ng / ml bez
predbežná koncentrácia;
- Vysoká selektivita a expresivita;
- malý objem analyzovanej vzorky (nie viac ako 2 ml vzorky);
- široká škála definovaných koncentrácií (od1 ng / ml do
- možnosť použitia rôznych detektorov a ich kombinácií, čo umožňuje poskytnúť selektivitu a malé časové definície;
- schopnosť plne automatizovať definíciu;
- V mnohých prípadoch úplná absencia predbežnej prípravy vzorky.
Zároveň, ako akákoľvek analytická metóda, iónová chromatografia nie je bez nedostatkov, ktoré možno pripísať:
- zložitosť syntézy iónomeničov, ktorá výrazne komplikuje
vývoj metódy;
- nižšia účinnosť separácie v porovnaní s HPLC v porovnaní s HPLC;
- potreba vysokej odolnosti proti korózii
chromatografický systém, najmä pri určovaní
katióny.
2.1 História vývoja:
Štúdium procesov výmeny iónov začala na začiatku XIX storočia. S pozorovaním týkajúcimi sa účinku pôd na chemické zloženie solových roztokov v kontakte s ním. Koncom 40. storočia Tompson poznamenal, že pôda absorbuje amoniak z vložených organických hnojív, príslušné experimenty uskutočnili špecialista ich Yorku D. Spence. Prvé výsledky experimentov D. Spence boli publikované G. Thompsonom v roku 1850. Článok poznamenáva, že "prvý objav vysokokvalitných vlastností pôdy môže ťažko zlyhať tak užitočné pre poľnohospodárstvo" a jeho posledná práca bola zverejnená E V roku 1852 a 1855.
2.3 Zásady separácie iónov v sorpčných procesoch
Ionomeničová chromatografia sa vzťahuje na chromatografiu s kvapalnou pevnou fázou, v ktorej je mobilná fáza kvapalina (eluent) a pevná fáza je tuhá látka (iónový výmenník). Spôsob ionomeničovej chromatografie je založený na dynamickom náhradnom procese iónov spojených s pevnou fázou, eluentové ióny vstupujúce do stĺpca. Oddelenie dochádza v dôsledku rôznej afinity pre iónovú výmenu iónov v zmesi, čo vedie k rôznym rýchlostiam ich pohybu pozdĺž kolóny.
Iónová chromatografia je variantom stĺpcovej ionomeničovej chromatografie.
Podľa odporúčaní JUPAK (1993) sú termíny iónové výmenu (IOC) a iónové (ich) chromatografia definované nasledovne. "Ionomeničová chromatografia je založená na rozdiele interakcií ionomeny pre jednotlivé analyzované látky. Ak sú ióny oddelené a môžu byť detegované pomocou detektora vodiča alebo nepriameho UV detekcie, potom sa nazýva iónová chromatografia."
Moderné (2005) Znenie: "Iónová chromatografia zahŕňa všetky vysoko výkonné kvapalinové chromatografické (HPLC) separáciu iónov v stĺpcoch v kombinácii s priamou detekciou v detektore prietoku a kvantitatívne spracovanie získaných analytických signálov." Táto definícia charakterizuje iónovú chromatografiu bez odkazu na separačný mechanizmus a spôsob detekcie, čím sa oddeľuje od klasickej výmeny iónov.
Nasledujúce zásady separácie platia v iónovom chromatografii:
Iónová výmena.
Vzdelávanie iónových párov.
Ióny vylúčenia.
Ion
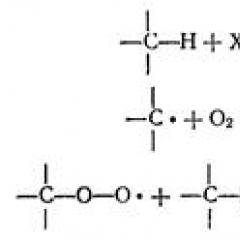
Ióna Exchange je reverzibilná heterogénna reakcia ekvivalentných ionizačných iónov v ionátovom fáze (protiióny), eluentových odborov. Anti -ions sú držané funkčnými skupinami ionetov na úkor elektrostatických síl. V súlade s katiónou chromatografiou sú tieto skupiny skupiny sulfónových kyselín; V prípade aniónovej chromatografie - kvartérne amóniové dôvody. Na obr. 1 ukazuje schému procesu výmeny katiónov a aniónov. Ióny stanovenej látky sú označené ako eluentové ióny súťažiace s nimi pre výmenné centrá - E.

Obr. 1. iónová výmena katiónov (A +) a aniónov (A-) na eluentových iónoch (E + alebo E-) za účasti katiónového výmenníka obsahujúcej funkčné sulfo skupiny - SO3-, a aniónový výmenník (kvartérna amóniová báza skupiny -n + R3).
Vzdelávanie iónu par
Na implementáciu tohto separačného mechanizmu sa používajú iónové reagencie, ktoré sa pridávajú do elučného roztoku. Takéto činidlá sú aniónové alebo katiónové povrchovo aktívne látky, napríklad alkylsulfónové kyseliny alebo tetraalklamámové soli.
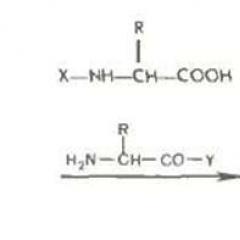
Spolu s opačne účtovanými ion-definovanými iónmi, ióny tohto iónového reagencie tvoria nestabilný iónový pár, ktorý sa môže držať na pevnej fáze v dôsledku intermolekulárnych interakcií. Separácia sa uskutočňuje v dôsledku rozdielu v konštante tvorby iónových párov a stupňov ich adsorpcie na sorbentovej matrici. Na obr. 2 znázorňuje statický iónový výmenný model v iónovej chromatografii po adsorpcii činidla na pevnú fázu. Táto separačná zásada sa používa pre anióny a katióny.

Obr. 2.. Iongemový model v iónovej parnej chromatografii.
Iónové vylúčenie
Ionecluzná chromatografia (IEX). V podstate sa používa na oddelenie slabých kyselín alebo báz. Najväčšia hodnota IEX musí určiť karboxylové a aminokyseliny, fenoly, sacharidy.
Na obr. 3 ukazuje princíp separácie pomocou IEX na príklad kyseliny R-COOH.
Obr. 3. R-COOH Karboxylová separačná schéma s použitím ionoecklusovej chromatografie.

V ionoeckskoluzionovej chromatografii ako pevná fáza sa často používa plnohodnotný sulfted katiónový výmenník, obsahujúci ión-voda (protiióny). V vodnom roztoku eluentov sú hydratované skupiny kyseliny sulfónovej kyseliny IONIS. Hydrátový plášť je obmedzený na imaginárnu negatívne nabitú membránu (Donnan membrána). Membrána je priepustná len pre neexpatované molekuly (napríklad voda).
Organické karboxylové kyseliny sa môžu oddeliť, ak sa ako eluent používajú silné minerálne kyseliny. V dôsledku nízkych hodnôt kyslých konštánt sú prítomné v takýchto roztokoch v nekalej forme. Tieto formy môžu prejsť cez membránu Donnna a adsorbované na pevnej fáze.
Pošlite svoju dobrú prácu v znalostnej báze je jednoduchá. Použite nižšie uvedený formulár
Študenti, absolventi študenti, mladí vedci, ktorí používajú vedomostnú základňu vo svojich štúdiách a práce, budú vám veľmi vďační.
pridané http://www.allbest.ru.
1. História otvárania a vývoja chromatografie
2. Základné ustanovenia
3. Klasifikácia metód chromatografickej analýzy
4. Adsorpčná chromatografia. Chromatografia na tenkej vrstve
4.1 Technika experimentu v tenkovrstvovej chromatografii
5. Plynová chromatografia
5.1 Plynová adsorpčná chromatografia
5.2 Plynová chromatografia
6. Distribučná chromatografia. Papierová chromatografia
7. Chromatografia sedimentov
7.1 Klasifikácia metód sedimentárnej chromatografie na technike experimentu
7.2 Chromatografia sedimentov na papieri
8. ION Zmenáreň Chromatografia
Záver
Bibliografia
1. HistóriaObjavy a vývoj chromatografie
Chromatografia je ruský vedecká, botanika a fyzikálnumochemista Michail Semenovičská farba.
Objav chromatografie sa vzťahuje na čas dokončenia práce na diplomovej práci v Petrohrade (1900 - 1902) a prvé obdobie práce vo Varšave (1902 - 1903). Skúmanie pigmentov rastlín, farba prešla roztokom zmesi veľmi málo líši sa vo farbe pigmentov cez trubicu naplnenú adsorbentným práškovým uhličitanom vápenatým a potom sa potom premyje adsorbent s čistým rozpúšťadlom. Samostatné zložky zmesi boli rozdelené a tvorené farebnými pruhmi. Podľa modernej terminológie sa farba objavila vývojový variant chromatografie (vyvíjanie kvapalnej adsorpčnej chromatografie). Hlavné výsledky výskumu o vývoji chromatografie, ktoré vytvorili ho. Farba načrtnutá v knihe "Chromophyls v rastlinnom a živočíšnom svete" (1910), čo je jeho doktorandská dizertačná práca. Chromatografia plynu sedimentárna iónová výmena
Farba široko používa chromatografickú metódu nielen na separáciu zmesi a vytvorenie IT multicomponency, ale aj pre kvantitatívnu analýzu, na tento účel rozbil sklenený stĺpec a narezal adsorpčnú kolónu na vrstvy. Farba vyvinula zariadenie na kvapalinovú chromatografiu, pričom prvýkrát vykonala chromatografické procesy za zníženého tlaku (čerpanie) a pri určitom pretlaku vyvinuté odporúčania na prípravu účinných stĺpcov. Okrem toho predstavil mnoho základných pojmov a podmienok novej metódy, ako napríklad "chromatografia", "prejav", "posunutie", "chromatogram" atď.
Chromatografia sa najprv použila veľmi zriedka, jeho skryté obdobie trvalo asi 20 rokov, počas ktorého sa objavil len veľmi malý počet správ o rôznych aplikáciách metódy. A len v roku 1931, R. Kunu (Nemecko) A. Winterstein (Nemecko) a E. LEDTERRE (Francúzsko), ktorí pracovali v chemickom laboratóriu (LED R. KUN), Ústavu cisára Wilhelma na lekárskom výskume v Heidelbergu, Podarilo sa prideliť tento spôsob A - a B-karotén zo surového karoténu a tým demonštrovať hodnotu farebného otvoru.
Dôležitým stupňom vývoja chromatografie bol objav sovietskych vedcov N.A. Izmailov a M.S. Schreiber metóda chromatografie v tenkej vrstve (1938), ktorá umožňuje analýzu mikrokolizmom látky.
Ďalším dôležitým krokom bol objav A. Martin a R. Sing (Anglicko) variantu kvapalnej distribučnej chromatografie na príklade separácie acetylových derivátov aminokyselín na kolóne naplnenej silikagélom, nasýteným vodou, s použitím chloroformu ako rozpúšťadlo (1940). Zároveň sa poznamenalo, že ako mobilná fáza môže byť použitá nielen kvapalina, ale aj plyn. O niekoľko rokov neskôr boli títo vedci navrhnutí na oddelenie derivátov aminokyselín na zvlhčenú vodou s butanolom ako mobilnej fázy. Implementovali tiež prvý dvojrozmerný separačný systém. Na otvorenie distribučnej verzie chromatografie, Martin a Sping dostal Nobelovu cenu v chémii. (1952). Ďalej, Martin a A. James vykonávali variant rozvodnej chromatografie plynu, čím sa oddelila zmes na zmiešanej sorbente z DS-550 silikónovej a kyseliny stearovej (1952 - 1953). Od tejto doby bol najintenzívnejší vývoj získaný plynovou chromatografiou.
Jedným z variantov plynovej chromatografie je chromantografia, v ktorej sa má zlepšiť separáciu plynnej zmesi súčasne s pohybom pohyblivého fázového plynu, ovplyvňuje sorbent a oddelenú zmes s pohyblivou teplotou s určitým gradientom ( AA Zhukhovitsky a Sotr., 1951).
Znateľným príspevkom k rozvoju chromatografickej metódy predstavil mesto Schwab (Nemecko), ktorý bol zakladateľom ionomeničovej chromatografie (1937 - 1940). Dostala ďalší rozvoj v dielach sovietskych vedcov E.N. Gapona a TB GAPONA, ktorá uskutočnila chromatografickú separáciu zmesi iónov v roztoku (spolu s FM Shemyakin, 1947), a tiež vykonaná myšlienka možnosti chromatografickej separácie zmesi látok na základe rozdielu v rozpustnosti rozpustnosti (sedimentárna chromatografia, 1948).
Moderná etapa vo vývoji ionomeničovej chromatografie začala v roku 1975 po práci mesta Smallla, T. Stevens a W. Bauman (USA), v ktorom navrhli novú analytickú metódu nazvanú iónovou chromatografiou (možnosť pre vysoko efektívne iónový výmenný chromatografia s kondaktometrickou detekciou).
Vytvorenie spoločnosti "Perkin-Elmer" M. Golley (USA) kapilárneho variantu chromatografie (1956), v ktorom sa sorbent aplikuje na vnútorné steny kapilárnej trubice, čo umožňuje analyzovať mikrokolizmus viaczložkových zmesí.
Koncom 60. rokov. Zvýšený záujem o tekutú chromatografiu. Tam bola vysoko účinná kvapalinová chromatografia (HPLC). To bolo uľahčené vytvorením vysoko citlivých detektorov, nových selektívnych polymérových sorbentov, nových zariadení, ktoré umožní pracovať pri vysokých tlakoch. V súčasnosti HPLC zaujíma vedúcu pozíciu medzi inými chromatografickými metódami a implementovaný v rôznych verziách.
2. Základné ustanovenia
Chromatografia je spôsob separácie a stanovenia látok založených na distribúcii zložiek medzi oboma fázami - pohyblivými a fixnými. Pevná (stacionárna) fáza slúži na pevnú poréznu látku (často nazývanú sorbent) alebo kvapalný film aplikovaný na pevnú látku. Mobilná fáza je kvapalina alebo plyn prúdi cez pevnú fázu, niekedy pod tlakom. Zložky zmesi zmesi (jadro) spolu s pohyblivou fázou sa pohybujú pozdĺž stacionárnej fázy. Zvyčajne sa umiestni do sklenenej alebo kovovej trubice, nazývanej kolónu. V závislosti od interakčnej sily s sorbentovým povrchom (v dôsledku adsorpcie alebo akýmkoľvek iným mechanizmom) sa zložky pohybujú pozdĺž kolóny pri rôznych rýchlostiach. Niektoré komponenty zostanú v hornej vrstve sorbentu, iní, v menšej miere interakcii s sorbentom, budú v spodnej časti kolóny a niektoré opustia stĺpec spolu s pohyblivou fázou (takéto komponenty sú neplatené, a Ich doba chovu určuje reproduktory "mŕtveho času"). Vyskytuje sa teda rýchle oddelenie zložitých zmesí komponentov. Treba zdôrazniť nasledujúce podrobnosti chromatografických metód: \\ t
1. Separácia je dynamická a akty sorpčného desorpcie zdieľaných zložiek sa opakujú. To spôsobuje výrazne vyššiu účinnosť chromatografickej separácie v porovnaní so statickými metódami sorpcie a extrakcie.
2. Počas oddelenia sa používajú rôzne druhy interakcie sorbátov a stacionárnych fáz: z čisto fyzickej na hemosorpciu. To spôsobuje možnosť selektívneho oddelenia širokého kruhu látok.
3. Na oddelených látkach môžete aplikovať rôzne ďalšie polia (gravitačné, elektrické, magnetické atď.), Ktoré meniace podmienky separácie, rozširujú možnosti chromatografie.
4. Chromatografia je hybridný spôsob, ktorý kombinuje simultánnu separáciu a definíciu niekoľkých zložiek.
5. Chromatografia vám umožňuje riešiť analytické úlohy (separácia, identifikácia, definícia) a preparatívne (čistenie, výber, koncentrácia). Riešenie týchto úloh je možné kombinovať vykonaním v režime "On Line".
6. Početné metódy sú klasifikované agregovaným stavom fáz, separačný mechanizmus a separačná technika. Chromatografické metódy sa líšia spôsobu vykonávania separačného procesu na prednú, tégliku a eluent.
3. Klasifikácia chromatografických metód analýzy
Formifikácie chromatografických metód sú založené na princípoch, ktoré berú do úvahy nasledujúce rôzne znaky procesu separácie: \\ t
* Rozdiely v súhrnnom stave fáz použitého chromatografického systému;
* Rozdiely v povahe interakcií oddelených látok s pevnou fázou;
* Experimentálne rozdiely v spôsoboch procesu chromatografickej separácie.
V tabuľkách 1? 3 ukazuje základné varianty klasifikácie známych chromatografických metód.
Vzhľadom k tomu, povaha interakcií oddelených zlúčenín s fázami rôznych chromatografických systémov sa môže veľmi líšiť, nie sú takmer žiadne objekty, pre separáciu, ktoré by nebolo možné nájsť vhodnú pevnú fázu (pevné alebo kvapalné) a valcovacie rozpúšťadlo systémy. Rozsah základných variantov chromatografie v závislosti od molekulovej hmotnosti zlúčenín podľa štúdia je uvedený v tabuľke. štyri.
4. Adsorpčná chromatografia. Chromatografia na tenkej vrstve
Jednou z najbežnejších adsorpčných chromatografických techník je tenkovrstvová chromatografia (TLC) - typ rovinnej chromatografie, pri ktorom sa adsorbent používa ako tenká vrstva na doske.
Princíp a základné pojmy metódy TLC. Na čistej plochom povrchu (doska skla, kovu, plastov), \u200b\u200bjedným alebo iným spôsobom, je aplikovaná tenká vrstva sorbentu, ktorá je najčastejšie upevnená na povrchu dosky. Rozmery dosky môžu byť odlišné (dĺžka a šírka - od 5 do 50 cm, hoci nie je potrebné). Na povrchu dosky, opatrne, aby nedošlo k poškodeniu sorbentovej vrstvy, načrtnuté (napríklad ceruzku) štartovacieho vedenia (vo vzdialenosti 2-3 cm od spodného okraja dosky) a čiaru Rozpúšťadlová povrchová úprava.
Schéma oddelenia komponentov A a v metóde TLC
Na štartovacej čiare sa platne aplikuje (mikroprchom, kapilárnou) vzorkou - malé množstvo tekutiny obsahujúcej zmes oddeliteľných látok, napríklad dvoch látok A a B vo vhodnom rozpúšťadle. Rozpúšťadlo je možné odpariť, potom sa doska ponorí do chromatografickej komory v kvapalnej fáze PF, ktorá je špeciálne vybraným rozpúšťadlom alebo zmesou rozpúšťadiel pre daný prípad. Pod pôsobením kapilárnych síl PF spontánne sa pohybujú pozdĺž NF z východiskovej čiary do rady prednej časti rozpúšťadla, ktorá sa stará s nimi komponenty A a vo vzorkách, ktoré sa pohybujú pri rôznych rýchlostiach. V tomto prípade je afinita komponentu A k NF je menšia afinita pre rovnakú fázu zložky B, takže zložka A sa pohybuje rýchlejšie ako zložka B. po dosiahnutí pohyblivého fázy (rozpúšťadla) rozpúšťadlovej čiary, Chromatografia sa preruší, doska sa odstráni z chromatografickej komory, suší sa vo vzduchu a určuje polohu škvŕn látok A a na povrchu dosky. Škvrny (zóny) majú zvyčajne oválny alebo okrúhly tvar. V posudzovanom prípade sa zložka škvrny a presunul z štartovej čiary do vzdialenosti l. A. , spot komponent - na diaľku l. Va rozpúšťadlo prechádzalo cez vzdialenosť L..
Niekedy súčasne s aplikáciou vzoriek oddelených látok na štartovacej čiare sa uplatňujú malé množstvá štandardu štandardu, ako aj svedkovia látok (tie, ktoré sú údajne obsiahnuté v analyzovanej vzorke).
Ak chcete charakterizovať spoločné komponenty, RF mobilita (alebo RF faktor) je zavedený v systéme:
R. f.\u003d V. 1 / V. E.\u003d (L. 1 / T) / (l / t) \u003d l 1 / L. ,
kde V. 1 = l. 1 / t. a V. E.= L./ t. - v súlade s tým rýchlosť pohybu i.- komponent a rozpúšťadlo E; l. 1 aL. - cesta i.- komponent a rozpúšťadlo, T je čas potrebný na presunutie rozpúšťadla zo štartovacieho vedenia k prednej čiare rozpúšťadla. Vzdialenosť l. 1 stlačte zo štartovacieho vedenia do stredu miesta príslušného komponentu.
Zvyčajne sa koeficient mobility spočíva v redistribúcii R. f. =0 - 1. Optimálna hodnota je 0,3 až 0,7, chromatografické podmienky sú vybrané tak, aby hodnota Rf sa líši od nuly a jednotiek.
Koeficient mobility je dôležitou charakteristikou systému Sorbent Sorbate. Pre reprodukovateľné a prísne podmienky chromatografie R. f. = const.
RF mobilita koeficient závisí od viacerých faktorov: povaha a kvalita rozpúšťadla, jeho čistota; Príroda a kvalita sorbentu (tenká vrstva), rovnomernosť jej zŕn, hrúbka vrstvy; činnosť sorbentu (obsah v IT vlhkosti); Techniky experimentu (hmotnostné vzorky, dĺžka mesiaca rozpúšťadla); Experimentovacia zručnosť atď. Costancy reprodukcie všetkých týchto parametrov v praxi je niekedy ťažké. Na vyrovnanie vplyvu podmienok procesu je zavedený faktor relatívnej mobility Rs..
Rs \u003d l / l umenie\u003d R. f./ R. f ( umenie ) ,
kde R. f. = l./ L.; R. f. (St)= l. umenie/ L.; l. cm. - vzdialenosť od štartovej čiary do stredu štandardného miesta.
Relatívny koeficient mobility RS je objektívnejšou charakteristikou mobility látky ako koeficient mobility r f.
Ako štandard je takáto látka často zvolená, pre ktorú v týchto podmienkach r f? 0,5. V chemickej povahe sa štandard vyberie v blízkosti oddelených látok. Pomocou štandardu je hodnota Rs zvyčajne leží v Rs \u003d 0,1-10, optimálne limity sú približne 0,5-1.
Pre spoľahlivejšiu identifikáciu zdieľaných zložiek používajú "svedkov" - referenčné látky, ktorých prítomnosť sa predpokladá v analyzovanej vzorke. Ak Rf \u003d Rf (Svid), kde Rf a Rf (Svid) - respektíve, koeficienty mobility tejto zložky a svedok, potom môžu s najväčšou pravdepodobnosťou predpokladať, že testovaná látka je prítomná v chromatografickej zmesi.
Na charakterizáciu oddelenia dvoch zložiek A a v týchto podmienkach sa zavádza stupeň (kritérium) separácie R (A / B): \\ t
R (a / b) \u003d d l.(\u003d 2d l. ,
kde D. l. - vzdialenosť medzi strediskami spotov komponentov A a B; A (a) a (b) - resp. Priemery miest A a B na chromatograme.
Čím väčšia je hodnota R (A / B), jasnejšie, škvrny zložiek A a B sú oddelené na chromatograme.
Ak chcete odhadnúť selektivitu separácie dvoch látok A a B, použite separačný koeficient ale:
a \u003d.l. B. / l. A.
Ak a \u003d 1,tieto komponenty A a B nie sú rozdelené.
Určiť stupeň separácie R (A / B) komponentov A a V.
4.1 Experimentálna technika v tenkej vrstve chromatografie:
ale) Vzorka. Analyzovaná kvapalná vzorka sa aplikuje na riadok štartu pomocou kapilárnej, mikro-hovno, mikropipety, opatrne dotýkajúce sa sorbentnej vrstvy (priemer škvrny na štartovacej čiare je zvyčajne od jedného do niekoľkých milimetrov). Ak sa na štartovaciu čiaru aplikuje niekoľko vzoriek, potom vzdialenosť medzi škvrnami vzoriek na štartovacej čiare by nemala byť menšia ako 2 cm. Používajú sa koncentrované roztoky. Spoty sa sušia vo vzduchu, po ktorej sa uskutoční chromatografia.
b) Vývoj chromatogramu (chromatografia).Spôsob sa uskutočňuje v uzavretých chromatografických komorách nasýtených pármi rozpúšťadiel, ktoré sa používajú ako PF, napríklad v sklenenej nádobe, na ktorej sa vzťahujú na vrchole veka.
V závislosti od smeru pohybu sa PF rozlišuje stúpajúci klesajúci a horizontálny chromatografia.
Vo forme vzostupnej chromatografie sa používajú len doštičky s pevnou sorbentnou vrstvou. PF sa naleje na spodnú časť komory (keďže druhé, sklenené chemické poháre vhodnej veľkosti môže byť použitá so skleneným vekom), chromatografická doska sa umiestni vertikálne alebo šikmo do komory tak, aby PF vrstva na dne Fotoaparát zvlhčuje spodnú časť dosky (pod štartovacou čiarou o 1,5 - 2 cm). PF sa pohybuje v dôsledku pôsobenia kapilárnych síl z zdola nahor (proti gravitácii) relatívne pomaly.
V klesajúcej variante chromatografie, platia aj platne s pevnou vrstvou. PF je privádzaný zhora a pohybuje sa nadol pozdĺž dosky sorbentnej vrstvy. Gravitačná sila urýchľuje pohyb PF. Toto uskutočnenie je implementované pri analýze zmesí obsahujúcich zložky, pomaly sa pohybuje s PF.
V uskutočnení horizontálnej chromatografie je doska umiestnená horizontálne. Môžete použiť obdĺžnikové alebo okrúhle dosky. Pri aplikácii kruhových dosiek (kruhový variant horizontálnej chromatografie) je štartovacia čiara označená ako kruh vhodného polomer (~ 1,5-2 cm), ktoré sa aplikujú vzorky. V strede okrúhlej dosky je otvor narezaný, do ktorého je knôt vložený do napájania PF. Ten sa pohybuje pozdĺž sorbentovej vrstvy zo stredu kruhu k jeho periférii. Chromatografia sa uskutočňuje v uzavretej komore - exsikátor alebo v Petriho variča. S kruhovou verziou, môžete súčasne analyzovať až niekoľko desiatok vzoriek.
V metódach TLC sa používa jednorozmerné, dvojrozmerné, viacnásobné (re-), krok chromatografie.
V jednorazovej chromatografii sa analýza vykonáva bez zmeny smeru pohybu PF. Táto metóda je najbežnejšia.
Dvojrozmerná chromatografia sa zvyčajne používa na analýzu komplexných zmesí (proteíny, aminokyseliny atď.), Zmes sa najprv uskutočňuje pomocou prvého PF1. Chromatogram sa získajú škvrny nie jednotlivé látky a zmesi niekoľkých neoddeliteľných zložiek. Potom sa cez tieto škvrny uskutoční nová štartová čiara, doska sa zapne 90 ° a je chromatografovaný znova, ale už s druhým PF2, snaha o konečne rozdeliť škvrny zmesami na škvrna jednotlivých zložiek.
Ak je doska štvorcová, potom sa vzorka aplikuje na uhlopriečku tohto štvorca v blízkosti jeho dolného rohu. Niekedy sa dvojrozmerná chromatografia uskutočňuje s rovnakým PF na štvorcovej doske.
Schéma ilustrujúca princíp dvojdimenzionálnej chromatografie:
a - chromatogram získaný z PF1;
b - chromatogram získaný z PF2
Vo viacnásobnom (re-) chromatografii sa proces uskutočňuje niekoľkokrát postupne postupne od rovnakého PF (zakaždým - po ďalšom sušení) až do požadovaného oddelenia škvŕn komponentov zmesi (zvyčajne - nie viac ako trikrát).
V prípade krokovej chromatografie sa proces uskutočňuje s rovnakou doskou postupne pomocou prikaždým novým PF, až kým sa nedosiahne jasné oddelenie škvŕn.
v) Dekódovanie chromatogramov. Ak sú škvrny na chromatograme natreté, po vysušení dosiek, určiť vzdialenosť od začiatočnej vedenia do stredu každého miesta a vypočítajte koeficienty mobility. Ak zloženie analyzovanej vzorky pozostáva z bezfarebných látok, čo dáva neinfarovaný, t.j. Vizuálne nie identifikované miesta na chromatograme, musíte minúť detekcia tieto miesta, pre ktoré chromatogram Šou.
Najčastejšie metódy detekcie sú opísané nižšie.
Ožarovanie ultrafialovým svetlom.Používa sa na detekciu fluorescenčných zlúčenín (spoty žiariace počas ožarovania UV žiarivej dosky) alebo petrolevaskulárnych látok, ale pomocou sorbentu s fluorescenčným indikátorom (sorbent svieti, škvrny nebudú svietiť). Tak zistené, napríklad alkaloidy, antibiotiká, vitamíny a iné liečivá.
Tepelné spracovanie.Doska sa sušila po chromatografii, jemne zahrievaná (až do ~ 200 ° C), zabránenie stmavnuce sorbentu samotného (napríklad, keď tenká vrstva sorbentu obsahuje škrob). Zároveň sa škvrny zvyčajne prejavujú vo forme hnedých zón (v dôsledku čiastočnej termolýzy organických zložiek).
Chemické spracovanie.Často vykazujú chromatogramy, spracúvajú ich s činidlami, ktoré tvoria farebné zlúčeniny so zdieľanými zložkami zmesí. Na tieto účely sa používajú rôzne reagencie: dvojica jódu, amoniaku, brómu, oxidu siričitého, sírovodík, špeciálne pripravené roztoky, ktoré sú ošetrené platne. Aplikujte univerzálne aj selektívne činidlá (koncepcia "universal" je dostatočne podmienečne).
Univerzálny reagentamimogoot slúži, napríklad, koncentrovaná kyselina sírová (pri zahrievaní, je stmavnutie organických zlúčenín), kyslý vodný roztok manganistanu draselného (zóna sa pozoroval vo forme hnedých škvŕn na fialovej sorbentné pozadie), roztoku Kyselina fosforu-molybdén počas zahrievania (modré škvrny sa objavujú na žltom pozadí) atď.
Ako selektívne použitie napríklad činidlo Dragendorf; Zimmermanové činidlo; vodný roztok amónneho sulfátu medi (10% CUSO 4, 2% v amoniaku); Zmes ninhydrínu C9H4O3H20CHU s etanolom a kyselinou octovou.
Reagent Dragandorf je roztokom hlavného dusičnanu Bondo 3, KJ iodid draselný a kyselina octová vo vode. Používa sa na určenie amínov, alkaloidov, steroidov.
Zimmermanové činidlo sa pripraví spracovaním roztoku alkalického roztoku KOH2% etanolu dinitrobenzénu, po ktorom nasleduje zahrievanie zmesi pri teplote ~ 70-100 ° C. Použiť na detekciu steroidov.
S pomocou Ningidrínu sa detegujú škvrny aminokyselín, proteínov a iných pripojení.
Používajú sa iné spôsoby detekcie miest. Napríklad ich rádioaktivita sa meria, ak niektoré oddelené zložky rádioaktívneho sú buď zavedené špeciálne prísady rádioaktívnych izotopov prvkov, ktoré sú súčasťou oddelených zložiek zmesi.
Po detekovaní bodov na chromatograme sú identifikované, t.j. Je určený, ktorým zlúčenina zodpovedá tomuto alebo toto miesto. Na tento účel sa najčastejšie používajú referenčné miesta "svedkov". Niekedy sú škvrny identifikované veľkosťou mobility koeficientov Rf, v porovnaní s hodnotami RF známych pre tieto stavy. Takáto identifikácia Rf je však často predbežná.
Farba fluorescenčných škvŕn sa tiež používa na účely identifikácie, pretože rôzne zlúčeniny sú fluorescenčné žiarením rôznych vlnových dĺžok (rôzne farby).
S chemickou detekciou škvŕn, selektívne reagencie dávajú maľované škvrny so zlúčeninami určitej povahy, ktorá sa používa aj na účely identifikácie.
Pomocou metódy TLC môžete nielen otvoriť, ale aj kvantifikovať obsah komponentov v zmesiach. Na tento účel sa to analyzujú škvrny na samotných chromatogram, alebo oddelené zložky z chromatogramu sa odstránia jedným alebo iným spôsobom (extrakcia, elúcia vhodnými rozpúšťadlami).
Pri analýze škvrny znamenajú existenciu určitého spojenia medzi oblasťou spotov a obsahom tejto látky (napríklad prítomnosť proporcionálnej alebo lineárnej závislosti), ktorá je stanovená metódou konštrukcie maturitného grafu, meranie Spoty "svedkov" spotov so známym obsahom analyzovaného komponentu.
Niekedy porovnávajú intenzitu farby škvŕn, verí, že intenzita farebných škvŕn je úmerná počtu tejto lakovanej zložky. Na meranie intenzity sa používajú rôzne techniky.
Pri demontáži oddelených zložiek z chromatogramu sa získa roztok obsahujúci túto zložku. Ten sa potom stanoví jedným alebo inou analytickou metódou.
Relatívna chyba kvantitatívneho stanovenia látky TLC je 5-10%.
TLC je liektický spôsob a je široko používaný na analýzu a kontrolu kvality rôznych liekov.
5. Plynová chromatografia
V plynovej chromatografii (GC) sa ako mobilná fáza používa inertný plyn (dusík, hélia, vodík), nazývaný nosič plynu. Vzorka sa privádza vo forme pary, fixná fáza slúži alebo tuhá látka - sorbent (plyn-adsorpčná chromatografia) alebo s vysokou teplotou varu aplikovanej tenkou vrstvou na pevnom nosiči (plynová chromatografia). Zvážte možnosť plynovej chromatografie (GLC). Kizelgur (diatómis) sa používa ako nosič - použije sa typ hydratovaného silikagélu, ktorý sa často lieči činidlami, ktoré prekladajú skupiny SI-OH v skupine SI-O-SI (CH3) 3, čo zvyšuje inertnosť dopravca s ohľadom na rozpúšťadlá. Jedná sa napríklad nosiče "chromozorb w" a "Gasohromq". Okrem toho sa používajú sklenené microsisus, teflón a iné materiály.
5.1 Gaza- adsorpčná chromatografia
Zvláštnosť spôsobu chromatografie plynovej čerpadla (GA) je, že ako fixná fáza sa používajú adsorbenty s vysokým špecifickým povrchom (10--1000 m 2 g-1) a distribúcia látok medzi pevnými a pohyblivými fázami je určený adsorpčným procesom. Adsorpcia molekúl z plynnej fázy, t.j. Koncentruje sa na povrch separácie pevných a plynných fáz, dochádza v dôsledku intermolekulárnych interakcií (disperzia, orientačná, indukcia), ktorá má elektrostatickú povahu. Je možné, tvorba vodíkových väzieb a prínos tohto typu interakcie do zadržaných objemov sa významne zníži s zvyšujúcou sa teplotou.
Pre analytickú prax je dôležité, aby sa pri konštantnej teplote, množstvo adsorbovanej látky na povrchu S S S bola úmerná koncentrácii tejto látky v plynnej fáze s M:
C. s. = kc. m. (1)
tí. takže distribúcia nastala v súlade s lineárnou izotermou adsorpcie (do - konštantná). V tomto prípade sa každá zložka pohybuje pozdĺž kolóny s konštantnou rýchlosťou, nezávisle od jej koncentrácie. Separácia látok je spôsobené rôznymi rýchlosťami ich pohybu. Preto je výber adsorbentného, \u200b\u200bplochy a povahy povrchu, z ktorých určuje selektivitu (separácia) pri danej teplote, je mimoriadne dôležité v medzerách.
Teplo adsorpcie klesá so zvyšujúcou sa teplotou DH / T.Z ktorej detekcie závisí a teda t. R. . Používa sa v praxi analýzy. Ak sú zlúčeniny oddelené vysoko rozdielnym volatilitou pri konštantnej teplote, potom nízko varené látky sa rýchlo eluujú, vysoko varu má väčší čas, ich píky na chromatograme budú nižšie a širšie, analýza trvá veľa času. Ak v procese chromatografie zvýšiť teplotu kolóny s konštantnou rýchlosťou (programovanie teploty), potom sa rovnomerne umiestnia vrcholy blízke šírkou na chromatograme.
Ako adsorbenty pre GI, aktívne uhlie, silikagély, porézne sklo, sa používa hlavne oxid hlinitý. Nehomogenity povrchu aktívnych adsorbentov je spôsobená hlavnou nevýhodou metód GAH a nemožnosti určovania vysoko adsorbovaných polárnych molekúl. Na geometricky a chemicky homogénnych makroporéznych adsorbentoch je však možné analyzovať zmesi silnej polárnych látok. V posledných rokoch, adsorbenty v nedávno produkujú adsorbenty s viac alebo menej homogénnym povrchom, ako sú porézne polyméry, makroporézne kremičité gély (satlohrom, zasiahnuté, sprej), porézne okuliare, zeolity.
Najrozšírenejším spôsobom chromatografie plynového čerpadla sa používa na analýzu zmesí plynov a uhľovodíkov s nízkym obsahom varu, ktoré neobsahujú aktívne funkčné skupiny. Adsorpčné izotermy takýchto molekúl sú blízko lineárneho. Napríklad na separáciu 2, N2, CO, CH4, CO 2 úspešne používa CLY. Teplota stĺpca je naprogramovaná tak, aby sa znížila čas analýzy znížením TR s vysokými vriacami. Na molekulárnych sints - vysoko farmaceutické prírodné alebo syntetické kryštalické materiály, ktoré majú všetky póry, ktoré majú približne rovnaké rozmery (0,4 až 1,5 nm), - môžu byť rozdelené vodíkmi izotopov. Sorbenty, nazývané lovci, sa používajú na oddelenie hydridov kovov (GE, as, SN, SB). Metóda GA na stĺpcoch s poréznymi polymérnymi sorbentmi alebo molekulovými veľkosťami uhlíka je najrýchlejší a najvhodnejší spôsob, ako určiť vodu v anorganických a organických materiáloch, napríklad v rozpúšťadlách.
5.2 Gaza- kvapalná chromatografia
V analytickej praxi sa častejšie používa metóda plynovej chromatografie (GLC). Je to spôsobené extrémnou rozmanitosťou kvapalných fixných fáz, čo uľahčuje výber selektívnej fázy tejto analýzy s linearitou distribučných izoterms v širšom koncentračnej oblasti, ktorá vám umožní pracovať s veľkými vzorkami a ľahko získať reprodukovateľné stĺpce.
Mechanizmus distribúcie zložiek medzi nosičom a fixnou kvapalnou fázou je založený na ich rozpustení v kvapalnej fáze. Selektivita závisí od dvoch faktorov: parná elasticita určenej látky a jej koeficient aktivít v kvapalnej fáze. Podľa zákona Raoula pri rozpustení elasticity pary látky nad roztokom p. \\ t i. priamo úmerné koeficient aktivity g molárnej frakcie N. i. v roztoku a tlaku pary čistej látky R ° i. Pri tejto teplote:
p \u003d n i p ° I (2)
Keďže koncentrácia I-TH komponentu v rovnovážnej parnej fáze je určená jeho čiastkovým tlakom, môžete to prijať
P i ~ c m a n i ~ c s
a koeficient selektivity:
Tak, tým nižšia teplota varu látky (Väčšia p 0 I), tým slabšia je udržiavaná v chromatografickom kolóne.
Ak je bod varu látok rovnaký, potom sa rozdiely v interakcii s pevnou kvapalnou fázou sa používajú na ich oddelenie: tým silnejšie je interakcia, tým menej koeficient aktivity a retencia.
Pevné kvapalné fázy . Aby ste zabezpečili selektivitu stĺpca, je dôležité správne vybrať pevnú kvapalnú fázu. Táto fáza by mala byť dobrým rozpúšťadlom pre zložky zmesi (ak je rozpustnosť malá, zložky sa rozprestierajú z kolóny veľmi rýchlo), neprchavé (tak, aby sa neodparovali pri prevádzkovej teplote stĺpca), chemicky inertné, musia Majú miernu viskozitu (inak difúzny proces spomaľuje) a keď sa aplikuje na nosič, aby vytvoril jednotný film, je s ním pevne spojený. Separačná kapacita pevnej fázy pre zložky tejto vzorky by mala byť maximálna.
Kvapalné fázy troch typov sa rozlišujú: nepolárne (nasýtené uhľovodíky, atď.), Mierne polárne (estery, nitrily atď.) A polárne (polyglykoly, hydroxylamia atď.).
Poznanie vlastností pevnej kvapalnej fázy a povahy oddeliteľných látok, ako je trieda, štruktúra, je možné rýchlo vybrať selektívnu kvapalnú fázu na oddelenie tejto zmesi. Treba mať na pamäti, že doba chovu zložiek bude prijateľná na analýzu, ak je polarita stacionárnej fázy a látka analyzovanej vzorky blízko. Pre rozpustené látky s blízkou polaritou, elučný poriadok zvyčajne koreluje s teplotou varu, a ak je teplotný rozdiel dostatočne veľký, je možné dokončiť separáciu. Na oddelenie blízkych varných látok s rôznou polaritou sa používa stacionárna fáza, selektívne drží jednu alebo viac zložiek v dôsledku dipólovej dipólovej interakcie. S zvýšením polarity kvapalnej fázy sa zvyšuje retenčný čas polárnych zlúčenín.
Na rovnomerne aplikovanie kvapalnej fázy do pevného nosiča sa zmieša s prchavým rozpúšťadlom, ako je éter. K tomuto roztoku sa pridá tuhý nosič. Zmes sa zahrieva, odparuje sa rozpúšťadlo, kvapalná fáza zostáva na nosiči. Suchý nosič s fixnou kvapalnou fázou aplikovaným týmto spôsobom je naplnený stĺpcom, ktorý sa snaží vyhnúť tvorbe dutín. Pre jednotné obaly cez stĺpec, prúd plynu prechádza a súčasne klepnutím na kolónu na balenie tesnení. Potom, pred pripevnením k detektoru sa kolóna zahrieva na teplotu 50 ° C nad jedným, v ktorom sa má použiť. V tomto prípade môžu existovať straty kvapalnej fázy, ale stĺpec je súčasťou stabilného prevádzkového režimu.
Médiá fixných kvapalných fáz. Pevné médium na disperziu pevnej kvapalnej fázy vo forme homogénneho tenkého filmu musia byť mechanicky trvanlivé s miernou špecifickou povrchovou plochou (20 m 2 / g), malou a rovnakou veľkosťou častíc a tiež stačí inertné do adsorpcie na povrchu pevného a plynného fázy Bolo to minimálne. Najnižšia adsorpcia je pozorovaná na nosičoch silánskoizovanej chromozorby, sklenených granúl a fluóropac (fluórované uhľovodíkový polymér). Okrem toho, tuhé nosiče by nemali reagovať na zvýšenie teploty a mali by sa ľahko vyrobiť s kvapalnou fázou. V plynovej chromatografii chelátov vo forme pevného nosiča sú najčastejšie používané nosiče silánených bielych diatomitídy - diatómový oxid kremičitý, alebo kizelgour. Ditomitída je mikrómna, obsahujúca voda, oxid kremičitý. Takéto nosiče zahŕňajú chromozorb W, Gasohrom Q, Chromaton N, et al. Okrem toho, sklenené gule a užívanie teflónu.
Chemicky súvisiace fázy. Často používajú modifikované nosiče, kovalentne spojené s kvapalnou fázou. V tomto prípade je stacionárna kvapalná fáza pevne držaná na povrchu aj pri najvyšších teplotách stĺpcov. Diatomitický nosič sa napríklad spracuje chlórsilánom s dlhým substituentom s dlhým reťazcom, ktorý má určitú polaritu. Chemicky spojená pevná fáza je efektívnejšia.
6. Distribučná chromatografia. Papierová chromatografia (chromatografia na papieri)
Distribučná chromatografia je založená na používaní rozdielov v rozpustnosti distribuovanej látky v dvoch kontaktných neintegrujúcich kvapalných fázach. Fázy - PF a NF sú kvapalné fázy. Pri pohybe kvapalného PF pozdĺž kvapaliny NF sa chromatografické látky neustále prerozdeľujú medzi oboma kvapalnými fázami.
Distribučná chromatografia sa vzťahuje na papier chromatugrafika (alebo chromatografia na papieri) v obvyklých možnostiach. V tomto spôsobe, namiesto dosiek s tenkou vrstvou sorbentu použitého pri TLC sa použije špeciálny chromatografický papier, podľa ktorého sa impregnatuje, kvapalný PF sa pohybuje počas chromatografie zo štartovacieho vedenia k povrchovej čiare rozpúšťadla.
Rozlišovať normálna fáza a verná papierová chromatografia.
V uskutočnení normálna fáza papierová chromatografia kvapalného NF je voda, sorbovaná vo forme tenkej vrstvy na vláknach a v pórách hydrofilný papier (až 25% hmotnosti). Táto viazaná voda v jej štruktúre a fyzikálnom stave je veľmi odlišná od konvenčnej kvapalnej vody. V ňom sú komponenty zdieľaných zmesí rozpustené.
Úloha PF pohybujúceho sa lisu sa hrá inou kvapalnou fázou, napríklad organická kvapalina s pridaním kyselín a vody. Kvapalný organický PF pred chromatografiou sa nasýti vodou tak, že PF sa nerozpustí sorted na vláknach hydrofilného chromatografického papiera.
Chromatografický papier vyrába priemysel. Musí spĺňať niekoľko požiadaviek: Pripravte sa z vysoko kvalitných vláknitých zlúčenín bavlny, aby boli homogénne v hustote a hrúbke, v smere orientácie vlákien, chemicky čistých a inertných v porovnaní s NF a zdieľanými zložkami.
V normálnom fázovom uskutočnení sú tekuté zmesi zložené z rôznych rozpúšťadiel najčastejšie používané ako PF. Klasickým príkladom takéhoto PF je zmes kyseliny octovej, n-butanolu a vody v objemovom pomere 1: 4: 5. Používajú sa rozpúšťadlá, ako je etylacetát, chloroform, benzén atď.
V uskutočnení vernáfazova papierová chromatografia Kvapalina NF je organické rozpúšťadlo, zatiaľ čo voda, vodné alebo alkoholické roztoky a alkoholové zmesi s alkoholmi, pôsobí ako kvapalný PF. Proces sa vykonáva pomocou hydrofóbny chromatografický papier. Získa sa ošetrením (impregnáciou) s naftalénom, silikónovým olejom, parafínom atď. Nepolárne a nízko polárne organické rozpúšťadlá sú sudované na hydrofóbnych papierových vláknach a prenikajú do pórov, ktoré tvoria tenkú vrstvu kvapaliny NF. Voda nie je udržiavaná na takomto papieri, nie je mokrý.
Technika papiera chromatografie všeobecne je rovnaká ako v metóde TLC. Zvyčajne sa Kashpo analyzovaného roztoku obsahujúceho zmes zdieľaných látok aplikuje na jazdný pruh chromatografického papiera na štartovacej čiare štartu. Po odparení rozpúšťadla je papier pod štartovacou čiarou ponorený do PF, umiestnenie papiera vertikálne (zavesenie). Zatvorte fotoaparát s vekom a chromatografiou, až kým sa PF nedosiahne líniu predného rozpúšťadla označeného na papieri. Potom sa proces preruší, papier sa suší vo vzduchu a detekciu spotov a identifikuje zložky zmesi.
Papierová chromatografia je podobná metóde TLC použitá v kvalitatívnej aj kvantitatívnej analýze.
Ak chcete kvantifikovať obsah jednej alebo inej zložky zmesi, používajú sa rôzne metódy:
1) Postupujte z prítomnosti určitej závislosti (proporcionálne, lineárne) medzi množstvom látky v oblasti škvŕn a spotov (často sa kalibračný program je vopred postavený);
2) Zvážte škrtovú škvrnu s látkou a rovnakým čistým papierom na ploche a potom z hľadiska rozdielu nájdu hmotnosť látky stanovenej;
3) Zohľadnite vzťah medzi intenzitou farby farby a obsahu v ňom v ňom, ktorá dáva farbu farbiva.
V niektorých prípadoch sa látky obsiahnuté v škvrnach extrahujú akákoľvek rozpúšťadlom a potom sa extrahuje.
Papierová chromatografia je metóda farmakopoeia, ktorá sa používa na oddelenie zmesí obsahujúcich anorganické aj organické látky. Spôsob je k dispozícii, jednoduchý na splnenie, ale vo všeobecnosti je horší ako modernejší TLC metóda, v ktorej sa aplikuje tenká vrstva sorbentu.
7. Sedimentárna chromatografia
Spôsob chromatografie sedimentov sa používa hlavne na separáciu a identifikáciu anorganických iónov, ktoré tvoria zmesi.
Podstata metódy. Chromatografia sedimentov je založená na používaní chemických reakcií vyzrážania zdieľaných zložiek zmesi s činidlom-precipentom, ktorý je súčasťou NF. Separácia sa uskutočňuje v dôsledku nerovnej rozpustnosti vytvorených zlúčenín, ktoré sa prenášajú do pohyblivej fázy pri rôznych rýchlostiach: menej rozpustné látky sa prenášajú do PF pomalšie ako rozpustné.
Môžete ilustrovať použitie spôsobu na príklade separácie halogenidových iónov: CL-iónový chlorid, bromid-ión-iónový ión a jodid-ion-ion-iónový ión, súčasne obsiahnutý v analyzovanom vodnom roztoku. Na to použite chromatografickú kolónu (reprezentujúcu sklenenú trubicu so žeriavom v dne) naplnenej sorbentom. Ten sa skladá z ich nosiča - oxid hlinitý al2O3 alebo Si02 kremík, impregnovaný roztokom dusičnanu strieborného agno 3 (obsah dusičnanu strieborného je asi 10% hmotn. Z hmotnosti nosiča sorbentu).
Prostredníctvom chromatografickej kolóny sa uskutočňuje vodný roztok obsahujúci zmes zdieľaných aniónov. Tieto anióny interagujú s ag + striebornými katiónmi, ktoré tvoria tak rozpustný strieborný halogenid:
AG + + I -\u003e AGIV (žltá)
AG + + BR -\u003e AGBRV (krém)
AG + + CL -\u003e AGCLV (biely)
Rozpustnosť striebra halogenidov vo vode sa zvyšuje v sekvencii:
AGL (K ° \u003d 8,3 * 10 -17)< АgВг (К° = 5,3*10 -13) < AgCl (K°= 1,78*10 -10),
kde v zátvorkách sú hodnoty produktov rozpustnosti pri teplote miestnosti. Najprv sa vytvorí žltá zrazenina jodidu striebra, pretože najmenej rozpustný na chromatograme sa pozoruje žltá (horná) zóna. Potom sa vytvorí os strieborného bromidu strieborného (medziľahlá zóna). Nakoniec sa vytvorí biela zrazenina chloridu striebra - spodná biela zóna je tmavá v dôsledku fotochemického rozkladu chloridu striebra s uvoľňovaním jemného kovového striebra.
Výsledkom je, že sa získa primárny sedimentárny chromatogram.
Pre jasnejšie oddeľovanie zón, po získaní primárneho chromatogramu, čisté rozpúšťadlo sa prechádza cez kolónu, čím sa získa sekundárny sedimentárny chromatogram s jasným separáciou zrážok zrážania.
V opísanom príklade bol precipitátor súčasťou NF, a roztok obsahujúci zmes zdieľaných iónov sa uskutočnil cez kolónu. Naopak, naopak, prejsť roztokom precipitátora cez kolónu v NF, ktoré sú chromatografické ióny. Zároveň sa však vytvárajú zmiešané zóny.
Schéma separácie CL-, BR- a Ióny v chromatografickom kolóne spôsobom sedimentárnej chromatografie.
7.1 Klasifikácia metód sedimentárnej chromatografie na technike experimentu
Zvyčajne rozlišovať stĺpec Sedimentárna chromatografia sa uskutočnila v chromatografických stĺpcoch a rovina Chromatografia s sedimentom implementovaná na papieri alebo v tenkej vrstve sorbentu.
Ako sorbenty pri sedimentárnej chromatografii sa používajú zmesi inertných médií s inšpirátom; sorbenty drží preciptiátory vo forme iónov (ionomeničové živice) alebo vo forme molekúl (aktívne uhlie); Papier impregnovaný s precipitantovým roztokom.
Nosiče najčastejšie si vyberajú silikagél, škrob, oxidy hlinitého, vápnika, síran bárnatý, ionomeničové živice atď. Nosič sa používa v jemnom dispergovanom stave s rozmermi približne 0,02-0,10 mm.
Ako precipitanty sa používajú také činidlá, ktoré tvoria nízko rozpustné precipitáty s chromatografickými iónmi, napríklad, jodid sodný Nai, sulfid sodný Na2S, sulfát sulfát SOP2S04, ferocyanid strieborný K4, oxychinolín, pyridín atď.
Zvyčajne sa pri použití spôsobu chromatografie stĺpcového sedimentov po prechode cez kolónu čistého rozpúšťadla sa získajú jasne oddelené zóny, z ktorých každý obsahuje iba jednu zložku (v prípade rozpustnosti zrážok sa líši najmenej trikrát). Spôsob je charakterizovaný dobrou reprodukovateľnosťou výsledkov.
V prípade tvorby bezfarebných oblastí zrážania je chromatogram znázornený alebo prechádza cez stĺpec-developer-developer, ktorý poskytuje vyzrážače natreté reakčné produkty, alebo okamžite zavádzal vývojár v PF alebo v NF.
7.2 Chromatografia sedimentov na papieri
Zvážte esenciu tejto metódy na príklad analýzy vodného roztoku obsahujúceho zmes medených katiónov Cu2 +? Iron Fe 3+ a hliník al 3+.
V strede papiera listu impregnovaného precipitant roztoku - ferocyanid draselný K4 sa kapilára aplikuje analyzovaným vodným roztokom. Cu 2+ a IONY IONY Fe2 + interagujú s fercyanidovými iónmi s tvorbou slabo rozpustných zrážok:
2CU 2+ + 4-\u003e CU 2 (BROWN)
4+ + 3 4-\u003e FE4 (BLUE)
Pretože ferokyanid meď (II) je menej rozpustný ako ferokyanid zo železa (III), potom sa rozlišuje zrazenina medi (II) ferokyanidu, ktorá tvorí centrálnu hnedú zónu. Potom sa vytvorí modrá zrazenina železitého železa (III), ktorá poskytuje modrú zónu. Hliníkové ióny sa presunujú do obvodu, čím sa získa bezfarebná zóna, pretože netvoria maľovaný hliníkový ferokyanid.
Systém rozdelenia CU2 +, FE3 + a AL3 + metódou sedimentárnej chromatografie.
Týmto spôsobom sa získa primárny chromatogram, kde sa zrážacie zrážky čiastočne prekrývajú.
Potom sa získa sekundárny chromatogram. Na to, vhodné rozpúšťadlo (v prípade posudzovaného materiálu je vodný roztok amoniaku) sa aplikuje kapilárou do stredu primárneho chromatogramu. Rozpúšťadlo spontánne sa pohybuje zo stredu papiera na obvod, ktorý sa odovzdáva sám a vyzráža sa, ktoré sa pohybujú pri rôznych rýchlostiach: zóna rozpustnejšia sedimentu železnej železa pohybuje rýchlejšiu zónu menej rozpustného sedimentu meďného ferokyanidu. V tomto štádiu, kvôli rozdielu v rýchlostiach zón vysídlenia, ich jasnejšie oddelenie dochádza.
Na otvorenie hliníkových iónov, ktoré tvoria bezfarebnú periférnu zónu, ukážku sekundárneho chromatogramu - rozprašovač (z postrekového) roztoku alizhára - organického činidla, ktorý tvorí s hliníkovými iónmi ružovými reakčnými produktmi. Získajte vonkajší ružový krúžok.
8. Iónová výmenná chromatografia
V ionomeničovej chromatografii sa separácia zložiek zmesi dosiahne reverzibilnou interakciou ionizujúcich látok s iónovými skupinami. Konzervácia e-postúpenia sorbentu je zabezpečená prítomnosťou protiiónov schopných iónom výmene umiestnenej v tesnej blízkosti povrchu. Ión zavedenej vzorky, ktorá spolupracuje s fixným nabitím sorbentu, výmeny s protiiónom. Látky, ktoré majú rôznu afinitu k fixnému náboja, sú rozdelené do aniónov alebo na katión. Anionáty majú pozitívne nabité skupiny na povrchu a sorbite z mobilnej fázy aniónov. Kationias, resp. Obsahuje skupiny s negatívnym nábojom, interakciou s katiónmi.
Ako mobilná fáza sa používajú vodné roztoky kyselín soli, báz a rozpúšťadiel typu kvapalného amoniaku, t.j. Systémy rozpúšťadiel s vysokým významom dielektrickej konštanty a veľkej tendencie k ionizám zlúčeniny. Typicky pracuje s tlmivými roztokmi, čo umožňuje nastavenie hodnoty pH.
Keď chromatografická separácia iónov analyzovanej látky súťažia s iónmi obsiahnutými v eluente, ktorý sa snaží spolupracovať s opačne nabitých sorbentových skupín. Z toho vyplýva, že ionomeničová chromatografia sa môže použiť na oddelenie všetkých zlúčenín, ktoré môžu byť ionizované akýmkoľvek spôsobom. Je možné analyzovať aj neutrálne molekuly cukrov vo forme ich komplexov s borátovým iónom.
Ionovitá výmenná chromatografia je nevyhnutná v oddelení vašich šťavy látok, ktoré nemôžu byť analyzované GLC bez prekladu na deriváty. Takéto zlúčeniny zahŕňajú aminokyseliny, peptidy, cukor.
Ion-výmenná chromatografia je široko používaná v medicíne, biológii, biochémii, na kontrolu životného prostredia, pri analýze obsahu liekov a ich metabolitov v krvi a moči, eradikáty v potravinárskych surovinách, ako aj na separáciu anorganických zlúčenín, vrátane Radioizotopy, lantanoidy, actinoidy atď. Analýza biopolymérov (proteíny, nukleové kyseliny atď.), Ktoré sa zvyčajne používajú hodiny alebo dni, s pomocou iónovej výmennej chromatografie sa uskutočňuje za 20-40 minút s lepšou separáciou. Použitie ionomeničovej chromatografie v biológii umožnila pozorovať vzorky priamo v biosruktúrach, čo znižuje možnosť preskupenia alebo izomerizácie, čo môže viesť k nesprávnemu interpretácii konečného výsledku. Je zaujímavé použiť túto metódu na riadenie zmien vyskytujúcich sa s biologickými tekutinami. Použitie poréznych slabých aniónových výmeny na báze silikagélu umožnilo rozdeliť peptidy. Mechanizmus výmeny iónov môže byť reprezentovaný ako nasledujúce rovnice:
pre aniónovú výmenu X - + R + Y - - Y - + R + X -
pre katiónovú výmenu X + + R - Y + - Y + + R - X +
V prvom prípade je ión x-vzorka konkurovať iónov hnuteľnej fázy y - pre iónové centrá R + iónový výmenník a v druhej hospodárskej súťaži s iónmi mobilnej fázy Y + pre iónové centrá R sú Katióny vzorky X +.
Samozrejme, že vzorové ióny, ktoré sú slabo komunikovať s iónomeničom, s touto konkurenciou budú slabo udržiavané na stĺpci a sú najprv vymyté a naopak silnejšie ióny budú eluovať z stĺpca. Sekundárne interakcie neiónovej povahy sa zvyčajne vznikajú v dôsledku adsorpcie alebo vodíkových väzieb vzorky s neiónou časťou matrice alebo v dôsledku obmedzenej rozpustnosti vzorky v pohyblivej fáze.
Oddelenie špecifických látok závisí predovšetkým na výber najvhodnejšej sorbentu a mobilnej fázy. Ako fixná fáza v ionomeničovej chromatografii sa používajú ionomeničové živice a silikátové gély s očkovanými iónovými skupinami.
Polystyrénové ionomeničové živice pre HPLC zrno 10 uM a menej majú selektivitu a stabilitu, ale mesh štruktúru z nich, vyznačujú sa vzdialenosťou medzi uzlami mesh 1,5 nm, čo je výrazne menšie ako veľkosť pórov používaných na silikagél Adsorpčná chromatografia (10 nM), spomaľuje prenos hmoty, a preto významne znižuje účinnosť. Ion-výmenné živice používané v HPLC sú hlavne kopolyméry styrénu a divinylbenzénu. Typicky pridajte 8-12%. Čím väčší obsah di-vinylbenzénu, tým väčšia je tuhosť a pevnosť polyméru, nad kapacitou a spravidla selektivita a menší opuch.
Podobné dokumenty
Celkové charakteristiky chromatografického procesu. Fyzikálne chemické základne chromatografie na tenkej vrstve, klasifikácia analytických metód. Varianty chromatografie podľa fázových stavov. Kontrola kvality potravinárskych výrobkov pomocou metódy TLC, zariadenia.
kurz práce, pridané 12/27/2009
Fenomény sa vyskytujú počas chromatografie. Dva prístupy k vysvetleniu sú teória teoretických tanierov a kinetickej teórie. Plyn, kvapalina, papierová chromatografia. Metóda iónovej výmeny. Prípady aplikácie ionomeničovej chromatografie. Gelchromatografia.
abstraktné, pridané 01/24/2009
Koncepcia a štruktúra polymérových sorbentov, histórie ich tvorby a vývoja, hodnoty v procese distribučnej chromatografie. Typy polymérnych sorbentov, možnosti ich použitia v exkluzívnej chromatografii. Vlastnosti používania tvrdých gélov.
abstraktné, pridané 07.01.2010
Vznik a vývoj chromatografie. Klasifikácia chromatografických metód. Chromatografia na pevnej fixnej \u200b\u200bfáze: plyn, kvapalina (kvapalná adsorpcia). Chromatografia na kvapalnej fixnej \u200b\u200bfáze: plynová kvapalina a gélová chromatografia.
abstraktné, pridané 01.05.2009
Podstatou chromatografickej metódy, histórie jeho vývoja a typov. Rozsah chromatografie, zariadení alebo inštalácií pre chromatografickú separáciu a analýzu zmesí látok. Schéma plynového chromatografu, jej hlavných systémov a princíp prevádzky.
abstraktné, pridané 09/25/2010
Základy spôsobu prenášanej chromatografie. Plynová chromatografia je univerzálny spôsob vysokej kvality a kvantitatívnej analýzy komplexných zmesí a spôsobu výroby jednotlivých zložiek v jeho čistej forme. Použitie plusovej plynovej chromatografie.
kurz práce, pridané 01/09/2010
Essence a obsah chromatografie ion-páru, jeho použitie v kvapalinovej chromatografii a extrakcii na extrakciu liečiva a ich metabolitov z biologických tekutín do organickej fázy. Varianty chromatografie iónových párov, charakteristických znakov.
abstraktné, pridané 07.01.2010
Plynová chromatografia je jednou z najsľubnejších fyzikálno-chemických výskumných metód, ktoré sa v súčasnosti rýchlo vyvíja. Klasifikácia chromatografických metód. Rôzne charakteristické znaky procesu. Podstatou chromatografických metód.
abstraktné, pridané 01/25/2010
Podstata vysoko účinnej kvapalinovej chromatografie (HPLC) ako spôsob analýzy a separácie komplexných nečistôt. Sorbenty, koordinácia a nasýtené cheláty; Vzory vplyvu štruktúry ligandu na správanie chelátov za podmienok infikovanej chromatografie.
abstraktné, pridané 11/10/2011
Koncepcia a hlavné fázy toku vylúčenej chromatografie, jej zásadnej funkcie a rozsahu aplikácie, odrôd a ich charakteristických vlastností. Charakteristiky zariadení používaných v procese exkluzívnej chromatografie.
Mnohé objavy minulého storočia sú povinní ruskej vedeckej farby Michail a jeho spôsob chromatografickej analýzy. Veľký počet vynikajúcich výskumníkov mu musí s ich úspechmi, a mnohým a Nobelovou cenou!
"... Bez Michaelovej práce, nebudeme mať nič spoločné so všetkými" pigmentmi ", nebolo by nič spoločné ..." - Tu je názor jedného slávneho anglického vedca.
Michail Semenovičská farba (1872-1919) - Syn Talianska a ruský intelektuál. Narodil sa v Taliansku v meste Asti, neďaleko Turína. V roku 1891 Mikhail vyštudoval Genevský gymnázia a vstúpil do fyziky a matematiky Fakulty Ženevskej univerzity. Zastupovanie dizertačnej práce "Štúdium fyziológie bunky. Materiály pre znalosti pohybu protoplazmy, plazmatických membrán a chloroplastov" Farba v októbri 1896 dostala lekára lekára prírodných vied. V decembri toho istého roku prichádza do St. Petersburg.
Mikhail nevedel, že štipendium Univerzity v Ženeve nie je uznaná v Rusku. Preto musel pracovať v slávnej Botanike Andrei Sergeyevich Famincin, ktorý tiež študoval chlorofyl, možno povedať o vtákoch práva. V Petrohrade sa farba zoznámil s inými vynikajúcimi botanikami a rastlinnými fyziológmi: i.p. Borodin, M.S. Voronin, A.N. Beketsovo. Bola to brilantná spoločnosť originálu bohatých na myšlienky mysliteľov a zručných experimentov. Farba pokračovala vo svojom výskume chloroplastov, ktorý sa pripravuje súčasne na nové magisterské skúšky a na obranu práce. Prešiel skúškou v roku 1899, a obhajoval svoju diplomovú prácu na Kazašskej univerzite 23. septembra 1901.
Od novembra 1901 pracuje farba ako asistentka oddelenia anatómie a fyziológie rastlín vo Varšavskej univerzite. Na Kindici XI v Kongrese prírodovedcov a lekárov urobil Michail Semenovič správu "Metódy a ciele fyziologického výskumu Chlorofyl", v ktorom prvýkrát uvádzali na spôsob adsorpčnej chromatografie.
Michail Semenovič vyriešil problém oddeľovania zelených listových pigmentov a sú veľmi blízke vlastnosťami. Okrem toho existujú aj iné, veľmi svetlé, pigmenty - karotenoidy v listoch. Je to vďaka karotenoidom a na jeseň žltej, oranžovej, objavia sa karmínové listy. Avšak, zatiaľ čo chlorofyls nie sú zničené, bolo takmer nemožné oddeliť ich pred karotenoidmi.
Ako poznámky YU.G. Chirkov, "Zdá sa, že otvorenie farby bola reakcia na existujúce metódy hrubých a vražedných metód ich separácie. Tu je jedna z techník.
Po prvé, extrakt alkoholu chlorofylu sa ťažil, potom jej tri hodiny boli varu s pridaním silného alkalického (žieravého draslíka). Výsledkom je, že chlorofyl sa rozkladá do kompozitných častí - zelených a žltých pigmentov.
Ale v procese výroby tohto lektvaru (takmer alchemické manipulácie) sa môže prirodzený chlorofyl kolaps. A potom by výskumník by sa zaoberal kusmi pigmentov a dokonca aj s výrobkami ich chemickej transformácie. "
O tom, ako sa stalo veľký objav, píše s.e. Shnol: "Vzal sklenenú trubicu, naplnil ho práškom kriedy a nalial malý alkoholový extrakt z listnatého extraktu na hornej vrstve a horná vrstva kriedy stĺpika bola rovnaká farba. A potom sa MS začala naliať na vrchole v trubike s čistým alkoholom. Drop na kvapku. Ďalšia časť rozpúšťadla bola eluovaná pigmentmi z obilia zŕn, ktoré sa posunuli po trubici. Tam, tam, čerstvé gramové hroby adsorbované pigmenty a zase dali ich nové časti Rozpúšťadlo. Na základe niekoľkých rôznych adsorpčných sily (ľahká elúcia) vynechal s pohyblivým rozpúšťadlom, rôzne pigmenty sa pohybovali pozdĺž kriedy stĺpca pri rôznych rýchlostiach a vytvorili homogénne natreté pruhy čistých látok v stĺpci kriedy. Bolo to krásne. Jasný zelený pás, prúžok žltej žltej - tieto sú dva typy chlorofylov - a jasne žlté-oranžové barotinoidy. M. nazývaný tento obrazový chromatogram. "
"Farba ukázala, - píše Chirkovov - že keď zeleninové pigmenty rozpustené ovce cez vrstvu bezfarebného poréznych sorbentov, jednotlivé pigmenty sa nachádzajú vo forme maľovaných zón - každý pigment má vlastnú farbu alebo aspoň tieň. Sorbent ( To môže byť krieda, cukor prášok ...) adsorb (povrchovo absorbuje: latinčina adsorbere znamená "prehĺtať") rôzne pigmenty s nerovnakom výkonu: niektoré môžu "skĺznuť" s riešením prúdu ďalej, iné budú zadržané bližšie. teda vrstva -N-law maľované farebné farby sorbentu nazývané chromatogram a metóda - chromatografia. "
Zdalo sa teda vyriešila zdanlivo intraktívna úloha. Metóda bola geniálna jednoduchá. Nie je vôbec podobná objemnému, že si vyžaduje veľký počet komplexných postupov reagencií.
Možno, že táto jednoduchosť spôsobila, že väčšina súčasníkov alebo neviedol tento úžasný objav, alebo, čo je stále smutné, vzbudeli proti jeho autora.
Ale čas sa nakladá. Farba bola vynájdená chromatografia na štúdium chlorofylu. Najprv pridelil látku nazývanú chlorofyl alfa a chlorofyl beta. Ukázalo sa, že je vhodné pre výskum nielen pigmenty, ale aj bezfarebných, neinknutých zmesí - proteínov, sacharidov. Pre šesťdesiatych rokov chromatografie dvadsiateho storočia bolo venovaných niekoľko tisíc štúdií. Chromatografia sa stala univerzálnou metódou.
"... ... Zásada chromatografickej separácie látok, otvorená M. Farba, podsiete sadu rôznych metód chromatografickej analýzy. Bez jeho použitia by väčšina úspechov vo vede a technike 20. storočia by bola nemožná. .
Základom všetkého je to jedna spoločná myšlienka. Je jednoduchá. To je v podstate myšlienka geometrického progresie. Nech sú vo všetkých jeho vlastnostiach veľmi blízko, veľmi blízko. Ani ukladanie ani odsávanie ani adsorpcia nie je rozdelená do pozorovateľného rozsahu. Nechajte jednu látku adsorbovaná na povrchu, napríklad uhličitan vápenatý (t.j. menej ako 1%).
Inými slovami, jeho obsah na adsorbente bude 0,99 od obsahu druhej. S adsorbentom zaobchádzame s akýmkoľvek rozpúšťadlom tak, že desorpcia (odpojenie) a elúcia (splachovanie) oboch látok a oboch z nich by sa pohybujú z adsorbentu na rozpúšťadlo a pohybujeme sa týmto výsledným roztokom na čerstvú časť adsorbentu. Potom bude podiel prvej látky na povrchu adsorbentu opäť 0,99 od obsahu druhého, to znamená, že časť je adsorbovaná, rovná 0,99 x 0,99 \u003d 0,98 z počiatočného množstva. Ešte raz, budeme vykonávať elúciu a znovu adsorpciu - teraz podiel prvej látky bude 0,98 x 0,99 \u003d 0,97 z obsahu druhého. Aby bol obsah prvej látky na ďalšiu časť adsorbentu, iba 1 percent obsahu druhého, bude potrebné opakovať cyklus absorpčného elučného cyklu asi 200-krát ...
Myšlienka viacnásobného konverzácie na separáciu látok môže byť modifikovaná do viacnásobného prerozdeľovania zmesi látok v systéme nesušených rozpúšťadiel. Toto je základ distribučnej chromatografie. Rovnaká myšlienka je základom súčasných metód elektroforézy, keď sa zmes látok pohybuje pri rôznych rýchlostiach rôznych adsorbentov v elektrickom poli.
1. ÚVOD.
2. Vznik a vývoj chromatografie.
3. Klasifikácia chromatografických metód.
4. Chromatografia na pevnej fáze:
a) chromatografia na plyn (plynová adsorpcia);
b) Chromatografia kvapaliny (kvapalná adsorpcia).
5. Chromatografia na kvapalnej fixnej \u200b\u200bfáze:
a) plynové kvapalinové chromatografie;
b) gélová chromatografia.
6. ZÁVER.
Ako lúče spektra sú rôzne zložky zmesi pigmentov prirodzene distribuované v kolóne oxidu uhličitého, čo umožňuje jeho kvalitatívne a kvantitatívne stanovenie. Týmto spôsobom sa získal chromatogram a navrhovaná metóda - chromatografická.
M. S. COLOR, 1906
Úvod
So potreba rozdeliť a analyzovať zmes látok, je potrebné čeliť nielen chemik, ale aj mnohým iným špecialistom.
V silnom arzenále chemických a fyzikálno-chemických metód separácie, analýzy, štúdie štruktúry a vlastností jednotlivých chemických zlúčenín a ich komplexných zmesí, jeden z popredných miest zaberá chromatografiu.
Chromatografia je fyzikálno-chemický spôsob separácie a analýzy zmesí plynov, výparov, kvapalín alebo rozpúšťadiel a určenie fyzikálno-chemických vlastností jednotlivých látok na základe distribúcie spoločných zložiek zmesí medzi oboma fázami: pohyblivým a fixným. Látky, ktoré tvoria pevnú fázu, sa nazývajú sorbentmi. Pevná fáza môže byť pevná a kvapalná. Mobilná fáza je tok kvapaliny alebo plynu, prefiltruje cez sorbentnú vrstvu. Mobilná fáza vykonáva funkcie rozpúšťadla a nosiča analyzovanej zmesi látok preložených do plynného alebo kvapalného stavu.
Existujú dva typy sorpcie: adsorpcia - absorpcia tuhých látok a absorpcie - rozpúšťanie plynov a kvapalín v kvapalných rozpúšťadlách.
2. Vyskytol tochromatografia a vývoj a rozvoj
Výskyt chromatografie ako vedeckej metódy je spojený s názvom nesplateného ruského vedeckého snahového semenoviča (1872 - 1919), ktorý v roku 1903 otvoril chromatografiu počas štúdie mechanizmu na transformáciu slnečnej energie v rastlinných pigmentoch. Tento rok by sa mal považovať za dátum vytvorenia chromatografickej metódy.
PANI. Farba prešla roztokom analyzovaných látok a pohyblivej fázy cez adsorpčný pilier umiestnený v sklenenej trubici. V tomto ohľade jej metóda dostala názov stĺpcovej chromatografie. V roku 1938 N.A. Izmailov a M.S. Schreiber ponúkol, že upraví farbu a vykoná separáciu zmesi látok na dosku pokrytej tenkou vrstvou adsorbentu. Ukázalo sa teda tenkovrstvová chromatografia, ktorá umožňuje analyzovať mikrokolizmus látky.
V roku 1947. TB Gapon, E.N. GAPON a F.M. Shemymakin Prvýkrát uskutočnil chromatografickú separáciu zmesi iónov v roztoku, vysvetľuje jeho prítomnosť výmennej reakcie medzi sorbentovými iónmi a iónmi obsiahnutými v roztoku. Teda ďalším smerom chromatografie bola otvorená - iónová výmenná chromatografia. V súčasnosti je ionomeničová chromatografia jedným z najdôležitejších smerov chromatografickej metódy.
E.N. a G. B. GAPON v roku 1948 implementovaný M.S. Myšlienka možnosti chromatografickej separácie zmesi látok na základe rozdielu rozpustnosti ťažko rozpustných zrážok. Tam bola sedimentová chromatografia.
V roku 1957, M. Golay navrhol aplikovať sorbentu na vnútorných stenách kapilárnej trubice - kapilárnej chromatografie. Tento variant vám umožňuje analyzovať mikrokolizmus viaczložkových zmesí.
V 60-tych rokoch existovala možnosť syntetizovať iónové aj nenabité gély, ktoré majú prísne definované veľkosti pórov. To umožnilo vyvinúť možnosť chromatografie, ktorej podstata spočíva v oddelení zmesi látok na základe rozdielu v ich schopnosti preniknúť gélovú chromatografiu. Táto metóda vám umožňuje oddeliť zmesi látok s rôznou molekulovou hmotnosťou.
V súčasnosti chromatografia získala výrazný vývoj. Dnes, rôzne metódy chromatografie, najmä v kombinácii s inými fyzikálnymi a fyzikálno-chemickými metódami, pomoc výskumníkmi a inžiniermi riešiť najdlhšie, často veľmi zložité úlohy vo vedeckom výskume a technike.
3. Klasifikchromatografické metódy
Rôzne modifikácie a varianty metódy chromatografie vyžaduje ich systematizáciu alebo klasifikáciu.
Základom klasifikácie môže byť uvedený na rôzne príznaky, a to:
1. Agregovaný stav fáz;
2. Separačný mechanizmus;
3. Spôsob vykonávania procesu;
4. Účel procesu.
Klasifikácia agregovaným stavom fáz:
plyn (pohyblivý fáza - plyn), plyn-kvapalina (mobilná fáza - plyn, fixná fáza - kvapalina), kvapalina (pohyblivá fáza - kvapalina) chromatografia.
Klasifikácia podľa mechanizmu separácie.
Adsorpčná chromatografia je založená na selektívnej adsorpcii (absorpcii) jednotlivých zložiek zmiešanej zmesi s vhodnými adsorbentmi. Adsorpčná chromatografia sa rozdelí do kvapaliny (kvapalina-adsorpčná chromatografia) a plyn (plynová adsorpčná chromatografia).
Ionomeničová chromatografia je založená na používaní procesov iónov výmeny, ktoré sa vyskytujú medzi pohyblivými iónmi adsorbentu a elektrolytovými iónmi, keď sa roztok analyzu analyzoval cez kolónu naplnenú ionomeničnou látkou (ionit). Ionity sú nerozpustné anorganické a organické zlúčeniny s vysokou molekulovou hmotnosťou. Oxid hlinitý sa používajú ako ionitov, permautis, sulfouggol a rôzne syntetické organické iónové výmenné látky - ion-výmenné živice.
Sedimentárna chromatografia je založená na rozdielnej rozpustnosti zrážok vytvorených zložkami analyzovanej zmesi so špeciálnymi činidlami. Napríklad, keď sa roztok zmesi NG (II) a PB solí prenáša cez kolónu s nosičom, ktorý je vopred impregnovaný roztokom KI, 2 farebné vrstvy sú vytvorené: horná, maľovaná v oranžovo-červenej (HGI 2), a dno, maľované žltou (PBI 2).
Klasifikácia podľa procesu vykonávania procesu.
Kolónová chromatografia je typ chromatografie, v ktorej sa kolóna používa ako nosič pre pevné rozpúšťadlo.
Papierová chromatografia je typ chromatografie, v ktorej sa ako nosič pre pevné rozpúšťadlo namiesto reproduktora používajú pásy alebo listy filtračného papiera, ktorý neobsahuje minerálne nečistoty. V tomto prípade sa na okraj papierových pásov aplikuje kvapka testovaného roztoku, napríklad zmes roztokov Fe solí (III) a CO (II). Papier sa suspenduje v uzavretej komore (obr. 1), znižuje jeho okraj s kvapkou testovaného roztoku do nádoby s pohyblivou rozpúšťadlom, napríklad s n-butylalkoholom. Pohyblivé rozpúšťadlo, pohybujúce sa papierom, wets ho. V tomto prípade každá látka obsiahnutá v analyzovanej zmesi s rýchlosťou, ktorá je inherentná, sa pohybuje v rovnakom smere ako rozpúšťadlo. Po ukončení separácie iónov sa papier suší a potom sa postrieka s činidlom, v tomto prípade s roztokom K4, ktorý tvorí maľované zlúčeniny s oddeliteľnými látkami (modrý - so iónmi železa, zeleno - s iónmi kobaltu). Zóny vytvorené s týmto spôsobom vo forme maľovaných škvŕn vám umožňujú vytvoriť prítomnosť jednotlivých zložiek.
Papierová chromatografia v kombinácii s použitím organických činidiel umožňuje vykonávať kvalitatívnu analýzu komplexných zmesí katiónov a aniónov. Na jednom chromatograme, s pomocou jedného činidla, môže byť zistená rad látok, pretože sa vyznačuje nielen zodpovedajúcim farbením, ale aj určitým umiestnením miesta na chromatograme.
Chromatografia na tenkej vrstve je typ chromatografie v jeho separačnom mechanizme podobný papierovom chromatografii. Rozdiel medzi nimi spočíva v tom, že namiesto plechov papiera sa oddelenie vykonáva na doskách potiahnutých tenkou vrstvou sorbentu z práškového oxidu hlinitého, celulózy, zeolitov, silikagélu, kizelur atď. a drží pevné rozpúšťadlo. Hlavnou výhodou tenkovrstvovej chromatografie je jednoduchosť zariadenia, jednoduchosť a vysoká rýchlosť experimentu, dostatočná prehľadnosť separácie zmesi látok a schopnosť analyzovať ultramickoolizmus látky.
Klasifikácia na účely chromatografického procesu.
Chromatografia má najväčšiu hodnotu ako spôsob kvalitatívnej a kvantitatívnej analýzy zmesí látok (analytická chromatografia).
Preparatívna chromatografia - typ chromatografie, v ktorej sa vyrába separácia zmesi látok v prípravách, t.j. Pre viac alebo menej významných množstiev látok v čistom, bez nečistôt. Úlohou preparatívnej chromatografie sa môže tiež koncentrovať a následné uvoľňovanie zo zmesi látok obsiahnutých vo forme mikrofrmus na hlavnú látku.
Non-analitická chromatografia je typ chromatografie, ktorá sa používa ako metóda vedeckého výskumu. Používa sa na štúdium vlastností systémov, ako sú roztoky, kinetiku chemických procesov, vlastnosti katalyzátorov a adsorbentov.
Takže chromatografia je univerzálny spôsob analýzy zmesí látok, produkujúcich látok v čistej forme, ako aj spôsob štúdia vlastností systémov.
4. Chromatografopraviť na pevnej fixnej \u200b\u200bfáze
ale)Plyn (G.azo adsorbvajíčko) Chromatografia
Plynová chromatografia - chromatografická metóda, v ktorej je mobilná fáza plyn. Plynová chromatografia dostala najväčšiu žiadosť o separáciu, analýzu a výskum látok a ich zmesí, pohybujúce sa bez rozkladu do pary.
Jednou z variantov plynovej chromatografie je plyn-adsorpčná chromatografia - to je spôsob, v ktorom je fixná fáza pevná adsorbent.
V plynovej chromatografii ako mobilná fáza (nosič plynu) používa inertný plyn: hélium, dusík, argón, významne menší ako vodík a oxid uhličitý. Niekedy nosný plyn slúži páru prchavých tekutín.
Plynový chromatografický proces sa zvyčajne vykonáva v špeciálnych zariadeniach nazývaných plynové chromatografy (obr. 3). V každom z nich sa nachádza systém prúdov nosiča plynu, systém prípravy a vloženie zmesi podľa štúdie, chromatografická kolóna s systémom regulácie teploty, analyzuje systém (detektor) a systém na registráciu výsledkov separácie a Analýza (rekordér).
Teplota v plynovej adsorpčnej chromatografie má teplotu. Jeho úloha sa skladá predovšetkým v zmene rovnováhy sorpcie v plynnom systéme - tuhá látka. Zo správnej voľby teploty stĺpca závisí, stupeň separácie zložiek zmesi a účinnosť stĺpca a celková sadzba analýzy. Existuje určitý teplotný rozsah kolóny, v ktorej je chromatografická analýza optimálna. Typicky sa tento teplotný interval nachádza v oblasti v blízkosti teploty varu chemickej zlúčeniny. Keď sa teploty varu zložiek zmesi výrazne líšia, aplikujte teplotu teploty stĺpca.
Rozdelenie chromatografického stĺpca je najdôležitejšia, ale predbežná prevádzka celého procesu plynovej chromatografickej analýzy. Nad binárnymi zmesami (plynové plynové zariadenie) spadajú do detekčného zariadenia. Tu je konverzia zmien v koncentráciách komponentov v priebehu času do elektrického signálu, zaznamenaný pomocou špeciálneho systému vo forme krivky, nazývaného chromatogramu. Výsledky celého zážitku sú do značnej miery závislé od správnej voľby typu detektora, jeho dizajnu. Existuje niekoľko klasifikácií detektorov. Rôzne diferenciálne a integrálne detektory. Diferenciálne detektory Zaregistrujte okamžitú hodnotu jednej z charakteristík (koncentrácia alebo prúd) v čase. Integrálne detektory zhrnujú množstvo látky na určité časové obdobie. Detektory sa tiež používajú v princípe účinku, citlivosti a účelu: termoconduktometrická, ionizácia, spektroskopická, hmotnostná spektrometrická, kapisterická, a mnoho ďalších.
Aplikácia plynovej adsorpčnej chromatografie
Plynová adsorpčná chromatografia sa používa v chemickom a petrochemickom priemysle na analýzu produktov chemickej a petrochemickej syntézy, zloženia olejových frakcií, stanovenie čistoty činidiel a obsah kľúčových produktov v rôznych štádiách technologických procesov atď.
Analýza trvalých plynov a ľahkých uhľovodíkov, vrátane izomérov, plynová chromatografia zaberá 5 až 6 minút. Predtým, na tradičných analyzátoroch plynu táto analýza trvala 5 až 6 hodín. To všetko viedlo k tomu, že plynová chromatografia sa začala široko používaná nielen vo výskumných ústavoch a kontrolných a meracích laboratóriách, ale aj do systému komplexnej automatizácie priemyselných podnikov.
Dnes sa pri hľadaní ropných a plynových polí používa plynová chromatografia, ktorá umožňuje určiť obsah organických látok, ktoré označujú blízkosť olejov a plynových polí vybraných zo vzoriek pôdy.
Plynová chromatografia sa úspešne používa v kriminii, kde sa používa na stanovenie totožnosti vzoriek krvných škvŕn, benzínu, olejov, falošných nákladných potravín atď. Veľmi často sa plynová chromatografia používa na určenie obsahu alkoholu v krvi vodičov automobilov. Niekoľko kvapiek krvi z prsta dostatočne zistiť, koľko, keď a čo alkohol pil.
Plynová chromatografia vám umožňuje získať cenné a jedinečné informácie o zložení potravinových vôní, ako je syr, káva, kaviár, brandy atď. Niekedy informácie prijaté plynovým chromatografickou analýzou nie sú šťastné. Napríklad, často v potravinárskych výrobkoch, je to zbytočné ako pesticídy alebo ovocná šťava obsahuje trichlóretylén, ktorý sa na rozdiel od zákazov použil na zvýšenie stupňa karoténu z ovocia, atď. Ale je to tieto informácie, ktoré chránia ľudské zdravie.
Avšak, tam sú často prípady, keď ľudia jednoducho zanedbávajú prijaté informácie. V prvom rade to odkazuje na fajčenie. Podrobná plynová chromatografická analýza dlhodobo zistilo, že dymové cigarety a cigareta obsahuje až 250 rôznych uhľovodíkov a ich deriváty, z ktorých približne 50 má karcinogénny účinok. To je dôvod, prečo fajčiari majú rakovinu pľúc v 10 krát častejšie, ale stále milióny ľudí pokračujú v jedine, ich kolegovia a príbuzní.
Plynová chromatografia je široko používaná v medicíne na stanovenie obsahu početných liekov, stanovenie hladiny mastných kyselín, cholesterolu, steroidov atď. V tele pacienta. Takéto analýzy poskytujú mimoriadne dôležité informácie o stave ľudského zdravia, priebeh jej choroby, účinnosti používania určitých liekov.
Vedecký výskum v metalurgii, mikrobiológii, biochémii, vo vývoji ochrany rastlín a nových liekov, pri vytváraní nových polymérov, stavebných materiálov a v mnohých iných rôznych oblastiach ľudskej praktickej aktivity je nemožné predstaviť si bez takejto výkonnej analytickej metódy ako plynu chromatografia.
Plynová chromatografia sa úspešne použije na stanovenie obsahu polycyklických aromatických zlúčenín, nebezpečných pre ľudské zdravie, vo vode a vo vzduchu, hladina benzínu vo vzduchu rovín čerpacích staníc, zloženie výfukových plynov vo vzduchu atď.
Táto metóda je široko používaná ako jedna z hlavných metód monitorovania čistoty životného prostredia.
Plynová chromatografia zaberá dôležité miesto v našich životoch, ktoré nám poskytuje kolosálne množstvo informácií. V národnom hospodárstve a vo výskumných organizáciách sa používa viac ako 20 tisíc rôznych plynových chromatografov, ktoré sú nepostrádateľnými asistentmi pri riešení mnohých zložitých úloh, denne vyplývajúcich z výskumných pracovníkov a inžinierov.
b)Kvapalina (kvapalná adsorpcia)chromatografia
Kvapalná chromatografia je skupina chromatografických variantov, v ktorých je pohyblivá fáza kvapalná.
Jedným uskutočnením kvapalinovej chromatografie je kvapalinovou adsorpčnou chromatografiou - to je spôsob, v ktorom je pevná fáza pevná adsorpčná.
Hoci kvapalinová chromatografia bola otvorená skôr ako plyn, len v druhej polovici dvadsiateho storočia vstúpil do obdobia výlučne intenzívny vývoj. V súčasnej dobe, podľa stupňa vývoja teórie chromatografického procesu a techník inštrumentálneho dizajnu, podľa účinnosti a separačnej rýchlosti, je nepravdepodobné, že by sa dosiahol spôsob metód plynovej chromatografickej separácie. Zároveň má každý z týchto dvoch hlavných typov chromatografie svoj vlastný primárny rozsah. Ak je plynová chromatografia vhodná najmä na analýzu, separáciu a výskum chemikálií s molekulovou hmotnosťou 500 - 600, potom sa môže použiť kvapalinová chromatografia na látky s molekulovou hmotnosťou niekoľkých stoviek niekoľko miliónov, vrátane extrémne zložitých makromolekúl polymérov, proteínov a nukleových kyselín. V rovnakej dobe, opozícia rôznych chromatografických metód je neodmysliteľne bez zdravého rozumu, pretože chromatografické metódy sú úspešne doplnené, a na veľmi úlohu konkrétnej štúdie, je potrebné pristupovať odlišne, a to, čo chromatografická metóda Umožňuje vám to vyriešiť s väčšou rýchlosťou, informatizovateľnosťou as menej nákladmi.
Podobne ako v plynovej chromatografii sa detektory používajú v modernej kvapalinovej chromatografii, ktorá môže kontinuálne opraviť koncentráciu stanovenej látky v prietoku tekutiny vypnutej z kolóny.
Univerzálny detektor pre kvapalinovú chromatografiu neexistuje. Preto by sa v každom konkrétnom prípade mali vybrať v najväčšom detektore Únie. Ultrafialové, refraktometrické, mikroorganisté detektory, refrakčné-ionizačné detektory boli najväčšie.
Spektrometrické detektory. Detektory tohto typu sú vysoko citlivé selektívne zariadenia, ktoré umožňujú veľmi malé látky koncentrácie v prúde kvapalnej fázy. Ich svedectvo závisí len málo na teplotné výkyvy a iné náhodné zmeny média. Jedným z dôležitých znakov spektrometrických detektorov je transparentnosť najviac rozpúšťadiel používaných v kvapalinovej adsorpčnej chromatografii v pracovnej oblasti vlnových dĺžok.
Najčastejšie používal absorpciu v UV, menej často v oblasti IR. V UV oblasti, spotrebiče pracujúce v širokom rozsahu sa používajú - od 200 nm do viditeľnej časti spektra alebo na určitých vlnových dĺžkach, najčastejšie pri 280 a 254 nm. Ako zdroje žiarenia sa používajú žlté žiarovky (254 nm), stredný tlak (280 nm) a zodpovedajúce filtre.
Detektory Micro Persorpcie. Základom mikroúčelových detektorov je založený na uvoľnení tepla počas adsorpcie látky na adsorbente, ktorý je naplnený detektorovou bunkou. Meria sa však, nie teplo, ale teplota adsorbentu, ku ktorému sa zahrieva v dôsledku adsorpcie.
Mikroreportný detektor je pomerne vysoko citlivý nástroj. Jeho citlivosť závisí predovšetkým z tepla adsorpcie.
Mikro Prevedenie detektorov sú univerzálne, vhodné na detekciu organických aj anorganických látok. Súčasne sú ťažké získať celkom jasné chromatogramy, najmä s neúplným oddelením zložiek zmesi.
5. ChromatografaTIA na kvapalnej fixnej \u200b\u200bfáze
a) plyn-kvapalinová chromatografia
Plynová chromatografia - plynová chromatografická metóda, v ktorej pevná fáza je mladá kvapalina aplikovaná na tuhý nosič.
Tento typ chromatografie sa používa na oddelenie plynov a výparov kvapalín.
Hlavným rozdielom v plynovej kvapaline z plyn-adsorpčnej chromatografie je, že v prvom prípade je metóda založená na použití procesu rozpúšťania a následného odparovania plynu alebo pary z kvapalného filmu držaného pevným inertným nosičom; V druhom prípade je proces separácie založený na adsorpcii a následnej desorpcii plynu alebo pary na povrchu pevnej látky - adsorbent.
Chromatografický proces môže byť schematicky znázornený nasledujúcim spôsobom. Zmes plynov alebo výparov prchavých kvapalín sa vstrekuje prúdom nosného plynu do kolóny naplneného pevným inertným nosičom, na ktorom je distribúcia nestabilnej kvapaliny (pevná fáza). Študované plyny a páry sú absorbované touto kvapalinou. Potom sú zložky zdieľanej zmesi selektívne posunuté v špecifickom poradí z kolóny.
V plynovej chromatografii sa používa množstvo detektorov špecificky reaguje na akékoľvek organické látky alebo na organických látkach so špecifickou funkčnou skupinou. Patrí medzi ne ionizačné detektory, elektronické detektory zachytávania, tepelné, spektrofotometrické a niektoré ďalšie detektory.
Flame-ionizačný detektor (PID). Práca PID je založená na tom, že organické látky, ktoré patria do plameňa hydrogénu, podliehajú ionizácii, v dôsledku čoho je ionizácia súčasne ionizácia, ktorá je súčasne ionizačná komora, ktorá je súčasne počet nabitých častíc.
PID je citlivý len na organické zlúčeniny a nie je citlivé alebo veľmi zle citlivé na takéto plyny ako vzduch, oxidy síry a uhlíka, sírovodík, amoniak, uhlík, vodná para a niekoľko ďalších anorganických zlúčenín. Necitlivosť PID do vzduchu umožňuje ho aplikovať na stanovenie znečistenia ovzdušia rôznymi organickými látkami.
Pri práci s PID sa použije 3 plyn: nosič plynu (hélium alebo dusík), vodík a vzduch. Všetok 3 plyn musí mať vysoký stupeň čistoty.
Detektor argónu. V detektore argónu je ionizácia spôsobená kolíziou molekúl určenej látky s metastabilnými atómami argónom vyplývajúcim z účinkov rádioaktívneho žiarenia.
Tepelný detektor. Princíp termo-iónového detektora je, že soli alkalických kovov, odparovanie v horáku plameňa, sú selektívne reagujúce so zlúčeninami obsahujúcimi halogény alebo fosforu. V neprítomnosti takýchto zlúčenín v ionizačnej komore detektora je stanovená rovnováha atómov alkalických kovov. Prítomnosť atómov fosforne v dôsledku ich reakcie s atómami alkalických kovov porušuje túto rovnováhu a spôsobuje vzhľad v iónovej štruktúre.
Pretože tepelný detektor má najvyššiu citlivosť na pripojenia obsahujúce fosfor, dostal názov fosfátu. Tento detektor sa používa hlavne na analýzu fosforodinorganických pesticídov, insekticídov a množstva biologicky aktívnych zlúčenín.
b)Gél chromatografia
Gélová chromatografia (gélová filtrácia) - Metóda separácie zmesí látok s rôznymi molekulovými hmotnosťami filtráciou analyzovaného roztoku prostredníctvom priečnych zosieťovaných bunkových gélov.
Oddelenie zmesi látok sa vyskytuje v prípade, že rozmery molekúl týchto látok sú odlišné, a priemer gélových zŕn je konštantný a iba tie molekuly môžu prejsť, ktorých rozmery sú menšie ako priemer gélové póry. Pri prefiltrovaní roztoku zmesi zmesi sa menšie molekuly prenikli do pórov gélu, sú oneskorené v rozpúšťadle obsiahnuté v týchto pórov a pohybovať sa pozdĺž gélovej vrstvy pomalšie ako veľké molekuly, ktoré nie sú schopné preniknúť do pórov. Gélová chromatografia teda umožňuje oddeliť zmes látok v závislosti od veľkosti a molekulovej hmotnosti častíc týchto látok. Táto separačná metóda je pomerne jednoduchá, rýchla a čo je najdôležitejšie, umožňuje oddeliť zmesi látok za podmienok bahna ako iné chromatografické metódy.
Ak sa gélové granuly napĺňajú kolónu a potom do nej nalejte roztok rôznych látok s inou molekulovou hmotnosťou, potom, keď sa roztok pohybuje pozdĺž gélovej vrstvy v kolóne, táto zmes sa uskutoční.
Počiatočné obdobie skúseností: aplikovanie roztoku analyzovanej zmesi na gélovej vrstve v stĺpci. Druhý stupeň - gél neinterferuje s difúziou malých molekúl v pórach, najväčšie molekuly zostávajú v roztoku obklopujúce gélové granule. Pri premytí vrstvou gélu s čistým rozpúšťadlom, veľké molekuly sa začínajú pohybovať rýchlosťou v blízkosti rýchlosti pohybu rozpúšťadla, zatiaľ čo malé molekuly musia najprv predfundu z vnútorného veku gélu do objemu medzi zrnami a ako a Výsledok z toho sú oneskorené a umyté rozpúšťadlom neskôr. Vyskytuje sa zmes látok podľa ich molekulovej hmotnosti. Umývanie látok z kolóny sa vyskytujú, aby sa znížila ich molekulová hmotnosť.
Použitie gélovej chromatografie.
Hlavným účelom gélovej chromatografie je separácia zmesí s vysokou molekulitou a stanovenie rozloženia molekulovej hromadnej hmotnosti polymérov.
Súčasne sa používa rovnako gélová chromatografia na oddelenie zmesi látok strednej molekulovej hmotnosti a dokonca aj spojenia s nízkou molekulovou hmotnosťou. V tomto prípade je dôležité, aby gélová chromatografia umožní oddeliť sa pri teplote miestnosti, čo je priaznivo odlíšiť z plyn-kvapalinovej chromatografie vyžadujúce zahrievanie na prenos analyzovaných látok do parnej fázy.
Oddelenie zmesi látok gélovou chromatografiou je možné a keď sú molekulové hmotnosti analyzovaných látok veľmi blízko alebo dokonca rovnaké. V tomto prípade sa používa interakcia riešení s gélom. Táto interakcia môže byť taká významná, čo znižuje rozdiely vo veľkostiach molekúl. Ak je povaha interakcie s gélom pre rôzne látky nie sú IDA, tento rozdiel sa môže použiť na oddelenie zmesi záujmu.
Príkladom je použitie gélovej chromatografie na diagnózu ochorení štítnej žľazy. Diagnóza je nastavená počtom jódu definovaného počas analýzy.
Vyššie uvedené príklady používania gélovej chromatografie ukazujú jeho dostatočné možnosti na riešenie širokej škály analytických úloh.
Záver
Ako vedecká metóda učenia sa okolo nás, chromatografia sa neustále vyvíja a zlepšuje. Dnes sa aplikuje tak často a tak široko vo vedeckom výskume, medicíne, molekulárnej biológii, biochémii, technológii a národnej ekonomike, čo je veľmi ťažké nájsť oblasť vedomostí, v ktorých sa chromatografia nepoužije.
Chromatografia ako metóda štúdie s výnimočnými schopnosťami je silným faktorom v poznatkoch a transformácii komplikujúceho sveta v záujme vytvorenia prijateľných podmienok ľudského biotopu na našej planéte.
S p as asi doL a t e r a t u rs
1. Ivazov b.v. Úvod do chromatografie. - M.: Vyššie. SK., 1983 - s. 8-18, 48-68, 88-233.
2. Kreszkov A.p. Základy analytickej chémie. Teoretické základy. Kvalitatívna analýza, prvá kniha, ED.4-E, rekreácia. M., "Chémia", 1976 - s. 119-125.
3. Sakodynsky K.I., OEKHOV B.I. Chromatografia vo vede a technike. - M.: Znalosti, 1982 - s. 3-20, 28-38, 58-59.