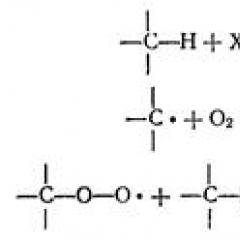
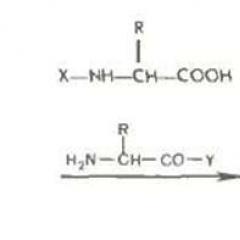
Syntéza tuhej fázy peptidov s ochrannými skupinami VOS a Fmoc. Štruktúra peptidov syntézy pevnej fázy kardioaktívneho peptidu
Peptidová komunikácia má vlastnosti čiastočne duálnej komunikácie. To sa prejavuje pri znižovaní dĺžky tohto spojenia (0,132 nm) v porovnaní s dĺžkou jednoduchej väzby s N (0,147 nm). Čiastočne blbná povaha peptidovej komunikácie je znemožniť voľné otáčanie substituentov okolo neho, takže peptidová skupina je plochá a má zvyčajne trans-konfiguráciu (F-la i). V poriadku je náprava peptidového reťazca séria tvrdých rovín s pohyblivými ("sklopnými") artikulácie na mieste, kde asymetrické atómy s (v F-Le I sú označené hviezdičkou).
V peptidových roztokoch existuje výhodná tvorba určitých konformy. S predlžovaním reťazca je získaná výraznejšia stabilita (podobná proteínom) objednaným prvkom sekundárnej štruktúry. Tvorba sekundárnej štruktúry je zvlášť charakteristická pre pravidelné peptidy, najmä pre polyamínové kyseliny.
Vlastnosť
Oligopeptidy podľa vlastností sú blízko aminokyselín, polypeptidy sú podobné proteínom. Oligopeptidy sú zvyčajne kryštalické látky, ktoré sa rozkladajú, keď sa zahrievajú na 200 300 0 ° C, že sú dobre rozpustné vo vode, zriedených kyselinách a alkáliách, sú takmer nerozpustné v organických rozpúšťadlách. Výnimky sú oligopeptidy konštruované z hydrofóbnych aminokyselinových zvyškov.
Oligopeptidy majú amfotérne vlastnosti a v závislosti od kyslosti média môžu existovať vo forme katiónov, aniónov alebo ožívaní iónov. Hlavné absorpčné pásy v IR spektre pre skupinu NH 3300 a 3080 cm-1, pre skupinu C \u003d 0 1660 cm-1. V UV spektrách sa absorpčný pás peptidovej skupiny nachádza v oblasti 180-230 nm. Peptidový izoelektrický bod (PI) sa značne líši a závisí od zloženia aminokyselinových zvyškov v molekule. Vesmídy RK a peptidov sú pre A-COXY cca. 3, pre -h 2 cca. osem.
Chemické vlastnosti oligopeptidov sú stanovené funkčnými skupinami obsiahnutými v nich, ako aj peptidové znaky. Ich chemické transformácie sú do značnej miery podobné zodpovedajúcim aminokyselinovým reakciám. Dávajú pozitívnu reakciu buretu a reakciu ningidrínu. Dipeptidy a ich deriváty (najmä étery) sa ľahko cyklizujú, otočia sa na diketopiperazines. Pod pôsobením 5,7 normálne peptidy kyseliny chlorovodíkovej sú hydrolyzované na aminokyseliny po dobu 24 hodín pri 105 ° C.
Syntéza peptid
V peptidovej syntéze, známe z organickej chémie reakcie získania amidov a špeciálne vyvinutých spôsobov syntézy peptidov. Na úspešnú implementáciu tejto syntézy je potrebné aktivovať karboxylovú skupinu, t.j. Zvýšiť elektrinu karbonylu. To sa dosahuje chemickou modifikáciou karboxylovej skupiny aminokyselín. Typ takejto modifikácie zvyčajne určuje názov metódy syntézy peptidov.
1. Metóda chlorydridu.
Spôsob je založený na reakcii získania amidov na interakciu chloridov chloridu s zodpovedajúcimi amínmi. Táto metóda získala prvé peptidy. V súčasnosti je táto metóda extrémne zriedkavá, pretože je sprevádzaná tvorbou vedľajších produktov a peptidov racemic.

2. Azidová metóda
Počiatočná látka v tomto spôsobe je najčastejšie etyléterová n-chránená aminokyselina, z ktorej sa získa hydrazid, druhý sa získa s použitím dusitanu sodného v prítomnosti kyseliny chlorovodíkovej v kyseline azide. V reakcii sa zvyčajne používa hydrazín, v ktorom je jeden z dusičov blokovaný ochrannou skupinou (Z-karbobenzoxy alebo carbohyterCluclear), ktorý zabraňuje tvorbe bočných dihydrazidov. Azidy pri interakcii s C-chránenými aminokyselinami v miernych podmienkach tvoria peptidy.
Racemizácia v tomto spôsobe je minimalizovaná, ale môžu byť nežiaduce reakcie, az: azidy môžu byť preskupené do izokyanátov, čo zase, keď interaktujú s alkoholom použitým ako rozpúšťadlom, tvoria uteráty.

3. Zmiešané anhydridy
Zmiešané anhydridy aminokyselín s derivátmi kyseliny uhlí získané napríklad boli zistené široké použitie v peptidovej syntéze, získanej napríklad s použitím izobutylchlórhličitanu: 
Reakcia v tejto syntéze sa uskutočňuje pri nízkej teplote (-10. -20 s), pomerne rýchlo, čo výrazne znižuje možnosť tvarovania vedľajších produktov a racemie. Rýchla stupňovitá syntéza peptidov s použitím zmiešaných anhydridov sa nazýva rema-syntéza. Spôsoby vzdelávania s použitím zmiešaných anhydridov sú široko používané v syntéze peptidov pevnej fázy.
Syntéza peptidov teda vyžaduje účtovníctvo a drsné súlad s niektorými faktormi. Na zníženie tvorby vedľajších produktov a racemie sa preto odporúčajú nasledujúce typové podmienky pre reakciu tvorby peptidovej komunikácie:
1) Spôsob sa musí vykonať pri nízkych teplotách, reakčný čas musí byť minimálny;
2) Reakčná hmotnosť musí mať pH blízko neutrálneho;
3) Organické zásady sa používajú ako reagencie viažuce kyseliny ako piperidín, morfolín atď.;
4) Reakcia je výhodne v bezvodom médiu.
Syntéza pevnej fázy
Syntéza s pevnou fázou - metodický prístup k syntéze oligomérov (polyméry) s použitím pevného nerozpustného médiáreprezentujúci organický alebo anorganický polymér.
Na začiatku 60-tych rokov bol navrhnutý nový prístup na riešenie problémov izolácie a čistenia, ktoré vznikajú pri syntéze peptidov. Neskôr otvorením tohto prístupu, R.B. Merrifield, v jeho Nobelovej prednáške povedal, ako sa to stalo: "Akonáhle som si myslel, ako sa dosiahol cieľ účinnejšej syntézy peptidov. Plán bol zbierať peptidový reťazec poštovej a počas syntézy, okruh by mal byť v jednom konci viazaný na tuhý nosič. " Výsledkom je, že uvoľňovanie a čistenie medziproduktov a cieľových peptidových derivátov sa jednoducho zmenšilo na filtráciu a dôkladné premytie pevného polyméru na odstránenie všetkých nadbytočných činidiel a vedľajších produktov zostávajúcich v roztoku. Takáto mechanická prevádzka sa môže uskutočňovať kvantitatívne, ľahko štandardizovať a dokonca byť automatizovaný. Podrobnejšie zvážte tento postup.
Syntéza pevnej fázy, \\ t
metodich. Prístup k syntéze oligo (poly) opatrenia s použitím pevného nerozpustného nosiča (N.), ktorý je tvrdý. alebo Noorg. polymér. To znamená, že je založený na skutočnosti, že prvé spojenie budúceho oligoméru je kovalentne upevnené na "kotvu" skupinu N., predĺženie obvodu sa uskutočňuje štandardnými monomérmi bežnými schémami používanými na syntézu v R-RAX. O výrobe. Syntetický stupeň. Oligomér sa štiepi z N. a purifikuje sa zodpovedajúcimi spôsobmi. T. S. Aplikujte v OSN. Na získanie polypeptidov, oligo-nukleotidov a oligosacharidov.
Pri syntéze polypeptidov ako N. NAB. Kopolymér styrénu a 1-2% divinylbenzénu modifikovaného podávaním skupiny dimetoxybenzylchloridovej skupiny na pripojenie prvej (s chránenou NH2 skupinou) pomocou C-End, napríklad:
Po odstránení N-chrániacej skupiny sa budova polypeptidového reťazca uskutočňuje štandardnými spôsobmi syntézy peptidov v p-re (pozri. Peptidy). Ako kondenzačné činidlá sú NAB. Často používané alebo premietacie aminokyseliny do aktivitu. Éter.
Pri syntéze oligonukleotidov ako N. používajú makroporézy alebo. \\ T Kotviaca skupina slúži karboxylovú skupinu oddelenú od N. Spets. "Noha", napr.

V purínovej alebo pyrimidovej báze
V prvej fáze je nukleozid pripojený k nosiču 3 "-hydroxylovej deoxyribose skupiny, v K-roj, silná skupina v polohe 5" je chránená dimetoxyitortime skupinou (CH3 OS 6N 4) 2 (C 6H 5) C (DMTR); Počet neskôr po jej štiepení sa ľahko merajú spektropometricky, čo slúži ako citácie. Charakteristika na zaťaženie nosiča a umožňuje odhadnúť výstupy v nasledujúcich štádiách predĺženia oligonukleotidového reťazca. Po odstránení skupiny DMTR sa zostava obvodu uskutočňuje s použitím fosfylatididov (F-la i; M. Kapozers, 1980) alebo fosfonátov (hydrofosfonáty) (II; R. RYISZZGG, 1986):

Implementovať T. s. Je potrebné vysoké výnosy (na úrovni 96-99%) v každej fáze dôchodku, ako aj účinné metódy čistenia a zvýraznenia syntézy. spojenia.
Použitie pevnej fázy umožňuje významne zjednodušiť a urýchliť každú fázu zvyšovania reťazca oligoméru, pretože separácia prebytočných zložiek, kondenzačných činidiel a vedľajších produktov umiestnených v P-RE, sa dosahuje certifikáciou reakcie . Zmesi a umývanie N. Vhodná sada p-Rite-Lei. T. Obr., Proces montáže oligomérového reťazca sa rozpadá na rad štandardných operácií: uvoľňovanie rastúceho konca reťazca, dávkovanie ďalšieho chráneného monoméru a kondenzačného činidla, prívod tejto zmesi na kolónu s n , Pre vypočítaný čas a pranie N. Vhodný R-Rider. Cyklus rozšírenia monomérnej jednotky m. B. Automatizované.
V centre automatického. Stužková. Syntetizátory leží všeobecným schematickým diagramom (pozri obr.). Mnohý Modely syntetizátora sa líšia v konštrukcii stĺpcov a ich čísla, spôsob, ako sa privádzajú reagencie a R-Ryteli, atď. Kontroly a programovanie sa vykonávajú vstavaným alebo vykresľovaným počítačom.

Automatika koncepcie. Stužková. syntetizátory (elektrické. Riadiaca čiara je indikovaná bodkovanou čiarou): 1-rini prívodu monomérov (m 1, m N.) a kondenzačné činidlo (KA); 2-line kŕmenie činidiel (napr. Oxidačné činidlá, acylačné činidlá, kt atď.) A phelters (P1, R N.); 3 - prepínateľné ventily; 4-stĺpec s nosičom, vybavený distribúciou. ventil; 5-fotometrický. bunka; 6 metrov; 7-kontrolná a programovacia jednotka; 8-Displej.
Potenciálne vlastnosti je demonštrované syntézou A (R. Merryfield, 1969) a ľudský rastový hormón (D. YAMASHIRO, 1970) s dĺžkou 124 a 183 aminokyselín. Avšak vďaka malým, ale neustálym racemication, ktorý sa vyskytuje pri tvorbe peptidovej komunikácie, syntetika. Majú nízke bioly. Automatická aktivita. Syntetizátory sa používajú CH. Arr. Na získanie krátkych polypeptidov (10-30 liniek), vrátane pre preparatívnu syntézu proteínu (1 g).
To znamená, že Merryphield (1962) pre syntézu polypeptidov je navrhnutý a vložený do praxe polypeptidov a potom sú syntéza oligonukleotidov (R. Letzinger, 1964) a oligosacharidov (A. Patchernik, 1973).
Existuje ďalší dôležitý aspekt používania N. pre držanie Mn. Org. P-qii (, halogenácia atď.). V tomto prípade upravené. N. pôsobí ako polymérne činidlo alebo katalyzátor a všetky transformácie substrátu sa vyskytujú v p-re. Napríklad ROP (OH) (OH) 2 fosfát (OH) 2 fosfáty sa uskutočňujú s použitím zosieťovaného polystyrénu, modifikovaného sulfolfochloridovou skupinou ako kondenzačného činidla.
Svietiť: Chémia polypeptidov, na. Od angličtiny, M., 1977; Reakcie podporované polynermi v organickej syntéze, ED. Podľa P. Hodge, D.C. Sherrington, Chichester, 1980; Syntéza oligonukleotidov, praktický prístup. Umývanie., 1984. B.K. Potapov.
Chemická encyklopédia. - M.: Sovietska encyklopédia. Ed. I. L. KNUNYASTSA. 1988 .
Sledujte, čo je "syntéza s pevnou fázou" v iných slovníkoch:
syntéza pevnej fázy - kombinačná chemická syntéza Syntéza rôznych kompozícií, ktorá využíva pevnú podporu na oddelenie kompozícií počas syntézy, čím sa zjednodušia identifikácia výsledných kompozícií, bola pripojená k rastúcemu peptidovému reťazcu, zatiaľ čo dicyklohexylkarbodiimid sa použil ako kondenzačné činidlo (DCC s prísadou N-hydroxykukcinimid (GS). Aktívny peptid sa oddelil od polyméru, chrániace skupiny boli odstránené pôsobením všetkého, čo môže byť napísané ako schéma (pozri s kyselinou 336, TFUK - kyselina trifluóroctová).
Celkový výťažok produktu 85 bol približne 40%, z ktorých sa môže získať iba 10% purifikovaného aktívneho 84.
Bloky sa syntetizovali väzbou fragmentov získaných buď lineárnou alebo konvergovanou syntézou. Pri konštrukcii bloku (1-12) sa väzba fragmentov uskutočnila cez prolínové väzby, pretože racemizácia je minimálna. Vo väčšine prípadov sa viazanie uskutočnilo aktivovaným éterom s použitím pentachlórfenyl (RSR) alebo -Netrolény. Syntéza schéma je binsiloxikarbonyl protetický blok je znázornený nižšie.

V prípadoch, keď prolínové väzby nemôžu byť použité ako miesto väzby fragmentov, ich zlúčenina sa uskutočňuje metódou azidu, pri ktorej menšia racemizácia.
Celková aktivita výrobku (80%) je vyššia ako v prípade syntézy suroviny Malcrop (30%).

Kombinatorická syntéza sa môže uskutočňovať nielen v roztoku (syntéza fázovej fázy), ale aj na povrchu pevnej chemicky inertnej fázy. V tomto prípade je prvý východiskový materiál chemicky "šitý" na funkčné skupiny na povrchu nosiča polyméru (najčastejšie sa používa esterová alebo amidová väzba) a je spracovaná roztokom druhej požadovanej zložky, ktorá je prevzatá do Významný prebytok reakcie na koniec. V takej forme reakcie existujú určité pohodlie, pretože produkt sa uvoľní: polymér (obvykle vo forme granúl) sa jednoducho filtruje, sa dôkladne premyje z druhého reagenčného zvyšku a chemicky štiepi cieľovú zlúčeninu z neho.
V organickej chémii nie je jediná reakcia, ktorá poskytuje v praxi kvantitatívny výťažok cieľových výrobkov. Jedinou výnimkou je zjavne kompletné spaľovanie organických látok v kyslíku pri vysokých teplotách na CO2 a H20. Preto je čistenie cieľového produktu vždy nevyhnutné, a často najťažšia a časovo náročná úloha. Zvlášť zložitá úloha je izolovať produkty peptidovej syntézy, napríklad separácia komplexnej zmesi polypeptidov. Preto bolo v peptidovej syntéze, že metóda syntézy na pevnom polymérnom substráte, vyvinutá na začiatku 60. rokov dvadsiateho storočia, bola získaná najväčšia distribúcia vyvinutá na začiatku 60. rokov.
Nosičom polyméru v metódou merryfield je granulovaný zosieťovaný polystyrén obsahujúci chlórmetylové skupiny v benzénovom jadre, ktoré sú linkermi spájajúcimi substrát s prvým aminokyselinovým zvyškom polypeptidu. Tieto skupiny konvertujú polyméru do funkčného analógu benzylchloridu a uvádzajú schopnosť ľahko vytvoriť pripojenie esterov zloženia pri reakciách s karboxylátovým aniónmi. Kondenzácia takejto živice s N-chránenými aminokyselinami vedie k tvorbe vhodných benzylesterov. Odstránenie N-ochrany z prvej aminokyseliny chránenej prvej aminokyseliny, kovalentne spojenej s polymérom. Aminoocylácia uvoľnenej aminoskupiny N-chráneného derivátu druhej aminokyseliny, nasledovaná odstránením n-ochrannej ochrany vedie k podobnému derivátu difeptidu tiež viazaného na polymér:
Takýto dvojstupňový cyklus (odstránenie ochrany - aminoocylácia) môže byť v zásade opakovať toľkokrát, koľko je potrebné na vytvorenie polypeptidového reťazca danej dĺžky.
Ďalší rozvoj myšlienok Meriferd bol smerovaný predovšetkým na vyhľadávanie a tvorbu nových polymérnych materiálov pre substráty, vývoj spôsobov oddelenia produktov a vytváranie automatizovaných zariadení pre celý cyklus syntézy polypeptidov
Účinnosť metódy Merofield bola preukázaná úspešnou syntézou radu prírodných polypeptidov, najmä inzulínu. Zvlášť vizuálne výhody boli preukázané v príklade syntézy enzýmovej ribonukleázy. Napríklad, cena značného úsilia, niekoľko rokov, Hirschmen s 22 zamestnancami uskutočnil syntézu ribonukleázového enzýmu (124 aminokyselinových zvyškov) s pomocou tradičných spôsobov kvapalnej fázy. Takmer súčasne sa rovnaký proteín získal automatizovanou syntézou pevnej fázy. V druhom prípade sa syntéza, vrátane iba 11 931 rôznych operácií, vrátane 369 chemických reakcií, uskutočnili dvaja účastníci (GATT a MERRYFIN) v priebehu niekoľkých mesiacov.
Myšlienky Merryfora slúžili ako základ pre vytváranie rôznych metód kombinatorickej syntézy knižníc polypeptidov rôznych budov.
Takže v roku 1982 bola navrhnutá pôvodná stratégia viacstupňovej paralelnej syntézy peptidov na pevnej fáze známej ako "rozdelená metóda" ( rozdeliť. - Metóda štiepania, separácie) alebo "mix a stripped" (Obr. 3). Jeho podstata je nasledovná. Predpokladajme, že tri aminokyseliny (A, B a C) musíte získať všetky možné kombinácie tripeptidov. Na tento účel sú granuly pevného polyméru nosiča (p) oddelené tromi rovnakými časťami a spracujú sa roztokom jednej z aminokyselín. V tomto prípade sú všetky aminokyseliny chemicky spojené s povrchom polyméru jednej z jeho funkčných skupín. Získané polyméry troch odrôd sa dôkladne premiešajú a zmes sa opäť oddelí na tri časti. Potom sa každá časť obsahujúca všetky tri aminokyseliny v rovnakých množstvách opäť ošetruje jedným z rovnakých troch aminokyselín a dostávajú deväť dipeptidov (tri zmesi troch produktov). Ďalšia zmes, separácia do troch rovnakých častí a liečenie aminokyselín poskytujú požadované 27 tripeptidov (tri zmesi deviatich výrobkov) len v deviatich štádiách, zatiaľ čo ich prijatie by vyžadovalo syntézu 27 × 3 \u003d 81 stupňov.
Ministerstvo školstva a vedy Ruskej federácie
FGAOU VPO "Ural Federálna univerzita s názvom po prvom prezidentom Ruska B. N. Yeltsin"
Oddelenie technológie organickej syntézy
Abstrakt na tému: "Princípy a metódy syntézy pevnej fázy. Syntézy peptidy "
Vykonal študent c. X-300803.
Shaikutdinova A.I.
KONTROLA BERSENEVA V.S.
Jekaterinburg 2013.
1. Úvod ............................................... ....................................... 3
2. Čo sú peptidy? .............................................. .. ................................................ štyri
2.1. Štruktúra peptidov ................................................ .................. 5
2.2. Syntéza peptidov ................................................... ................... .7
3. Syntéza peptidov s pevnou fázou ............................................ ......... 10
3.1. Metóda Merrinfield ................................................... ............. 10
3.2. Solídny substrát .................................................... .................. 14
3.3. Výber podkladu ................................................. .................. ... 14
3.4. Linkers ..................................................... ............................. 16
4. Prvá syntéza prírodného hormónu - oxytocín ............................... 22
5. Syntéza inzulínu v klietke ............................................... ............................
6. ZÁVER ................................................... .......................................... ..34
7. Literatúra ................................................... .............................. ... 35
Úvod
V organickej chémii nie je jediná reakcia, ktorá poskytuje v praxi kvantitatívny výťažok cieľových výrobkov. Jedinou výnimkou je zrejme celkový spaľovanie organických látok v kyslíku pri vysokých teplotách až do CO2 a H20. Preto čistenie cieľového produktu je komplexná a časovo náročná úloha. Napríklad 100% purifikácia peptidových syntéznych produktov je ťažký problém. Prvá úplná syntéza peptidu, oxytocínový hormón (1953 g), ktorý obsahuje iba 8 aminokyselinových zvyškov, sa považoval za vynikajúci úspech, ktorý ho priviedol k autora, V. du Vino, Nobelovej cenu z roku 1955. Nasledujúcich dvadsať rokov sa syntéza polypeptidov takejto zložitosti otočila v rutine, takže teraz sa syntéza polypeptidov pozostávajúcich zo 100 a ďalšie aminokyselinových zvyškov už nie je považovaná za neodolateľnú náročnú úlohu.
Cieľ: Rozoberať a vysvetliť: "Čo spôsobilo také dramatické zmeny v oblasti syntézy polypeptidov?"
Čo sú peptidy?
Peptidy - prírodné alebo syntetické zlúčeniny, \\ tmolekulyktoré sú postavené z rezíduíalfa-aminokyseliny prepojené peptidovými (amidovými) väzbami C (0) NH. Môže obsahovať B.molekulatiež neinderuovaný komponent (napr. Zvyšoksacharid). Počet aminokyselinových zvyškov zahrnutých vmolekulypeptidy rozlišujú dipeptidy, tripeptidy, tetrapeptidy atď. Peptidy obsahujúce až 10 aminokyselinových zvyškov sa nazývajú oligopeptidy obsahujúce viac ako 10 aminokyselinových zvyškov prírodných polypeptidov polypeptidy.s molekulovou hmotnosťou viac ako 6 tisícproteíny.
Prvýkrát sa peptidy izolovali z enzymatických proteínových hydrolyzov. Termín "peptidy" navrhuje E. Fisher. Prvý syntetický peptid dostal T. Kursius v roku 1881. E. Fisher do roku 1905 vyvinula prvý všeobecný spôsob syntézy peptidov a syntetizoval množstvo oligopeptidov rôznych budov. Existujúci príspevok k rozvoju chémie peptidov urobil študentov E. Fisher E. Abdergalden, Lake a M. Bergman. V roku 1932 sa pri syntéze peptidov benzyloxykarbonylovú skupinu použili M Bergman a L. ZervAs (karbobenzoxy skupina) na ochranu alfa-aminoskupín aminokyselín, ktoré znamenali novú fázu vo vývoji peptidovej syntézy. Získané N-chránené aminokyseliny (N-karbobenzoxyamínové kyseliny) boli široko používané na získanie rôznych peptidov, ktoré boli úspešne použité na štúdium viacerých kľúčových problémov chémie a biochémie týchto látok, napríklad na štúdium substrátovej špecifickosti proteolytiky enzýmy. S použitím N-karboenzoxyamínových kyselín sa najprv syntetizovali prírodné peptidy (glutatión, karnosín atď.). Dôležitým úspechom v tejto oblasti sa vyvinula na začiatku 50. rokov. P. Vogan a ďalšie. Syntéza peptidov zmiešanými anhydridmi.
V roku 1953 V. du Vino syntetizoval prvý peptidový hormón-toxotcín. Na základe pojmov vyvinutých P. Merryphield v roku 1963 boli vytvorené automatické peptidové syntetizátory. Dostali intenzívne vývojové metódy kontrolovanej enzymatickej syntézy peptidov. Použitie nových metód umožnilo vykonávať syntézu hormonálneho inzulínu atď.
Úspechy syntetickej chémie peptidov boli pripravené úspechy vo vývoji takýchto spôsobov separácie, čistenia a analýzy peptidov, ako je iónomeničová chromatografia, elektroforéza na rôznych nosičoch, gélovú filtráciu, vysoko účinnú kvapalinovú chromatografiu (HPLC), imuno- \\ t Chemická analýza atď. Dostal veľké vývojové metódy na analýzu koncových skupín a spôsobov stupňovitého štiepenia peptidu. Boli vytvorené najmä automatické analyzátory aminokyselín a automatické prístroje na stanovenie primárnej štruktúry peptid-tzv sekvenčníkov.