Semgikov yu.d. Visoko molekularni spojevi - datoteka N1.docx
UDC 541.64: 547.32: 547.371
Radikalna kopolimerizacija stirena i nezasićenih glicidil estera
Ma Chernigovskaya, t.v. Okulovova
Andgask Državna tehnička akademija,
665835, Irkutsk Regija, Angarsk, ul. Tchaikovsky, 60, [Zaštićeno e-poštom]
Istražuje se binarna radikalna kopolimerizacija nezasićenih glicidil estera (alitko-lglicidil etera, vinilglicidil eter etilen glikola) s stirenom u toluenu mediju. Izračunavaju se konstanti kapolimerizacije i mikrostruktura kopolimera. Utvrđeno je da sastav kopolimera ovisi o strukturi nezasićenog glicidil etera. Kopolimeri alilglicidil etera s bilo kojim sastavom izvorne monomerne smjese su blizu u svojoj strukturi alternativni. S kopolimerizacijom stirena s vinilglicidil eterom etilen glikola, potonji je karakteriziran manjom reaktivnošću. Il. 2. kartica. 3. Bibliograd. 14 imenovano.
Ključne riječi: radikalna kopolimerizacija; Stiren; alilglicidil eter; Vinilglicidi ethere etilen glikola.
Radikalna kopolimerizacija stirena i nezasićenih glicidilnih etera
M.a. Chernigovskaya, t.v. Raskulova.
Andgask Državna tehnička akademija,
60, Chaikovskogo St., 665835, Angaransk, Irkutsk Regija, 665835 Rusija, [Zaštićeno e-poštom]
Radikalna kopolimerizacija stirena i nezasićenog glicidil etera, etilen glikol vinil glicidil eter) ispitan je u otopini toluen. Izračunati su omjeri reaktivnosti i parametri kopolimerne mikrostrukture. Utvrđeno je da kompozicija kopolimera ovisi o nezasićenoj konstrukciji glicidil etera. Kopolimeri stirena i alil-glicidil etera imaju alternativnu strukturu. Etilen glikol vinil glicidil eter ima manje reaktivnost od stijena u kopolimerizaciji. 2 figure. 3 tablice. 14 izvora.
Ključne riječi: radikalna kopolimerizacija; Stiren; Alil glicidil eter; Etilen glikol vinil glicidil eter. Uvod
Jedan od obećavajućih smjerova je sinteza kopolimera s aktivnim funkcijama spojeva visoke molekulske mase. Kao monomeri
za takve sinteze, epoksi spojevi i posebno nezasićeni glicidil esteri (NGE) rastu kamate. Kopolimeri koji sadrže u sastavu NGE linkova zanimljivi su za teoretske studije, budući da istovremena prisutnost u sastavu ciklusa oksirana i atoma kisika u bočnom lancu omogućuje manifestiranje učinaka formiranja kompleksiranja.
S druge strane, takvi polimeri pružaju širok raspon mogućnosti za izmjenu usmjeravanja provođenjem u reakcije imena u oksirane cikluse i stoga otvaraju put do dobivanja materijala, uključujući kompozit, s unaprijed određenim vrijednim kompleksom svojstava.
NGE spektar koji se koristi u reakcijama radikalne kopolimerizacije prilično je širok, međutim, najugroženiji derivati \u200b\u200bmetakrilne kiseline (na primjer, glicidil metakrilat), al-lilglicidil eter (dob), kao i vinilg-licimidil esteri glikola (na primjer , Vinilglicidil eter etilen glikol (PG)). Najzanimljiviji kao modifikatori industrijskih polimera čini se da su dob i VGE, budući da zbog niske reaktivnosti moraju biti dio polimera u ograničenim količinama bez promjene općeg kompleksa osnovnih svojstava polimera.
Tradicionalna područja korištenja ovih spojeva u procesima kopolimerizacije detaljno se raspravljaju u radu. Nedavno, kopolimeri koji sadrže epoksi se sve više koriste za proizvodnju raznih nanomaterijala i nanokomoznosti [na primjer, 5, 6], kao i funkcionalne polimerne kompozitne materijale. Stoga, proučavanje procesa procesa kopolimerizacije NGE, uključujući dob i PEA, s osnovnim industrijskim monomerima predstavlja nesumnjivo znanstveno interesa.
Svrha ovog rada bila je proučavanje binarnog radikalnog kopolimerizacije stirena (ST) s dobi i VGE.
Eksperimentalni dio
Za sintezu kopolimera koristili su robu proizvodnju JSC AZP-a (čistoće
99,8%) sa konstantima: p \u003d 0,906 g / ml, 1Kip \u003d 145 ° C, dob (proizvod tvrtke "Ashsi") sa konstantima: p \u003d 0,962 g / ml, ^ IP \u003d 154 ° C, PI20 \u003d \u003d 1 , 4330 i VGE, dobiveni u IRIH SB RA, oguljeni na kromatografsku čistoću
99,9% sa sljedećim konstantima: P \u003d 1,038
g / ml, ^ ip \u003d 204 ° C, \u003d 1,4310.
Kopolimerizacija je provedena u otopini toluena na temperaturi od 60 ° C i deset puta otapala. Kao inicijator je korišten azo-bis-izomaznom kiselina u količini od 1% mase. Dobiveni kopolimeri su izolirani izoliranim izobutanolom, pročišćenom otplatom izobutanola iz acetona i osušen na konstantnu masu.
Pripravak dobivenih proizvoda utvrđen je prema podacima elementarne analize (C, H), funkcionalne analize (sadržaj epoksidnih skupina) i IR spektroskopije. Određivanje sadržaja epoksidnih skupina u sastavu kopolimera provedeno je metodom inverzne titracije s kloridom klorovodičnom kiselinom prema. Relativna viskoznost je određena za 1% otopine u cikloheksanonu na 25 ° C.
Rasprava o rezultatima
Ovisno o sastavu početne smjese, rezultirajući kopolimeri su kruti u prahu ili amorfne tvari bijele, dobro topljive u polarnim otapalima.
Činjenica kopolimerizacijskog postupka u proučavanim sustavima potvrđena je pomoću podataka turbidimetrijskog titracije. Na primjer, na krivuljama turbidimetrijskog titracije kopolimera ST - VGE (Sl. 1) se uočava, naznačena time, što ukazuje na stvaranje kopolimera, a ne mješavinu dva homopolimera. Slična slika je opažena za kopolimere st - as.
U IR spektri NGE, apsorpcijski bar se uočava u području od 1620-1650 cm - 1, karakterističnog za dvostruku vezu. Prisutnost ciklusa oksirano je potvrđeno prisutnošću apsorpcijskih bendova u slijedećim područjima u spektru: 765 i 915 cm - 1, koji se odnose na oscilacije valencije koje su bogate asipmetom u epoksidnom prstenu; 1230 cm - 1 koji se odnosi na simetrične valence oscilacije epoksidnog prstena; 3060 cm - 1 koji odgovara oscilaciji metilenske skupine u epoksidnom prstenu.
U IR spektri kopolimera apsorpcijskog benda karakterističnog za dvostruku vezu, je odsutan, što potvrđuje protok procesa kopolimerizacije prema vinilu ili alil skupinama. U područjima apsorpcijske karakteristike ciklusa oksirana i alkilnih skupina, kopolimerni spektri su identični spektrima početne NGE.
Eksperimentalni podaci dobiveni kao rezultat proučavanja procesa kopolimerizacije u ST - VGE i ST-Age sustavima prikazani su u tablici. jedan.
Pretpostavljalo se da je proučavana NGE
O 0,2 0,4 0,6 0,8 1.0
Volumen talog, ml
Sl. 1. Ovisnost optičke gustoće otopina kopolimera ST - PARGE iz volumena dodanog talog (metanol). Sadržaj VGE u početnoj smjesi (% mol.): 1 - 10; 2 - 25; 3 - 50
stol 1
Opće zakonitosti kopolimerizacije st-NGE u otopini toluena _ (patka1% mase., 60 ° S, 2 h) __
Br. Sastav početne smjese,% mola. Sastav kopolimera,% mola. Izlaz,%
STE NGE STE NGE
Sustav st - a
1 95 5 36,36 63,64 3,7
2 90 10 55,14 44,86 12,6
3 70 30 47,16 52,84 32,4
4 50 50 92,32 7,68 20,2
5 30 70 46,73 53,27 19,8
6 10 90 60,13 39,87 19,3
Sustav st - wge
1 90 10 91,98 8,02 68,5
2 75 25 79,93 20,07 56,7
3 50 50 67,95 32,05 46,2
4 25 75 55,08 44,92 38,1
5 10 90 46,45 53,55 32,5
imaju nižu reaktivnost u radikalnoj kopolimerizaciji nego umjetnosti. Takva slika je doista opažena za kopolimere st. Oni su obogaćeni poveznicama stanice u cijelom intervalu interval, dok sadržaj VGE jedinice u sastavu kopolimera povećava simbates njegov broj u smjesi monomera (tablica 1).
Za kopolimera st
druga slika. Uz bilo koji sastav početne monomerne smjese, sadržaj ST i dobnih jedinica u kopolimerima su gotovo isti i kreće se od 40 do 64% mola., Što ukazuje na formiranje proizvoda blizu izmjenične (tablica 1).
Kako se analiza književnih podataka pokazuje, za dob, procese naizmjenične kopolimerizacije s dovoljno procesa
tablica 2
Opći obrasci kopolimerizacije BX - NGE u otopini toluena
(Patka 1% mase., 60 ° S, 2 h)
Sastav početne smjese,% mola. Sastav kopolimera,% mola. Izlaz,% viskoznost [g |], dl / g
NGE NGE NGE
Sustav BH - dob
95,0 5,0 96,79 3,21 3,19 0,20
90,0 10,0 93,92 6,08 2,88 0,15
85,0 15,0 87,92 10,58 2,56 0,08
73,7 26,3 76,19 23,81 2,69 0,04
30,1 69,9 44,69 55,31 2,48 0,04
Sustav BH - VM
95,0 5,0 95,55 4,45 3,78 0,29
90,0 10,0 92,44 7,56 3,45 0,26
80,0 20,0 88,44 11,56 3,01 0,22
75,0 25,0 78,79 21,21 2,91 0,17
25,0 75,0 36,62 63,38 2,23 0,13
Širok raspon monomera [na primjer, 11, 12]. To se objašnjava formiranjem kompleksa s prijenosom naboja između dobi i druge somonske mjere, u kojoj dob igra ulogu donatora. Međutim, proučavanje binarnih radikalnih kopolimerizacije starosti s BX koju autori provodi nisu otkrile formiranje naizmjeničnih kopolimera (tablica 2).
Formiranje naizmjeničnih kopolimera s kopolimerizacijom starosti CEC može biti povezano s formiranjem kompleksa s prijenosom naboja između EPOC skupine starosti i aromatskog prstena stirena. Rezultirajući kompleks dalje igra ulogu "individualnog monomera" u kopolimerizaciji, što dovodi do proizvodnje izmjenične strukture.
Izlazi proizvoda, općenito, smanjenje
uz povećanje sadržaja nedjelotvornih monomera u sastavu kopolimera (tablica 1), što je posljedica povećanja koncentracije NGE u početnoj mješavini komonoma. Povećanje koncentracije nisko-aktivnog monomera povećava svoj sadržaj u kopolimeru, ali smanjuje ukupnu brzinu rasta lanca i stoga smanjuje proizvodnju proizvoda i njegovu molekulsku masu. Ovaj argument potvrđuje vrijednosti relativne viskoznosti otopina kopolimera (na primjer, dob) i njihove ovisnosti o esterima eterične smjese (Sl. 2).
Izračun konstantne relativne aktivnosti monomera (konstanti kopolimerizacije) za proučavane sustave provedeni su različitim metodama. Konstante kopolimerizacije sustava
Sl. 2 Ovisnost relativne viskoznosti kopolimera s sadržajem starosti u izvornoj smjesi
Tablica 3.
Konstante kopolimerizacije i prosječna dužina blokova blokova sv ^^ _a nge ^ 2) kao dio kopolimera_
Sustav m1 m1 r li l2
Sustav st - ae 0.70 0.47 R1 \u003d 0.09 1 1
0,50 0,92 R2 \u003d 0,05 21 1
0,75 0,20 N1 \u003d 1,13 ± 0,09 N2 \u003d 0,22 ± 0,02 10 1 1
Sustav ST - VGE 0,50 0,32 9 1
ST - dob je izračunat na temelju podataka funkcionalne analize nelinearne metode najmanjih kvadrata u paketu Mathcad 11 Enterprise Edition, što omogućuje izračune na bilo kojim skupovima eksperimentalnih podataka. Konstante kopolimerizacije za ST-VE sustav izračunati su standardnim metodama FINEMAN-a - Ross i Kelane - BDU-SHA, koristeći metodu planiranja eksperimenta na Mortimeri i Tidwel. Vrijednosti konstanta kopolimerizacije prikazane su u tablici. 3. Na temelju vrijednosti konstanti kopolimerizacije utvrđeni su parametri mikrostrukture kopolimera, koji su također prikazani u tablici. 3.
Dobivene vrijednosti konstanta kopolimerizacije potvrđuju zaključak ranije o različitim reaktivnosti NGE u procesima kopolimerizacije iz čl. Za sustav ST - dob, vrijednosti izračunatih konstanti kopolimerizacije su blizu nule, što je karakteristično za naizmjenične kopolimere. Izračun mikrostrukture ovih kopolimera pokazalo je da se bez obzira na sastav početne smjese dobivaju gotovo strogo izmjenični proizvodi (tablica 3).
Vrijednosti relativne aktivnosti konstante za kopolimere st - wge ukazuju na nižu reaktivnost PG u radikalne kopolimerizacije u odnosu na umjetnost. VGE je prisutan u strukturi podataka
polimeri su samo u obliku pojedinačnih veza, a dužina blokova blokova st u kopolimera prirodno se smanjuje s smanjenjem udjela stanice u početnoj smjesi.
Dakle, struktura kopolimera umjetnosti i NGE, očito, može se odraziti sljedećom formulom:
- // lsk. 1998. T. 71, br. 7. str. 1184-1188.
2. Glikoli vinil esteri - obećavajući monomeri za postupke polimerizacije / HP Grigorieva [i drugi]. L.: Izdavačka kuća LTI, 1982. 9 s.
3. Okulovova t.v. Kopolimerizacija viniylg-log mesisa s funkcionalno supstituiranih vinil monomera: Dr. Njega. Znanosti: 02.00.06: branio 04/21/2010: App. 10/08/2010. Irkutsk, 2010. 315 str.
4. Pokrovskaya Ma, Okulovova t.v. Kopolimerizacija alilglicidil etera s stiren // biltenom agta. 2011. № 5. str. 87-89.
5. Površinska funkcionalizacija SI3N4 nanočestica po cijevi polimerizacije glicidil metakrilata i stijena / luo ying // J. Appl. Polim. Sci-a. 2006. V. 102. Ne. 2. str. 992.
6. Tan Chung-Sung, Kuo Ting-Wu. Sinteza polikarbonata i silikagela nanokomita iz kopolimeriza-tion CO2 s alil glicidil eterom, cikloheenčem oksidom i sol-gelom // j.plj. Polim. Sci-a. 2005. V. 98. Ne. 2. str. 750.
7. Formiranje kompozita na temelju VI-nylglicidil etera etilen glikola i vinilhla-Rida / O.V. Lededeva [et al.] // plastične mase. 2013. br. 9. str. 35-39.
8. Kalinina M.S. Analiza kondenzacijskih polimera. M.: Science, 1983. 296 str.
9. Praktični vodič za određivanje molekularnih težina i distribucije molekularne mase polimera / A.I. Khtenstein [i drugi]. M.: Kemija, 1964. 188 str.
10. Frakcije polimera / ed. M. Kantova. M.: Mir, 1971. 444 str.
11. Heapley F., Lovell P.A., McDonald J. NMR-studije o slobodno radikalnoj polimerizaciji i kopolimerizaciji monomera i polimera koji sadrže alil skupine // EUR. Polim. J. 2. 1993. V. 29, br. 2. R. 255.
12. Yu Qing-Bo, Bai Ru-KE, Zhang Ming Hee. Živi radikalni kopolimerizacija alilglicidil etera s metilakrilatom u prisutnosti benzil-dazol-1-karbodiaciateate // Anhui Ligong Daxue Xebao. Ziran Kexue Ban; J. Anhui univ. Sci-a. I tehnol. Natur. Sci-a. 2006. V. 26, br. 3. P. 56.
13. Učinak pretposljedbene veze u kopolimerizaciji vinil klorida i neodređenim glicidil-out esterima / TV-om Schulakova [et al.] // Spojevi visoke molekularne težine A. 2000. T. 42, br. 5. P. 744-750.
14. Tidwell P.W., Mortimer G.A. Poboljšana metoda izračunavanja omjera reaktivnosti kopolimerizacije // J. Polym. Sci-a. A. 1965. V. 3. str. 369.
S polimerizacijom mješavine dva ili više monomera se često formira mješavina homopolimera, ali novi proizvod u kojem se distribuiraju sve vrste monomerne jedinice duž svakog polimernog lanca. Takav proizvod se naziva kopolimer i reakcija na kojoj se formira - kopolimerizacija.
Fizikalna svojstva kopolimera uglavnom se određuju prirodom, relativnom količinom i mjestom monomernih jedinica duž lanca. Postoje statistički kopolimeri, blokirani kopolimeri i cijepljeni (ili "graft" -) kopolimeri.
Statistički kopolimeri karakteriziraju slučajna raspodjela različitih veza duž lanca:
~ A-in-in-a-in-in-in-in-in-a-in-in-in-in-in-in-in-in-in-in-in-u-
Makromolekule blokiraju kopolimeri su izgrađeni od izmjeničnih sekvenci, "blokova" iste vrste polimernih jedinica:
~
Graft ("graft" -) kopolimeri se odlikuju prisutnošću bočnih lanaca cijepljenih na glavni lanac polimera:
Statistička kopolimerizacija
Odnos monomernih jedinica u polimeru često se razlikuje od omjera monomera u izvornoj smjesi. Relativni trend monomernih jedinica na uključivanje u polimerni lanci ne odgovara u općem slučaju relativne brzine tijekom homopolimerizacije. Doista, neki monomeri,
na primjer, malenički anhidrid, kopolimeri se lako formiraju, ali ne pokazuju nedosljednosti za formiranje polimera.
Kada se razmatra problem strukture kopolimera, preporučljivo je usvojiti sljedeće pretpostavke:
- 1) reaktivnost rastućeg radikala ne ovisi o duljini materijalnog lanca;
- 2) reaktivnost rastućeg radikala određena je monomernoj vezi na kojoj je lokaliziran nespareni elektron i ne ovisi o izmjeni veza u makro-radikal;
- 3) s dovoljnom duljinom makro-radikala, monomer se troši samo za nastavak rasta i ne sudjeluje u prijenosnim reakcijama;
- 4) stacionarni proces.
Formiranje dvostrukih kopolimera - rezultat četiri reakcije rasta konkurentnih lanca:

Pod tim uvjetima, brzina protoka monomera A i B izražena su jednadžjima
Uzimanje što K.
| Aa. |
| P. |
| Ab |
| P. |
= r. 1 I. DO
| Bb. |
| P. |
| Bačan |
| P. |
= r. 2, gdje r. 1 I. r. 2 - Relativna reaktivnost odnosno monomera A i B, dobivamo jednadžbu pripravka kopolimera na svakom specifičnom trenutku reakcije:
Za svaki par parametara monomera r. 1 I. r. 2 karakteriziraju odnos reakcijskog kapaciteta monomera. Vrijednost r I.je odnos reakcije brzine konstanta određenog makro-radikala u kojem je lokaliziran nespareni elektron
na monomeru, koji je kraj link lanca, na konstantu njihove brzine reakcije s drugim monomerom u sustavu. Vrijednost r. 1\u003e 1 znači da bi aktivni centar trebao biti lakše reagirati s monomerom istog tipa i r. 1 < 1 - преимущественно с другим мономером. Значения r I. Ne ovise o metodi izražavanja koncentracija monomera. Pripravak kopolimera ovisi o relativnim koncentracijama monomera u početnoj smjesi i ne ovisi o razrjeđenju i ukupnoj brzini reakcije. Promjena r. 1 I. r. 2 označava promjenu reakcijskog mehanizma.
Sastav statističkog kopolimera ne ovisi o ukupnoj brzini procesa kopolimerizacije i prirode inicijatora. Procijeniti prosječni sastav kopolimera na različitim stupnjevima transformacije s poznatim vrijednostima r. 1 I. r. 2 ili za izračunavanje r. 1 I. r. 2 Prema poznatom sastavu početne smjese monomera i pripravak kopolimera koristi integralnu jednadžbu Mayo Lewisa.
Svi gore opisani uzorci razmatrani su na primjerima polimerizacije jedanmonomer (homopolimerizacija). Ali, kao što znate, široko se koristi i kopolimerizacija- Zajednička polimerizacija dva ili tri monomera. Provodi se dobivanje polimera širem spektrom svojstava, da se dobiju materijali s unaprijed određenim svojstvima, kao iu temeljnim istraživanjima kako bi se odredila reaktivnost monomera. Sastav kopolimerizacije je kopolimeri.
U osnovi mehanizam radikalne kopolimerizacije je potpuno sličan mehanizmu radikalne homopolimerizacije, Međutim, ovdje se pojavljuje nekoliko problema.
1) Prilikakopolimerizacija - hoće li se poveznice oba (ili tri) polimera uključiti u polimernog lanca, ili će se svaki monomer posebno polimerizirati i formira se mješavina homopolimera.
2) Omjer između sastava kopolimer i sastav uzet za procesmješavine monomera. Ovdje se namijenjeno diferencijalsastav kopolimera, tj. Njegov sastav trenutno (Ako preuzmete sastavni sastav, tj. Sastav cijele mase kopolimera, jasno je da s velikom dubinom procesa, približno se podudara s pripravkom mješavine monomera, na različitim dubinama procesa , mogu se formirati makromolekule s različitim omjerima monomernih jedinica.
Ako je diferencijalni sastav kopolimera slučajnostsa pripravkom uzet za polimerizaciju smjese monomera, zatim se zove kopolimerizacija azeotropni, Nažalost, slučajevi azeotropne kopolimerizacije prilično su rijetki; U većini slučajeva, diferencijalni sastav kopolimera drugačije jeiz pripravka smjese monomera. To znači da u procesu polimerizacije, monomeri se ne troše u omjeru u kojem se uzimaju; Jedan od njih se konzumira brže od drugog, iu toku reakcije mora se dodati da se održava konstantni sastav smjese monomera. Odavde je jasno koliko je važno nije samo visokokvalitetno, već i kvantitativanrješavanje ovog problema.
3) Priroda strukture nastalog kopolimera, Je statistički, naizmjenični ili blok kopolimerni oblici (vidi stranicu 7-8).
Otopina svih tih problema slijedi iz analize. kinetika Formiranje makromolekule kopolimera, tj. Faze lanac rastas kopolimerizacijom (jer se u ovoj fazi formira makromolekula kopolimera).
Razmotrite najjednostavniji slučaj kopolimerizacije dva monomeri, konvencionalno ukazujući na njihove simbole A i B. Faza rasta lanca u ovom slučaju, za razliku od homopolimerizacije, uključuje elementarne reakcije, a ne jedan, i četiri Vrste: Doista, tijekom rasta, formiraju se "živi" lanci dviju vrsta - s terminalnim radikalnom vezom monomera a [~ a, dopušta, "CH2-CH (X)] i s terminalnom radikalnom vezom monomera u [~ B, recimo ~ CH 2-CH (Y)] i svaki od njih se može pridružiti "svom" i "stranim" monomeru:
Diferencijalni sastav kopolimera ovisi o omjeru brzine ovih četiriju reakcija, konstanti brzine su naznačeni kao K11 ... K 21.
Monomer A je dio kopolimera reakcijom 1) i 4); Stoga je brzina potrošnje ovog monomera jednaka zbroju brzina tih reakcija:
M.  onomomer u reakciji kopolimera 2) i 3), a za njega:
onomomer u reakciji kopolimera 2) i 3), a za njega:
Diferencijalni sastav kopolimera je jednak omjeru brzine ulaska u kopolimer oba monomera:
U  ova jednadžba je teško odrediti koncentracije radikala. Mogu se isključiti iz jednadžbe ako uđete uvjeti kvaziranja: Koncentracija obje vrste Radikali (~ a i ~ b) konstantno; Što se tiče homopolimerizacije, provodi se stanje kvazistacije samo na niskim dubinama procesa.Iz ovog stanja slijedi da je brzina uzajamne transformacije obje vrste radikala isto.Budući da takve transformacije javljaju u reakcijama 2 i 4, onda:
ova jednadžba je teško odrediti koncentracije radikala. Mogu se isključiti iz jednadžbe ako uđete uvjeti kvaziranja: Koncentracija obje vrste Radikali (~ a i ~ b) konstantno; Što se tiče homopolimerizacije, provodi se stanje kvazistacije samo na niskim dubinama procesa.Iz ovog stanja slijedi da je brzina uzajamne transformacije obje vrste radikala isto.Budući da takve transformacije javljaju u reakcijama 2 i 4, onda:
Zamjena dobivene ekspresije za jednadžbu diferencijalnog sastava polimera, u njemu smo rezali i, nakon niza transformacija dobivamo:
E.  tada se zove jednadžba glavne lewisove jednadžbe(Ponekad se zove jednadžba Meyo). Ova jednadžba odražava ovisnost diferencijalnog sastava kopolimera iz sastava monomerne smjese i na vrijednosti R1 i R2. Parametri R1 i R2 se nazivaju konstante kopolimerizacije, Fizičko značenje ovih konstanta slijedi iz njihove definicije: svaki od njih izražava komparativna aktivnost svakog od radikala u odnosu na "svoj" i "vanzemaljski" monomer (Konstantan R1 - za radikal ~ a, konstantan R2 - za radikal ~ b). Ako je radikal lakše pridružiti se "svom" monomeru nego "tuđi", r i\u003e 1, ako je lakše "Alien", r i< 1. Иначе говоря, константы сополимеризации
характеризуют komparativna reaktivna sposobnost monomera.
tada se zove jednadžba glavne lewisove jednadžbe(Ponekad se zove jednadžba Meyo). Ova jednadžba odražava ovisnost diferencijalnog sastava kopolimera iz sastava monomerne smjese i na vrijednosti R1 i R2. Parametri R1 i R2 se nazivaju konstante kopolimerizacije, Fizičko značenje ovih konstanta slijedi iz njihove definicije: svaki od njih izražava komparativna aktivnost svakog od radikala u odnosu na "svoj" i "vanzemaljski" monomer (Konstantan R1 - za radikal ~ a, konstantan R2 - za radikal ~ b). Ako je radikal lakše pridružiti se "svom" monomeru nego "tuđi", r i\u003e 1, ako je lakše "Alien", r i< 1. Иначе говоря, константы сополимеризации
характеризуют komparativna reaktivna sposobnost monomera.
Lijevi dio jednadžbe Maine-Lewis je diferencijalni sastav kopolimera. Na desnoj strani mogu se razlikovati dva bića: 1) sastav monomerne smjese [a] / [b]; 2) faktor koji sadrži konstante kopolimerizacije R1 [a] + [b] / R2 [b] + [a] \u003d d (označavamo simbol D). Lako je vidjeti da na d \u003d 1 d [a] / d [b] \u003d [a] / [b], tj. Azeotropna kopolimerizacija. Kao što je gore spomenuto, slučajevi azeotropne kopolimerizacije su vrlo rijetki, tj. U većini slučajeva d ≠ 1. Tako je faktor D faktor koji određuje razliku između diferencijalnog sastava kopolimera iz pripravka smjese monomera. Ako d\u003e 1, kopolimer je obogaćen monomerom u usporedbi s početnom smjesom (tj. Monomer A se troši u većim udjelu od monomera b). S D.< 1, напротив, быстрее расходуется мономер В.
Vrijednost tvornice D u potpunosti je određena vrijednostima konstanta kopolimerizacije; Posljedično konstante kopolimerizacije određuju omjer diferencijalnog sastava kopolimera i pripravak smjese monomera uzetih u reakciju.
Poznavanje vrijednosti konstanta kopolimerizacije također omogućuje suditi strukturu nastalog kopolimera, kao i mogućnost ili nemogućnosti same kopolimerizacije.
Razmotrite osnovne varijante kopolimerizacije, određene vrijednosti konstanta kopolimerizacije. To je prikladno predstaviti ih grafički u obliku krivulja ovisnosti o diferencijalnom sastavu kopolimera iz pripravka koji se uzima da reagira smjesu monomera (Sl. 3).
R  iP. 3. Ovisnost diferencijalnog sastava kopolimera iz pripravka smjese monomera.
iP. 3. Ovisnost diferencijalnog sastava kopolimera iz pripravka smjese monomera.
1. r. 1 = r. 2 = 1. U ovom slučaju, d [a] / d [b] \u003d [a] / [b], tj. za bilo tkonastaje sastav smjese monomera azeotropnikopolimerizacija. Ovo je rijetka opcija. Grafički se izražava točkara izravno 1 - redak azeotrop.Primjer takvog sustava -popolimerizacija tetrafluoroetilena s kloritrifluoretilenom na 60 ° C.
2. r. 1 < 1, r. 2 < 1 . Oba konstante su manje od jednog. To znači da svaki radikalni po mogućnosti reagira s zbormonomer, tj. Možete govoriti o povećanoj tendenciji monomera na kopolimerizaciju.
 ALI) Sastav kopolimera.Diferencijalni sastav kopolimera obogaćen monomerom, koji nije dovoljno u mješavini monomera(krivulja 2 na slici 3). Lako je ukloniti iz analize činjenice da je u jednadžbi Meio-Lewisa: na [A]<< [B]
D
< 1, следовательно, d[A]/d[B]
< ,
а при [B]
<< [A]
D
>1 i d [a] / d [b]\u003e. Krivulja 2 prelazi azeotrop liniju, tj. s nekim jedanomjer monomera polimerizacije azeotropnih. Ovaj omjer je jednostavan za izračun, jer U ovom slučaju, d \u003d 1; Odavde:
ALI) Sastav kopolimera.Diferencijalni sastav kopolimera obogaćen monomerom, koji nije dovoljno u mješavini monomera(krivulja 2 na slici 3). Lako je ukloniti iz analize činjenice da je u jednadžbi Meio-Lewisa: na [A]<< [B]
D
< 1, следовательно, d[A]/d[B]
< ,
а при [B]
<< [A]
D
>1 i d [a] / d [b]\u003e. Krivulja 2 prelazi azeotrop liniju, tj. s nekim jedanomjer monomera polimerizacije azeotropnih. Ovaj omjer je jednostavan za izračun, jer U ovom slučaju, d \u003d 1; Odavde:
B Struktura kopolimera.Budući da je svaki radikal poželjno spojen Stranac Monomer, u kopolimeru postoji tendencija naizmjenično.Ako konstante kopolimerizacije nisu mnogo manji od jedinice, ovaj trend se ne izražava vrlo značajno, a kopolimer je bliže statističkom od izmjeničnog koeficijenta mikro-metrogena do m (str. 7) bliže 1 od K2] , No, manja je veličina konstanti, veća je struktura polimera koji se približava. Krajnji slučaj je beskrajno mala vrijednost obje konstante (R1 → 0, R2 → 0); To znači da svaki radikal reagira samo s "strancem" monomerom, drugim riječima, svaki od monomera odvojenone polimerizira, ali zajednooni tvore kopolimer. Prirodno, takav kopolimer ima strogo naizmjeničnu strukturu. Primjer takvog sustava je par: 1,2-difeniletilen - maleinsko anhidrid. Postoje i slučajevi kada je jedan od konstanti beskonačno mali, a drugi ima konačnu vrijednost; U takvim slučajevima, samo jedan od samog monomera nije polimeriziran, ali može tvoriti kopolimer s drugim partnerom. Primjer takvog sustava je stiren-maleinsko anhidrid.
3. r. 1 > 1, r. 2 < 1 или r. 1 < 1, r. 2 > 1 . Jedan od konstanti je više od jednog, drugi je manji od jedan, tj. Jedan od monomera lakše reagira s "svojim" monomerom, a drugi - s "strani". To znači da jedan od monomera je aktivniji od drugog Tijekom kopolimerizacije, jer lakše od drugog reagira oba radikali. Prema tome, za bilo tkosastav monomerne smjese, diferencijalni sastav kopolimera obogaćen je jedinicama aktivnijeg monomera (na slici 3 - krivulje 3 'za R1\u003e 1, R2< 1 и 3’’ для r 1 < 1, r 2 > jedan). Ovdje je nemoguća azeotropna polimerizacija.
Struktura kopolimera makromolekule u ovoj izvedbi je najbliži statistički.Privatno (a ne tako rijetko naišao) slučaj: r 1 r 2 \u003d 1, tj. R1 \u003d 1 / R2, dok vrijednosti konstanti nisu mnogo veće od ili manje od jedne. To znači da usporedna aktivnost monomera u odnosu na obaradikali isto(Na primjer, na R1 \u003d 2, R2 \u003d 0,5, monomer je 2 puta aktivniji u monomeru u reakcijama kao s radikalnim ~ A} i s radikalnim ~ B, ▪). U tom slučaju, sposobnost svakog monomera da uđe u polimerni lanac ne ovisi o prirodi radikalas kojom se suočava i jednostavno je određen vjerojatnostsudara sa svakim radikalima. Stoga će struktura kopolimera biti isključivo statistička (k m2). Ovaj se slučaj zove savršena kopolimerizacija - ne zato što u isto vrijeme se formira idealan kopolimer (radije, naprotiv), ali analogno s konceptom savršenog plina, gdje je, kao što je poznato, raspodjela čestica je potpuno statistička. Najpoznatiji primjeri takve kopolimerizacije mogu se pripisati kopolimerizaciji butadiena s stirenom na 60 ° C (R1 \u003d 1.39, R2 \u003d 0,78). U općem slučaju, opcija "jedna konstanta je više od jednog, a druga manje" je možda najčešća.
4. r. 1 > 1, r. 2 > 1. Oba konstanta su više jedinica; Svaki od radikala poželjno reagira s "svojim" monomerom; Sustav ima smanjenu sklonost kopolimerizaciji. O sastavkopolimer, onda bi trebao biti večera monomer koji nekoliko u mješavini monomera. Ova slika je upravo suprotna od onoga što se promatra za R1 opciju.< 1, r 2 < 1, а на рис. 3 была бы представлена кривой, зеркально подобной кривой 2. Но этот вариант kopolimerizacija Rijetku je; Moguće je da je moguće spominjati kopolimerizaciju butadiena s izoprenom na 50 ° C (R1 \u003d 1.38, R2 \u003d 2.05), gdje su konstante samo mnogo više od jednog. No, nažalost, postoje slučajevi kada su obje konstante beskrajno velike (R1 → , R2 ); U tom slučaju, kopolimerizacija se jednostavno ne događa, svaki od monomera se polimerizira odvojeno i formira se mješavina dva homopolimera (primjer - para: butadien - akrilna kiselina). Vrlo korisno bi bilo opcija u kojoj bi konstanti imali više, ali konačan veličina; U ovom slučaju, formirana blokirati kopolimere;nažalost, takve usluge još nisu pronađene.
Pojam "konstanti kopolimerizacije" ne mogu se doslovno percipirati: njihove vrijednosti za ovaj monomer mogu se značajno promijeniti kada se reakcijski uvjeti mijenjaju, posebno, kada se temperatura promijeni. Na primjer, s kopolimerizacijom akrilonitrila s metil akril na 50 ° C R1 \u003d 1.50, R2 \u003d 0.84, i na 80 ° C R1 \u003d 0.50, R2 \u003d 0.71. Stoga, kada su konstantne vrijednosti potrebno odrediti uvjete.
Plan predavanja:
1. radikalna polimerizacija.
2. Ionska polimerizacija
Dobivena je velika većina visokih molekularnih spojeva kao rezultat polimerizacije i polikondenzirajućih reakcija.
Polimerizacija
Polimerizacija je proces proizvodnje polimera, u kojima se konstrukcija makromolekula odvija do dosljednog dodavanja molekula malog molekulske mase (monomera) do aktivnog centra koji se nalazi na kraju rastućeg lanca. Za polimerizaciju, faze inicijacije i rasta lanca su.
Inicijacija - Ova transformacija malog udjela molekula Molera M do AM * aktivnih centara koji mogu pričvrstiti nove molekule monomera. U tu svrhu, patogeni se uvode u sustav ( inicijatori I ili Katalizatori) polimerizacija. Inicijacija polimerizacije može biti predstavljena na ovaj način:
Ako je jedan monomer uključen u polimerizaciju, onda dobiti Homopolimeri, Ako su dva ili više kopolimeri. Ovisno o prirodi aktivnog centra razlikuju se radikal i ionska polimerizacija i kopolimerizacija.
Radikalna polimerizacija
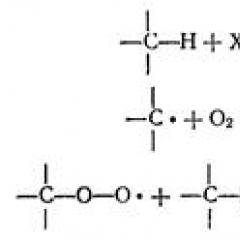
Radikalna polimerizacija uvijek se nastavlja kroz mehanizam lanca. Funkcije aktivnih srednjih proizvoda tijekom radikalne polimerizacije se izvode slobodni radikali. Zajednički monomeri koji ulaze u radikalnu polimerizaciju uključuju vinil monomere: etilen, vinil klorid, vinil acetat, vinil acetat, vinil acetat, tetrafluoroetilen, akrilonitril, metakrilonitril, metil akrilat, metil metakrilat, stiren i dieen monomera (butadien, izopren, kloroprenid.).
Radikalna polimerizacija je karakteristična za sve znakove lančanih reakcija poznatih u kemiji spojeva niske molekulske mase (na primjer, interakcije na svijetlom kloru i vodiku). Takvi znakovi su: oštri učinak manje količine nečistoća za brzinu procesa, prisutnost indukcijskog razdoblja i protoka procesa kroz slijed od tri faze ovisno o međusobno - formiranje aktivnog centra (besplatno radikalni), rast lanca i prekida kruga. Temeljna razlika između polimerizacije iz jednostavnih lančanih reakcija je u tome što je u fazi rasta, kinetički lanac je utjelovljen u materijalnom lancu rastućeg makro-radikala, a taj lanac odrasta do formiranja polimerne makromolekule.
Pokretanje radikalne polimerizacije je svedeno na stvaranje slobodnih radikala u reakcijskom mediju sposobno za pokretanje reakcijskih lanaca. Faza inicijacije uključuje dvije reakcije: pojavu primarnih slobodnih radikala inicijatora R * (1a) i interakciju slobodnog radikala s molekulom monomera (16) da se formira radikal M *:

Reakcija (1b) Potrebno je mnogo puta brže od reakcije (1A). Prema tome, stopa inicijacije polimerizacije određuje reakciju (1a), kao rezultat kojih se generiraju slobodni R * radikali. Slobodni radikali, koji su čestice s nesparenim elektronima mogu se formirati iz molekula pod utjecajem fizičkog utjecaja - toplina, svjetla, penetracijskog zračenja, kada se energija akumulira dovoljna za rupturu π-komunikaciju. Ovisno o vrsti fizički učinak Monomer tijekom inicijacije (formiranje primarne radikalne polimerizacije radikalne polimerizacije je podijeljena na toplinsku, zračenje i fotopolimerizaciju. Osim toga, inicijacija se može provesti zbog propadanja do radikala posebno unesenih u sustav tvari - inicijatori. Ova se metoda naziva stvarna inicijacija.
Toplinska inicijacija leži u Udarac Na visokim temperaturama polimerizacije čistih monomera bez uvođenja posebnih inicijatora na reakcijski medij. U tom slučaju nastaje formiranje radikala, u pravilu, zbog razgradnje malih količina peroksidnih nečistoća, koje se mogu pojaviti kada monomer interagira s air kisikom. U praksi se na taj način dobiva takozvani blok polistiren. Međutim, metoda toplinske inicijacije polimerizacije nije pronašla široku distribuciju, jer zahtijeva visoke troškove toplinske energije, a stopa polimerizacije je u većini slučajeva mali. Može se povećati, povećavajući temperaturu, ali je molekulska masa dobivenog polimera smanjena.
Fotoobizacija Polimerizacija se javlja kada je monomer osvijetljen svjetlom lampe žive, u kojem monomer molekula apsorbira kvadrat svjetla i ide u uzbuđeni energetsko stanje. Posjedovanje s drugom molekulom monomera, deaktivira se prenosom posljednjeg dijela energije, dok se obje molekule pretvaraju u slobodne radikale. Brzina fotopolimerizacije povećava se s povećanjem intenziteta zračenja i, za razliku od toplinske polimerizacije, ne ovisi o temperaturi.
Inicijacija zračenja Polimerizacija u principu slično fotokemijskom. Inicijacija zračenja se sastoji od izloženosti monomerima emisija energije visoke energije (γ -Tch, brzi elektroni, α - Čestice, neutrone itd.). Prednost fotografija i kemijskih metoda inicijalizacije je sposobnost da se odmah "uključi i isključi i isključi", kao i polimerizacija na niskim temperaturama.
Međutim, sve ove metode su tehnološki složene i mogu biti popraćene interno nepoželjnim reakcijama u dobivenim polimerima, kao što je uništavanje. Stoga se u praksi najčešće koristi kemijska (stvarna) inicijacija polimerizacije.
Kemijska inicijacija Provodi se uvođenjem monomera nestabilnih tvari niske molekularne težine koje imaju nisku energiju u svom sastavu - inicijatori lako dezintegriraju slobodne radikale pod utjecajem topline ili svjetla. Najčešći inicijatori radikalne polimerizacije su peroksidi i hidroperoksidi (vodikov peroksid, benzoil peroksidi, hidroperoksidi mpem.-butil i izopropilbenzen i sur.), Azo i diazo spoj (diazobisazomajska kiselina, diazominobenzen, itd.), persulfate od kalija i amonijevog. Ispod su reakcija odgovora nekih inicijatora.
Peroksid tert-butil (alkil peroksid):


Aktivnost i mogućnost korištenja inicijatora radikala polimerizacije određena je brzinom njihove razgradnje, što ovisi o temperaturi. Izbor određenog inicijatora posljedica je temperature koja je potrebna za sintezu polimera. Dakle, dinilille azobizualna kiselina se koristi na 50-70 ° C, benzoil peroksid - na 80-95 ° C i peroksid tert-boutila - na 120-140 ° C.
Učinkoviti inicijatori koji omogućuju provođenje procesa radikalne polimerizacije u sobi i smanjenim temperaturama, su redoks sustavi. Obično, peroksidi, hidroperoksidi, persulfati i drugi redukcijski agensi obično se koriste kao oksidirajuća sredstva (FE, CO, Cu) metali (FE, CO, Cu) metali, sulfiti, amini itd.
Pitanja za samo-test:
1. Koje tvari su inicijatori radikalne polimerizacije?
2. Što je pokretanje radikalne polimerizacije?
3. Vrste inicijacije.
4. Što je polimerizacija?
Predavanje 6. Kopolimerizacija.
Plan predavanja:
1.Popolimerizacija
2. Tehničke metode za homo- i kopolimerizaciju.
Kopolimerizacija
Kopolimerizacija se sastoji u dobivanju tvari visoke molekularne težine iz smjese dva ili više monomera zvanih komonomeri i sama tvari - kopolimer. Makromolekule kopolimera sastoje se od elementarnih veza svih monomera prisutnih u početnoj reakcijskoj smjesi. Svaki komonomer daje kopolimeru na koji uključuje, njegova svojstva, dok svojstva kopolimera nisu jednostavna suma svojstava pojedinih homopolimera. Prema tome, sadržaj male količine stirena u polivinil acetatnim lancima povećava temperaturu staklene prijelaza potonjeg, eliminira svojstvo hladnoće i povećava njezinu površinsku tvrdoću.
Uzorci kopolimerizacije mnogo su kompliciraniji od uzoraka homopolimerizacije. Ako u homopolimerizaciji postoji jedan tip rastućeg radikala i jedan monomer, zatim s binarnom kopolimerizacijom, u kojoj samo dva monomera sudjeluje, postoje najmanje četiri vrste rastućih radikala. Doista, ako dva monomera A i B interakciju s slobodnim R radikalima, koji su nastali tijekom razgradnje inicijatora, formiraju se primarni radikali, od kojih jedan ima terminalnu vezu A, i drugi - u:

Svaki primarni radikal može reagirati s monomerom A i monomerom u:

Omjer konstante brzine reakcije svakog radikala s "njegovim" monomerom do konstantne stope reakcije s "strancem" monomerom Konstante kopolimerizacije ili relativne aktivnostimonomeri:
Vrijednosti R a i Rb određuju sastav kopolimernih makromolekula u većoj mjeri od omjera monomera u izvornoj reakcijskoj smjesi. Na primjer, u par vinil acetata (a) -styrol (c), konstanti kopolimerizacije su RA \u003d 0.01, Rb \u003d 55. To znači da kada se kopolimer dobije polimerizacijom u masi i otapalu, makromolekule sadrže znatno više stiren veze od vinil acetata. Ako je relativna aktivnost komonoma blizu jednog, onda svaki radikal s jednakom vjerojatnošću interaktira i s "njegovim" i s "strancem" monomerom. Uključivanje monomera u lanca je slučajno i oblike statistički kopolimer. Takva kopolimerizacija se zove Savršen. Primjer sustava blizu savršenog, je par butadien-stiren.
Reakcije kopolimerizacije mogu teći i radikalnim i ionskim mehanizmom. S utjecajem iona kopolimerizacije na konstanti kopolimerizacije, utječe priroda katalizatora i otapala. Stoga kopolimeri dobiveni od istih komonoma u istom početnom omjeru u prisutnosti različitih katalizatora, imaju različit kemijski sastav. Prema tome, kopolimer stirena i akrilonitrila, sintetiziran iz ekvimolarne smjese monomera u prisutnosti benzoil peroksida, sadrži 58% stilanskih jedinica. U isto vrijeme, s anionskom kopolimerizacijom na cilindru C6H5 mgbr, sadržaj stirenskih veza u makromolekulama je 1%, a pri kationskoj polimerizaciji u prisutnosti SNCl 4 - 99%.
U praktičnom smislu su zanimljivi blok- i Probačen kopolimeri. U makromolekulama ovih kopolimera nalaze se područja visoke duljine od veza svakog komonomera.
Blok kopolimeri dobivaju se različitim metodama. Prvo, s anionskom polimerizacijom jednog monomera, "živi" lanci koji se pojavljuju, to jest, makroinaci, mogu inicirati polimerizaciju drugog monomera:
Drugo, s intenzivnim mehaničkim učincima na mješavinu različitih polimera dolazi do uništenja lanaca i stvaranje makro-radikala. Makrodikali, međusobno u interakciji, oblikuju blok kopolimer.
Blok kopolimeri također mogu se formirati od oligomera zbog interakcije terminalnih skupina.
Kopolimeri se dobivaju, u pravilu, interakcija monomera s polimerom i rjeđe interakcija dva različita polimera među sobom. Budući da se reakcija prijenosa lanca s konverzijom polimera molekula na makro-radikale koristi u makromolekulama, atomi ili skupine s povećanom pokretljivošću (na primjer, brom) često uvode, što ubrzava reakciju prijenosa vrijednosti , Dakle, ako je reakcijski medij polimer na bazi monomera CH2 \u003d CHX, monomer CH2 \u003d CHY i inicijator, proces formiranja kopolimera za graft nastavlja se kako slijedi. Prvo proizlazi srednji makro-radikal:
Zatim, ovaj makro-radikal inicira polimerizaciju monomera da se formira bočne grane:

Priprema blokova i graft kopolimera gotovo je uvijek popraćena formiranjem tomopolimera iz monomera prisutnog u reakcijskoj zoni.
UDC 541.64: 547.32: 547.371
Radikalna kopolimerizacija stirena i nezasićenih glicidil estera
Ma Chernigovskaya, t.v. Okulovova
Andgask Državna tehnička akademija,
665835, Irkutsk Regija, Angarsk, ul. Tchaikovsky, 60, [Zaštićeno e-poštom]
Istražuje se binarna radikalna kopolimerizacija nezasićenih glicidil estera (alitko-lglicidil etera, vinilglicidil eter etilen glikola) s stirenom u toluenu mediju. Izračunavaju se konstanti kapolimerizacije i mikrostruktura kopolimera. Utvrđeno je da sastav kopolimera ovisi o strukturi nezasićenog glicidil etera. Kopolimeri alilglicidil etera s bilo kojim sastavom izvorne monomerne smjese su blizu u svojoj strukturi alternativni. S kopolimerizacijom stirena s vinilglicidil eterom etilen glikola, potonji je karakteriziran manjom reaktivnošću. Il. 2. kartica. 3. Bibliograd. 14 imenovano.
Ključne riječi: radikalna kopolimerizacija; Stiren; alilglicidil eter; Vinilglicidi ethere etilen glikola.
Radikalna kopolimerizacija stirena i nezasićenih glicidilnih etera
M.a. Chernigovskaya, t.v. Raskulova.
Andgask Državna tehnička akademija,
60, Chaikovskogo St., 665835, Angaransk, Irkutsk Regija, 665835 Rusija, [Zaštićeno e-poštom]
Radikalna kopolimerizacija stirena i nezasićenog glicidil etera, etilen glikol vinil glicidil eter) ispitan je u otopini toluen. Izračunati su omjeri reaktivnosti i parametri kopolimerne mikrostrukture. Utvrđeno je da kompozicija kopolimera ovisi o nezasićenoj konstrukciji glicidil etera. Kopolimeri stirena i alil-glicidil etera imaju alternativnu strukturu. Etilen glikol vinil glicidil eter ima manje reaktivnost od stijena u kopolimerizaciji. 2 figure. 3 tablice. 14 izvora.
Ključne riječi: radikalna kopolimerizacija; Stiren; Alil glicidil eter; Etilen glikol vinil glicidil eter. Uvod
Jedan od obećavajućih smjerova je sinteza kopolimera s aktivnim funkcijama spojeva visoke molekulske mase. Kao monomeri
za takve sinteze, epoksi spojevi i posebno nezasićeni glicidil esteri (NGE) rastu kamate. Kopolimeri koji sadrže u sastavu NGE linkova zanimljivi su za teoretske studije, budući da istovremena prisutnost u sastavu ciklusa oksirana i atoma kisika u bočnom lancu omogućuje manifestiranje učinaka formiranja kompleksiranja.
S druge strane, takvi polimeri pružaju širok raspon mogućnosti za izmjenu usmjeravanja provođenjem u reakcije imena u oksirane cikluse i stoga otvaraju put do dobivanja materijala, uključujući kompozit, s unaprijed određenim vrijednim kompleksom svojstava.
NGE spektar koji se koristi u reakcijama radikalne kopolimerizacije prilično je širok, međutim, najugroženiji derivati \u200b\u200bmetakrilne kiseline (na primjer, glicidil metakrilat), al-lilglicidil eter (dob), kao i vinilg-licimidil esteri glikola (na primjer , Vinilglicidil eter etilen glikol (PG)). Najzanimljiviji kao modifikatori industrijskih polimera čini se da su dob i VGE, budući da zbog niske reaktivnosti moraju biti dio polimera u ograničenim količinama bez promjene općeg kompleksa osnovnih svojstava polimera.
Tradicionalna područja korištenja ovih spojeva u procesima kopolimerizacije detaljno se raspravljaju u radu. Nedavno, kopolimeri koji sadrže epoksi se sve više koriste za proizvodnju raznih nanomaterijala i nanokomoznosti [na primjer, 5, 6], kao i funkcionalne polimerne kompozitne materijale. Stoga, proučavanje procesa procesa kopolimerizacije NGE, uključujući dob i PEA, s osnovnim industrijskim monomerima predstavlja nesumnjivo znanstveno interesa.
Svrha ovog rada bila je proučavanje binarnog radikalnog kopolimerizacije stirena (ST) s dobi i VGE.
Eksperimentalni dio
Za sintezu kopolimera koristili su robu proizvodnju JSC AZP-a (čistoće
99,8%) sa konstantima: p \u003d 0,906 g / ml, 1Kip \u003d 145 ° C, dob (proizvod tvrtke "Ashsi") sa konstantima: p \u003d 0,962 g / ml, ^ IP \u003d 154 ° C, PI20 \u003d \u003d 1 , 4330 i VGE, dobiveni u IRIH SB RA, oguljeni na kromatografsku čistoću
99,9% sa sljedećim konstantima: P \u003d 1,038
g / ml, ^ ip \u003d 204 ° C, \u003d 1,4310.
Kopolimerizacija je provedena u otopini toluena na temperaturi od 60 ° C i deset puta otapala. Kao inicijator je korišten azo-bis-izomaznom kiselina u količini od 1% mase. Dobiveni kopolimeri su izolirani izoliranim izobutanolom, pročišćenom otplatom izobutanola iz acetona i osušen na konstantnu masu.
Pripravak dobivenih proizvoda utvrđen je prema podacima elementarne analize (C, H), funkcionalne analize (sadržaj epoksidnih skupina) i IR spektroskopije. Određivanje sadržaja epoksidnih skupina u sastavu kopolimera provedeno je metodom inverzne titracije s kloridom klorovodičnom kiselinom prema. Relativna viskoznost je određena za 1% otopine u cikloheksanonu na 25 ° C.
Rasprava o rezultatima
Ovisno o sastavu početne smjese, rezultirajući kopolimeri su kruti u prahu ili amorfne tvari bijele, dobro topljive u polarnim otapalima.
Činjenica kopolimerizacijskog postupka u proučavanim sustavima potvrđena je pomoću podataka turbidimetrijskog titracije. Na primjer, na krivuljama turbidimetrijskog titracije kopolimera ST - VGE (Sl. 1) se uočava, naznačena time, što ukazuje na stvaranje kopolimera, a ne mješavinu dva homopolimera. Slična slika je opažena za kopolimere st - as.
U IR spektri NGE, apsorpcijski bar se uočava u području od 1620-1650 cm - 1, karakterističnog za dvostruku vezu. Prisutnost ciklusa oksirano je potvrđeno prisutnošću apsorpcijskih bendova u slijedećim područjima u spektru: 765 i 915 cm - 1, koji se odnose na oscilacije valencije koje su bogate asipmetom u epoksidnom prstenu; 1230 cm - 1 koji se odnosi na simetrične valence oscilacije epoksidnog prstena; 3060 cm - 1 koji odgovara oscilaciji metilenske skupine u epoksidnom prstenu.
U IR spektri kopolimera apsorpcijskog benda karakterističnog za dvostruku vezu, je odsutan, što potvrđuje protok procesa kopolimerizacije prema vinilu ili alil skupinama. U područjima apsorpcijske karakteristike ciklusa oksirana i alkilnih skupina, kopolimerni spektri su identični spektrima početne NGE.
Eksperimentalni podaci dobiveni kao rezultat proučavanja procesa kopolimerizacije u ST - VGE i ST-Age sustavima prikazani su u tablici. jedan.
Pretpostavljalo se da je proučavana NGE
O 0,2 0,4 0,6 0,8 1.0
Volumen talog, ml
Sl. 1. Ovisnost optičke gustoće otopina kopolimera ST - PARGE iz volumena dodanog talog (metanol). Sadržaj VGE u početnoj smjesi (% mol.): 1 - 10; 2 - 25; 3 - 50
stol 1
Opće zakonitosti kopolimerizacije st-NGE u otopini toluena _ (patka1% mase., 60 ° S, 2 h) __
Br. Sastav početne smjese,% mola. Sastav kopolimera,% mola. Izlaz,%
STE NGE STE NGE
Sustav st - a
1 95 5 36,36 63,64 3,7
2 90 10 55,14 44,86 12,6
3 70 30 47,16 52,84 32,4
4 50 50 92,32 7,68 20,2
5 30 70 46,73 53,27 19,8
6 10 90 60,13 39,87 19,3
Sustav st - wge
1 90 10 91,98 8,02 68,5
2 75 25 79,93 20,07 56,7
3 50 50 67,95 32,05 46,2
4 25 75 55,08 44,92 38,1
5 10 90 46,45 53,55 32,5
imaju nižu reaktivnost u radikalnoj kopolimerizaciji nego umjetnosti. Takva slika je doista opažena za kopolimere st. Oni su obogaćeni poveznicama stanice u cijelom intervalu interval, dok sadržaj VGE jedinice u sastavu kopolimera povećava simbates njegov broj u smjesi monomera (tablica 1).
Za kopolimera st
druga slika. Uz bilo koji sastav početne monomerne smjese, sadržaj ST i dobnih jedinica u kopolimerima su gotovo isti i kreće se od 40 do 64% mola., Što ukazuje na formiranje proizvoda blizu izmjenične (tablica 1).
Kako se analiza književnih podataka pokazuje, za dob, procese naizmjenične kopolimerizacije s dovoljno procesa
tablica 2
Opći obrasci kopolimerizacije BX - NGE u otopini toluena
(Patka 1% mase., 60 ° S, 2 h)
Sastav početne smjese,% mola. Sastav kopolimera,% mola. Izlaz,% viskoznost [g |], dl / g
NGE NGE NGE
Sustav BH - dob
95,0 5,0 96,79 3,21 3,19 0,20
90,0 10,0 93,92 6,08 2,88 0,15
85,0 15,0 87,92 10,58 2,56 0,08
73,7 26,3 76,19 23,81 2,69 0,04
30,1 69,9 44,69 55,31 2,48 0,04
Sustav BH - VM
95,0 5,0 95,55 4,45 3,78 0,29
90,0 10,0 92,44 7,56 3,45 0,26
80,0 20,0 88,44 11,56 3,01 0,22
75,0 25,0 78,79 21,21 2,91 0,17
25,0 75,0 36,62 63,38 2,23 0,13
Širok raspon monomera [na primjer, 11, 12]. To se objašnjava formiranjem kompleksa s prijenosom naboja između dobi i druge somonske mjere, u kojoj dob igra ulogu donatora. Međutim, proučavanje binarnih radikalnih kopolimerizacije starosti s BX koju autori provodi nisu otkrile formiranje naizmjeničnih kopolimera (tablica 2).
Formiranje naizmjeničnih kopolimera s kopolimerizacijom starosti CEC može biti povezano s formiranjem kompleksa s prijenosom naboja između EPOC skupine starosti i aromatskog prstena stirena. Rezultirajući kompleks dalje igra ulogu "individualnog monomera" u kopolimerizaciji, što dovodi do proizvodnje izmjenične strukture.
Izlazi proizvoda, općenito, smanjenje
uz povećanje sadržaja nedjelotvornih monomera u sastavu kopolimera (tablica 1), što je posljedica povećanja koncentracije NGE u početnoj mješavini komonoma. Povećanje koncentracije nisko-aktivnog monomera povećava svoj sadržaj u kopolimeru, ali smanjuje ukupnu brzinu rasta lanca i stoga smanjuje proizvodnju proizvoda i njegovu molekulsku masu. Ovaj argument potvrđuje vrijednosti relativne viskoznosti otopina kopolimera (na primjer, dob) i njihove ovisnosti o esterima eterične smjese (Sl. 2).
Izračun konstantne relativne aktivnosti monomera (konstanti kopolimerizacije) za proučavane sustave provedeni su različitim metodama. Konstante kopolimerizacije sustava
Sl. 2 Ovisnost relativne viskoznosti kopolimera s sadržajem starosti u izvornoj smjesi
Tablica 3.
Konstante kopolimerizacije i prosječna dužina blokova blokova sv ^^ _a nge ^ 2) kao dio kopolimera_
Sustav m1 m1 r li l2
Sustav st - ae 0.70 0.47 R1 \u003d 0.09 1 1
0,50 0,92 R2 \u003d 0,05 21 1
0,75 0,20 N1 \u003d 1,13 ± 0,09 N2 \u003d 0,22 ± 0,02 10 1 1
Sustav ST - VGE 0,50 0,32 9 1
ST - dob je izračunat na temelju podataka funkcionalne analize nelinearne metode najmanjih kvadrata u paketu Mathcad 11 Enterprise Edition, što omogućuje izračune na bilo kojim skupovima eksperimentalnih podataka. Konstante kopolimerizacije za ST-VE sustav izračunati su standardnim metodama FINEMAN-a - Ross i Kelane - BDU-SHA, koristeći metodu planiranja eksperimenta na Mortimeri i Tidwel. Vrijednosti konstanta kopolimerizacije prikazane su u tablici. 3. Na temelju vrijednosti konstanti kopolimerizacije utvrđeni su parametri mikrostrukture kopolimera, koji su također prikazani u tablici. 3.
Dobivene vrijednosti konstanta kopolimerizacije potvrđuju zaključak ranije o različitim reaktivnosti NGE u procesima kopolimerizacije iz čl. Za sustav ST - dob, vrijednosti izračunatih konstanti kopolimerizacije su blizu nule, što je karakteristično za naizmjenične kopolimere. Izračun mikrostrukture ovih kopolimera pokazalo je da se bez obzira na sastav početne smjese dobivaju gotovo strogo izmjenični proizvodi (tablica 3).
Vrijednosti relativne aktivnosti konstante za kopolimere st - wge ukazuju na nižu reaktivnost PG u radikalne kopolimerizacije u odnosu na umjetnost. VGE je prisutan u strukturi podataka
polimeri su samo u obliku pojedinačnih veza, a dužina blokova blokova st u kopolimera prirodno se smanjuje s smanjenjem udjela stanice u početnoj smjesi.
Dakle, struktura kopolimera umjetnosti i NGE, očito, može se odraziti sljedećom formulom:
- // lsk. 1998. T. 71, br. 7. str. 1184-1188.
2. Glikoli vinil esteri - obećavajući monomeri za postupke polimerizacije / HP Grigorieva [i drugi]. L.: Izdavačka kuća LTI, 1982. 9 s.
3. Okulovova t.v. Kopolimerizacija viniylg-log mesisa s funkcionalno supstituiranih vinil monomera: Dr. Njega. Znanosti: 02.00.06: branio 04/21/2010: App. 10/08/2010. Irkutsk, 2010. 315 str.
4. Pokrovskaya Ma, Okulovova t.v. Kopolimerizacija alilglicidil etera s stiren // biltenom agta. 2011. № 5. str. 87-89.
5. Površinska funkcionalizacija SI3N4 nanočestica po cijevi polimerizacije glicidil metakrilata i stijena / luo ying // J. Appl. Polim. Sci-a. 2006. V. 102. Ne. 2. str. 992.
6. Tan Chung-Sung, Kuo Ting-Wu. Sinteza polikarbonata i silikagela nanokomita iz kopolimeriza-tion CO2 s alil glicidil eterom, cikloheenčem oksidom i sol-gelom // j.plj. Polim. Sci-a. 2005. V. 98. Ne. 2. str. 750.
7. Formiranje kompozita na temelju VI-nylglicidil etera etilen glikola i vinilhla-Rida / O.V. Lededeva [et al.] // plastične mase. 2013. br. 9. str. 35-39.
8. Kalinina M.S. Analiza kondenzacijskih polimera. M.: Science, 1983. 296 str.
9. Praktični vodič za određivanje molekularnih težina i distribucije molekularne mase polimera / A.I. Khtenstein [i drugi]. M.: Kemija, 1964. 188 str.
10. Frakcije polimera / ed. M. Kantova. M.: Mir, 1971. 444 str.
11. Heapley F., Lovell P.A., McDonald J. NMR-studije o slobodno radikalnoj polimerizaciji i kopolimerizaciji monomera i polimera koji sadrže alil skupine // EUR. Polim. J. 2. 1993. V. 29, br. 2. R. 255.
12. Yu Qing-Bo, Bai Ru-KE, Zhang Ming Hee. Živi radikalni kopolimerizacija alilglicidil etera s metilakrilatom u prisutnosti benzil-dazol-1-karbodiaciateate // Anhui Ligong Daxue Xebao. Ziran Kexue Ban; J. Anhui univ. Sci-a. I tehnol. Natur. Sci-a. 2006. V. 26, br. 3. P. 56.
13. Učinak pretposljedbene veze u kopolimerizaciji vinil klorida i neodređenim glicidil-out esterima / TV-om Schulakova [et al.] // Spojevi visoke molekularne težine A. 2000. T. 42, br. 5. P. 744-750.
14. Tidwell P.W., Mortimer G.A. Poboljšana metoda izračunavanja omjera reaktivnosti kopolimerizacije // J. Polym. Sci-a. A. 1965. V. 3. str. 369.