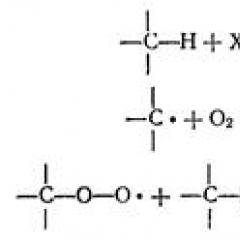
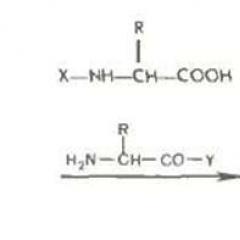
Kromatografi gelişimi. Bir araştırma yöntemi olarak kromatografi
Kromatografi bir Rus bilim adamı, botanik ve fizikokemist Mikhail semenovich rengidir.
Kromatografinin keşfi, Master'ın St. Petersburg'da (1900 - 1902) ve Varşova'daki ilk çalışmaların ilk döneminde (1902 - 1903) çalışmalarının tamamlanmasının zamanını ifade eder. Bitkilerin pigmentlerini keşfetmek, renk, bir adsorban tozlu kalsiyum karbonat ile doldurulmuş tüpten pigmentlerin renginde çok az farklılaştı ve daha sonra net bir çözücü ile adsorbanı yıkandı. Karışımın ayrı bileşenleri bölünmüş ve renkli çizgiler oluşturulmuştur. Modern terminolojiye göre, renk, kromatografinin gelişen varyantını keşfetti (sıvı adsorpsiyon kromatografisi geliştirme). Onun tarafından yaratılan kromatografinin gelişimi konusundaki araştırmanın temel sonuçları. Doktora tezi olan "Bitki ve Hayvan Dünyasında Kromofiller" (1910) kitabında belirtilen renk. Kromatografi Gazı Sedimanter İyon Değişimi
Renk, sadece karışımın ayrılması için değil, kromatografik yöntemi, karışımın ayrılması için değil, aynı zamanda kantitatif analiz için de kullandı, bunun için cam kolonunu kırdı ve adsorban kolonunu katmanlara kesti. Renk, sıvı kromatografi için ekipman geliştirmiştir, ilk kez indirgenmiş basınç altında kromatografik işlemler (pompalama) ve bazı aşırı basınçlarda, verimli sütunların hazırlanması için geliştirilen önerilerde bulundu. Buna ek olarak, "kromatografi", "tezahür", "yer değiştirme", "kromatogram", vb. Gibi yeni bir yöntemin birçok temel kavramını ve şartını tanıttı.
Kromatografi ilk olarak çok nadiren kullanılmıştır, gizli süresi yaklaşık 20 yıl sürdü, bu sırada yöntemin çeşitli uygulamaları hakkında sadece çok az sayıda mesaj ortaya çıktı. Ve sadece 1931'de, R. Kunu (Almanya) A. Winterstein (Almanya) ve E. Letterre (Fransa), Heidelberg'deki Tıbbi Araştırmalarda İmparator Wilhelm Enstitüsü, İmparatorluk Enstitüsü, Bu yöntemi ham karotenden A - ve B-karoten tahsis etmeyi başardı ve böylece renk açıklığının değerini gösterir.
Kromatografinin gelişiminde önemli bir aşama, Sovyet bilimcilerinin N.A'yı keşfedilmesiydi. Izmailov ve M.S. Schreiber kromatografi yöntemi ince bir katmanda (1938), maddenin mikrocolizmine sahip analizi sağlayan.
Bir sonraki önemli adım, A. Martin ve R. Sing (İngiltere), sıvı dağılım kromatografisinin varyantı, amino asitlerin asetil türevlerinin, silika jeli ile doldurulmuş, suyla doldurulmuş, su ile dolu, su ile dolu bir kolonun ayrılması üzerine bir çözücü olarak (1940). Aynı zamanda, sadece sıvının bir mobil faz olarak kullanılamayacağı, aynı zamanda gaz olarak kullanılabileceği belirtildi. Birkaç yıl sonra, bu bilim adamları, mobil faz olarak butanol ile su ile nemlendirilmiş amino asitlerin türevlerinin ayrılmasını yapmaları önerildi. Ayrıca ilk iki boyutlu ayırma sistemini uyguladılar. Kromatografinin dağıtım sürümünün açılması için Martin ve Sing, Nobel Ödülü'nü kimyada aldı. (1952). Ayrıca, Martin ve A. James, karışımın DS-550 silikon ve stearik asitten (1952 - 1953) arasındaki karışık bir sorbent üzerine ayıran bir gaz dağıtım kromatografisi varyantı gerçekleştirmiştir. Bu zamandan itibaren en yoğun gelişme, gaz kromatografi yöntemi ile elde edildi.
Gaz kromatografisi değişkenlerinden biri, gaz karışımının hareketli faz - gazın hareketi ile aynı anda ayrılmasını, sorbent'i ve ayrılmış karışımı, uzunluğu belirli bir gradyanı olan hareketli bir sıcaklık alanı ile etkilediği kromantografidir. AA Zhukhovitsky ve SOTR., 1951).
Kromatografik metodun gelişimine göze çarpan bir katkı, iyon değişim kromatografısinin kurucusu olan Schwab (Almanya) şehri tarafından tanıtıldı (1937 - 1940). Sovyet bilim adamlarının çalışmalarında daha fazla gelişme aldı. Gapona ve TB Çözeltideki iyonların bir karışımının kromatografik ayrımını gerçekleştiren Gapona (FM Shemyakin, 1947 ile birlikte) ve ayrıca çözünürlük çözünürlüğündeki farkı temel alan bir madde karışımının kromatografik ayrılması olasılığını da gerçekleştirmiştir. (Sedimanter kromatografi, 1948).
İyon değişim kromatografisi gelişmesindeki modern aşama, 1975'te, ION kromatografisi denilen yeni bir analitik yöntem (yüksek verimli bir seçenek) önerdikleri Sendla, T. Stevens ve W. Bauman'ın (ABD) çalışmalarından sonra başladı. İyon değişim kromatografisi ile konakometrik algılama ile).
Şirketin "Perkin-Elmer" M. Golley'in (ABD), chromatography'nin (1956) 'nın kılcal organlarının iç duvarlarına uygulanacağı, çok bileşenli karışımların mikrotizmasını analiz etmeyi sağlayan kromatografi (1956). Golley (ABD) oluşturulması.
60'ların sonunda. Sıvı kromatografisine ilgi arttı. Yüksek verimli sıvı kromatografisi (HPLC) vardı. Bu, son derece hassas dedektörlerin oluşturulmasıyla, yeni seçici polimer sorbentleri, yeni ekipman, yüksek basınçlarda çalışmasına izin vererek kolaylaştırılmıştır. Halen, HPLC, diğer kromatografi yöntemleri arasında lider bir pozisyon kaplar ve çeşitli versiyonlarda uygulanır.
Kromatografi, bileşenlerin iki faz-astar arasındaki dağılımına dayanan maddelerin ayrılması ve belirlenmesi yöntemidir. Sabit (sabit) faz, katı gözenekli bir maddeye (genellikle bir sorbent olarak adlandırılır) veya bir katıya uygulanan bir sıvı film sunar. Mobil faz, bazen basınç altında, sabit bir fazdan akan bir sıvı veya gazdır. Karışımın karışımının bileşenleri (çekirdek) hareketli fazda hareketli faz boyunca hareket eder. Genellikle sütun denilen bir cam veya metal tüp içine yerleştirilir. Sorbent yüzeyindeki etkileşim kuvvetine bağlı olarak (adsorpsiyon veya başka bir mekanizma nedeniyle), bileşenler kolon boyunca farklı hızlarda hareket eder. Bazı bileşenler, sorbentin üst katmanında kalacaktır, diğerleri, sorbent ile etkileşime giren, kolonun alt kısmında olacaktır ve bazıları kolonun hareketli faz ile birlikte bırakacağı (bu bileşenler ücretsizdir) Onların holding zamanları "ölü zaman" hoparlörleri belirler).
Böylece, karmaşık bileşen karışımlarının hızlı ayrılması meydana gelir.
Tarih açma:
Kromatografinin Doğuşu
Bu günün akşamı, Varşova Naturalistler Derneği Biyolojik Anabilim Dalı'nın bir toplantısında, Anatomi Anabilim Dalı Anatomisi ve Fizyoloji Fizyolojisi Anadilimi Mikhail Semenovich'in Asistanı "Bir Adsorpsiyon Fenomenası Kategorisinde ve Kullanımda bunların biyokimyasal analizine. "
Ne yazık ki, Botanik'in oluşumunda olan M.S. TSvet, açıklığının kimyasal analitik yönünü uygun şekilde takdir etmedi ve az miktarda çalışmalarını kimyasal dergilerde yayınladı. Daha sonra, önerilen M.S.'nin gerçek ölçeğini takdir eden kimyagiydi. Analitik kimyanın en yaygın yöntemi haline gelen kromatografik yöntemin rengi.
Kromatografik yöntemlerin aşağıdaki detayları vurgulanmalıdır:
1. Ayırma dinamiktir ve paylaşılan bileşenlerin emilim-desorpsiyonu eylemleri tekrarlanır. Bu, kromatografiklerin önemli ölçüde daha fazla verimliliğine neden olur.
statik sorpsiyon yöntemlerine kıyasla ayırma ve
Çıkarma.
2. Ayırma sırasında, şerbatların ve sabit fazların çeşitli etkileşimi türleri kullanılır: tamamen fizikselden hemosorpsiyondan.
Bu, geniş bir aralığın seçici olarak ayrılmasının olasılığına neden olur.
3. Ayrılmış maddelerde, ayrılma koşullarını değiştiren, kromatografi olanaklarını genişleten çeşitli ek alanları (yerçekimi, elektrikli, manyetik vb.) Uygulayabilirsiniz.
4. Kromatografi, birkaç bileşenin eşzamanlı ayrılmasını ve tanımını birleştiren hibrit bir yöntemdir.
5. Kromatografi, hem analitik görevleri (ayırma, tanımlama, tanım) ve hazırlayıcı (temizlik, seçim, konsantrasyon) çözmenizi sağlar. Bu görevleri çözmek, "çevrimiçi" modunda bunları gerçekleştirerek birleştirilebilir.
Çok sayıda yöntem, fazların toplam durumu, ayırma mekanizması ve ayrılma tekniği ile sınıflandırılır.
Kromatografik yöntemler, yürütme yönteminde farklılık gösterir
Ön, çok önemli ve eluent üzerindeki ayırma işlemi.
İyonik kromatografi
İyon kromatografisi, iyon değiştiricilere katyonları ve anyonları ayırmak için yüksek verimli sıvı kromatografisidir.
düşük kapasite. Yaygın iyon kromatografisi
avantajlarının sayısı nedeniyle:
- çok sayıda inorganik belirleme yeteneği ve
organik iyonlar, aynı anda katyonları tanımlar ve
- Tespitin yüksek hassasiyeti (olmadan 1 ng / ml'ye kadar)
ön konsantrasyon;
- Yüksek seçicilik ve ifade;
- Analiz edilen numunenin küçük hacmi (en fazla 2 ml numune);
- çok çeşitli tanımlanmış konsantrasyonlar (1 ng / ml
- Çeşitli dedektörleri ve kombinasyonlarını kullanma olasılığı, bu da seçicilik ve küçük zaman tanımı sağlamayı mümkün kılar;
- Tanımı tam olarak otomatikleştirebilme yeteneği;
- Çoğu durumda, ön örnek hazırlığının eksiksizliği.
Aynı zamanda, herhangi bir analitik yöntem olarak, iyon kromatografisi, aşağıdakilere atfedilebilecek eksikliklerden yoksun değildir:
- İyon eşanjörlerinin sentezinin karmaşıklığı, bu da büyük ölçüde karmaşıklaştırır
yöntemin geliştirilmesi;
- HPLC'ye kıyasla HPLC'ye kıyasla daha düşük bir ayrılık verimliliği;
- Yüksek Korozyon Dayanımı İhtiyacı
kromatografik sistem, özellikle belirlenirken
katyonlar.
2.1 Geliştirme Tarihi:
İyon değişim süreçlerinin incelenmesi XIX yüzyılın başında başladı. Toprakların bununla temas halinde tuz çözeltilerinin kimyasal bileşimi üzerindeki etkisi ile ilgili gözlemlerle. 1940'ların sonlarında, Tompson, toprağın amonyağı girilen organik gübrelerden emdiğini, ilgili deneylerin York D. Spence'in uzmanı tarafından yapıldığını belirtti. D. Spence deneylerinin ilk sonuçları, 1850'de G. Thompson tarafından yayınlandı. Makale, "Toprağın yüksek kaliteli özelliklerinin ilk keşfi, tarım için yararlı olamaz" ve son çalışması yayınlandı. 1852 ve 1855'te.
2.3 Sorpsiyon süreçlerinde iyonların ayrılmasının prensipleri
İyon değişim kromatografisi, mobil fazın bir sıvı (elüent) olduğu ve sabit bir fazın bir katı (iyon değiştirici) olduğu sıvı katı faz kromatografısini belirtir. İyon değişim kromatografisi yöntemi, sabit bir fazla ilişkili iyonların dinamik bir değiştirme işlemine dayanır, sütuna giren eluent iyonları. Ayırma, karışımdaki iyon iyon değişimi için farklı afinite nedeniyle oluşur, bu da kolon boyunca hareketlerinin farklı hızlarına yol açar.
İyon kromatografisi, bir sütun iyon değişim kromatografisi varyantıdır.
JUPAK (1993) önerilerine göre, iyon değişimi (IOC) ve iyonik (onların) kromatografisi terimleri aşağıdaki gibi tanımlanır. "İyon değişim kromatografisi, bireysel analiz edilen maddeler için iyon değişim etkileşimindeki farkına dayanır. İyonlar ayrılırsa ve bir iletken detektörü veya dolaylı UV tespiti kullanılarak tespit edilebiliyorsa, o zaman iyon kromatografisi denir."
Modern (2005) İfadeler: "İyon kromatografisi, kolonlarda iyonların tüm yüksek performanslı sıvı kromatografik (HPLC) ayrılmasını içerir, akış dedektöründe doğrudan algılama ve elde edilen analitik sinyallerin kantitatif işlenmesi ile birlikte." Bu tanım, iyon kromatografisini ayrılma mekanizmasına ve algılama yöntemine atıfta bulunmadan karakterize eder ve böylece klasik iyon değişiminden ayrılır.
İyon kromatografisinde aşağıdaki ayırma prensipleri uygulanır:
İyon değişimi.
İyon çiftlerinin eğitimi.
Dışlama iyonları.
İyon değişimi
İyon değişimi, iyonat fazında (sezonlar), elüentin sendikalarındaki eşdeğer iyonizasyon iyonlarının geri dönüşümlü bir heterojen tepkisidir. Anti-AntiAnons, elektrostatik kuvvetlerin pahasına olan fonksiyonel Ionets grupları tarafından tutulur. Kural olarak, katyonik kromatografide bu gruplar sülfonik asit gruplarıdır; Anyonik kromatografi durumunda - Kuaterner amonyum zeminler. İncirde. Şekil 1, katyon ve anyonların değişim sürecinin şemasını göstermektedir. Belirlenen maddenin iyonları, değişim merkezleri için onlarla rekabet eden eluent iyonları olarak işaretlenmiştir - E.

İncir. 1. Fonksiyonel Sülfo Grupları - SO3- ve Anyon Eşanjörü (Kuaterner Amonyum Bankası) içeren bir katyon eşanjörünün katılımıyla (A +) ve Anyonlar (A-+) ve Anyonlar (A-) takas değişimi (Kuaterner amonyum tabanı) Gruplar -N + R3).
İyon par
Bu ayırma mekanizmasını uygulamak için, elüent çözeltisine eklenen iyon eşleştirilmiş reaktifler kullanılır. Bu tür reaktifler, anyonik veya katyonik yüzey aktif cisimleri, örneğin alkil sülfonik asitler veya tetraalklamonyum tuzlarıdır.
Karşı yüklü iyon tanımlı iyonlarla birlikte, bu iyon çifti reaktifinin iyonları, intermoleküler etkileşimler nedeniyle sabit fazda tutulabilen, sabit fazda tutulabilen tahsil edilemez bir iyonik çift oluşturur. Ayırma, iyonik çiftlerin oluşumunun sabitlerindeki farklar ve sorbent matrisindeki adsorpsiyon derecelerinin farkları nedeniyle gerçekleştirilir. İncirde. Şekil 2, reaktifin sabit fazdaki adsorpsiyonundan sonra iyon çift kromatografisinde statik bir iyon değişim modelini göstermektedir. Bu ayırma prensibi hem anyonlar hem de katyonlar için kullanılır.

İncir. 2.. İyon-buhar kromatografisinde iyon değişim modeli.
İyonik hariç tutma
İyonkgüzyon kromatografisi (IEX). Temel olarak, zayıf asitleri veya bazları ayırmak için kullanılır. IEX'in en büyük değeri, karboksilik ve amino asitleri, fenolleri, karbonhidratları belirlemelidir.
İncirde. Şekil 3, R-CoOH asitleri örneğinde IEX kullanarak ayrılma ilkesini göstermektedir.
İncir. 3. İyonoecklusion kromatografisi kullanılarak R-CoOH karboksilik asit ayırma şeması.

Sabit bir faz olarak ionoeckskoluzion kromatografisinde, iyon suyu (süvari) içeren tamamen sümüklü bir katyon eşanjörü kullanılır. Sulu bir elüent çözeltisinde, sülfonik asit iyonis grupları nemlendirilir. Hidrat kabuğu, hayali olumsuz yüklü bir membranla (Donnan membran) ile sınırlıdır. Membran, yalnızca pürüzsüz olmayan moleküller için geçirgendir (örneğin, su).
Güçlü mineral asitler eluent olarak kullanıldığında organik karboksilik asitler ayrılabilir. Asitlik sabitlerinin düşük değerleri nedeniyle, haksız formda bu tür çözümlerde karboksilik asitler bulunur. Bu formlar Donnan membranından geçebilir ve sabit fazda adsorbe edilebilir.
Bilgi tabanında iyi çalışmanızı göndermeniz basittir. Aşağıdaki formu kullanın
Öğrenciler, lisansüstü öğrenciler, bilgi tabanını çalışmalarında kullanan genç bilim adamları ve çalışmaları size minnettar olacak.
tarafından gönderildi http://www.allbest.ru.
1. Kromatografinin açılış ve gelişmesinin tarihçesi
2. Temel Hükümler
3. Kromatografik analiz yöntemlerinin sınıflandırılması
4. Adsorpsiyon kromatografisi. İnce tabaka kromatografisi
4.1 İnce katman kromatografisinde deney tekniği
5. Gaz Kromatografisi
5.1 Gaz-Adsorpsiyon Kromatografisi
5.2 Gaz-Sıvı Kromatografisi
6. Dağıtım kromatografisi. Kağıt kromatografisi
7. Tortu kromatografisi
7.1 Deneme tekniği üzerinde tortul kromatografi yöntemlerinin sınıflandırılması
7.2 Kağıt üzerinde tortu kromatografisi
8. İyon değişim kromatografisi
Sonuç
Bibliyografi
1. TARİHKromatografi Keşifleri ve Geliştirme
Kromatografi bir Rus bilim adamı, botanik ve fizikokemist Mikhail semenovich rengidir.
Kromatografinin keşfi, Master'ın St. Petersburg'da (1900 - 1902) ve Varşova'daki ilk çalışmaların ilk döneminde (1902 - 1903) çalışmalarının tamamlanmasının zamanını ifade eder. Bitkilerin pigmentlerini keşfetmek, renk, bir adsorban tozlu kalsiyum karbonat ile doldurulmuş tüpten pigmentlerin renginde çok az farklılaştı ve daha sonra net bir çözücü ile adsorbanı yıkandı. Karışımın ayrı bileşenleri bölünmüş ve renkli çizgiler oluşturulmuştur. Modern terminolojiye göre, renk, kromatografinin gelişen varyantını keşfetti (sıvı adsorpsiyon kromatografisi geliştirme). Onun tarafından yaratılan kromatografinin gelişimi konusundaki araştırmanın temel sonuçları. Doktora tezi olan "Bitki ve Hayvan Dünyasında Kromofiller" (1910) kitabında belirtilen renk. Kromatografi Gazı Sedimanter İyon Değişimi
Renk, sadece karışımın ayrılması için değil, kromatografik yöntemi, karışımın ayrılması için değil, aynı zamanda kantitatif analiz için de kullandı, bunun için cam kolonunu kırdı ve adsorban kolonunu katmanlara kesti. Renk, sıvı kromatografi için ekipman geliştirmiştir, ilk kez indirgenmiş basınç altında kromatografik işlemler (pompalama) ve bazı aşırı basınçlarda, verimli sütunların hazırlanması için geliştirilen önerilerde bulundu. Buna ek olarak, "kromatografi", "tezahür", "yer değiştirme", "kromatogram", vb. Gibi yeni bir yöntemin birçok temel kavramını ve şartını tanıttı.
Kromatografi ilk olarak çok nadiren kullanılmıştır, gizli süresi yaklaşık 20 yıl sürdü, bu sırada yöntemin çeşitli uygulamaları hakkında sadece çok az sayıda mesaj ortaya çıktı. Ve sadece 1931'de, R. Kunu (Almanya) A. Winterstein (Almanya) ve E. Letterre (Fransa), Heidelberg'deki Tıbbi Araştırmalarda İmparator Wilhelm Enstitüsü, İmparatorluk Enstitüsü, Bu yöntemi ham karotenden A - ve B-karoten tahsis etmeyi başardı ve böylece renk açıklığının değerini gösterir.
Kromatografinin gelişiminde önemli bir aşama, Sovyet bilimcilerinin N.A'yı keşfedilmesiydi. Izmailov ve M.S. Schreiber kromatografi yöntemi ince bir katmanda (1938), maddenin mikrocolizmine sahip analizi sağlayan.
Bir sonraki önemli adım, A. Martin ve R. Sing (İngiltere), sıvı dağılım kromatografisinin varyantı, amino asitlerin asetil türevlerinin, silika jeli ile doldurulmuş, suyla doldurulmuş, su ile dolu, su ile dolu bir kolonun ayrılması üzerine bir çözücü olarak (1940). Aynı zamanda, sadece sıvının bir mobil faz olarak kullanılamayacağı, aynı zamanda gaz olarak kullanılabileceği belirtildi. Birkaç yıl sonra, bu bilim adamları, mobil faz olarak butanol ile su ile nemlendirilmiş amino asitlerin türevlerinin ayrılmasını yapmaları önerildi. Ayrıca ilk iki boyutlu ayırma sistemini uyguladılar. Kromatografinin dağıtım sürümünün açılması için Martin ve Sing, Nobel Ödülü'nü kimyada aldı. (1952). Ayrıca, Martin ve A. James, karışımın DS-550 silikon ve stearik asitten (1952 - 1953) arasındaki karışık bir sorbent üzerine ayıran bir gaz dağıtım kromatografisi varyantı gerçekleştirmiştir. Bu zamandan itibaren en yoğun gelişme, gaz kromatografi yöntemi ile elde edildi.
Gaz kromatografisi değişkenlerinden biri, gaz karışımının hareketli faz - gazın hareketi ile aynı anda ayrılmasını, sorbent'i ve ayrılmış karışımı, uzunluğu belirli bir gradyanı olan hareketli bir sıcaklık alanı ile etkilediği kromantografidir. AA Zhukhovitsky ve SOTR., 1951).
Kromatografik metodun gelişimine göze çarpan bir katkı, iyon değişim kromatografısinin kurucusu olan Schwab (Almanya) şehri tarafından tanıtıldı (1937 - 1940). Sovyet bilim adamlarının çalışmalarında daha fazla gelişme aldı. Gapona ve TB Çözeltideki iyonların bir karışımının kromatografik ayrımını gerçekleştiren Gapona (FM Shemyakin, 1947 ile birlikte) ve ayrıca çözünürlük çözünürlüğündeki farkı temel alan bir madde karışımının kromatografik ayrılması olasılığını da gerçekleştirmiştir. (Sedimanter kromatografi, 1948).
İyon değişim kromatografisi gelişmesindeki modern aşama, 1975'te, ION kromatografisi denilen yeni bir analitik yöntem (yüksek verimli bir seçenek) önerdikleri Sendla, T. Stevens ve W. Bauman'ın (ABD) çalışmalarından sonra başladı. İyon değişim kromatografisi ile konakometrik algılama ile).
Şirketin "Perkin-Elmer" M. Golley'in (ABD), chromatography'nin (1956) 'nın kılcal organlarının iç duvarlarına uygulanacağı, çok bileşenli karışımların mikrotizmasını analiz etmeyi sağlayan kromatografi (1956). Golley (ABD) oluşturulması.
60'ların sonunda. Sıvı kromatografisine ilgi arttı. Yüksek verimli sıvı kromatografisi (HPLC) vardı. Bu, son derece hassas dedektörlerin oluşturulmasıyla, yeni seçici polimer sorbentleri, yeni ekipman, yüksek basınçlarda çalışmasına izin vererek kolaylaştırılmıştır. Halen, HPLC, diğer kromatografi yöntemleri arasında lider bir pozisyon kaplar ve çeşitli versiyonlarda uygulanır.
2. Temel hükümler
Kromatografi, bileşenlerin iki faz - hareketli ve sabit arasındaki dağılımına dayanan maddelerin ayrılması ve belirlenmesi yöntemidir. Sabit (sabit) faz, katı gözenekli bir maddeye (genellikle bir sorbent olarak adlandırılır) veya bir katıya uygulanan bir sıvı film sunar. Mobil faz, bazen basınç altında, sabit bir fazdan akan bir sıvı veya gazdır. Karışımın karışımının bileşenleri (çekirdek) hareketli fazda hareketli faz boyunca hareket eder. Genellikle sütun denilen bir cam veya metal tüp içine yerleştirilir. Sorbent yüzeyindeki etkileşim kuvvetine bağlı olarak (adsorpsiyon veya başka bir mekanizma nedeniyle), bileşenler kolon boyunca farklı hızlarda hareket eder. Bazı bileşenler, sorbentin üst katmanında kalacaktır, diğerleri, sorbent ile etkileşime giren, kolonun alt kısmında olacaktır ve bazıları kolonun hareketli faz ile birlikte bırakacağı (bu bileşenler ücretsizdir) Onların holding zamanları "ölü zaman" hoparlörleri belirler). Böylece, karmaşık bileşen karışımlarının hızlı ayrılması meydana gelir. Kromatografik yöntemlerin aşağıdaki detayları vurgulanmalıdır:
1. Ayırma dinamiktir ve paylaşılan bileşenlerin emilim-desorpsiyonu eylemleri tekrarlanır. Bu, statik emilim ve ekstraksiyon yöntemlerine kıyasla kromatografik ayrımın önemli ölçüde daha fazla verimliliğine neden olur.
2. Ayırma sırasında, şerbatların ve sabit fazların çeşitli etkileşimi türleri kullanılır: tamamen fizikselden hemosorpsiyondan. Bu, geniş bir madde çemberinin seçici olarak ayrılmasının olasılığına neden olur.
3. Ayrılmış maddelerde, ayrılma koşullarını değiştiren, kromatografi olanaklarını genişleten çeşitli ek alanları (yerçekimi, elektrikli, manyetik vb.) Uygulayabilirsiniz.
4. Kromatografi, birkaç bileşenin eşzamanlı ayrılmasını ve tanımını birleştiren hibrit bir yöntemdir.
5. Kromatografi, hem analitik görevleri (ayırma, tanımlama, tanım) ve hazırlayıcı (temizlik, seçim, konsantrasyon) çözmenizi sağlar. Bu görevlerin çözümü, "on line" modunda gerçekleştirilerek birleştirilebilir.
6. Çok sayıda yöntem, fazların toplam durumu, ayırma mekanizması ve ayırma tekniği ile sınıflandırılır. Kromatografik yöntemler, ayırma işlemini ön, pota ve eluent olarak yürütme yönteminde farklılık gösterir.
3. Kromatografik Analiz Yöntemlerinin Sınıflandırılması
Kromatografik yöntemlerin oluşumları, ayrılma işleminin aşağıdaki farklı özelliklerini dikkate alan ilkelere dayanmaktadır:
* Kullanılan kromatografik sistemin aşamalarının toplam durumundaki farklılıklar;
* Ayrılmış maddelerin sabit fazlı etkileşimlerinin niteliğindeki farklılıklar;
* Kromatografik ayrılma işlemi için yöntemlerde deneysel farklılıklar.
Tablo 1? 3, bilinen kromatografik yöntemlerin sınıflandırılmasının temel çeşitlerini göstermektedir.
Ayrılmış bileşiklerin etkileşimlerinin çeşitli kromatografik sistemlerin aşamaları ile etkileşimlerinin niteliği büyük ölçüde değişebilir, neredeyse hiçbir nesne bulunmadığından, uygun bir sabit faz (katı veya sıvı) ve yuvarlanma solventi bulmak mümkün olmayacağı için neredeyse hiç nesne yoktur. sistemler. Çalışma altındaki bileşiklerin moleküler ağırlığına bağlı olarak temel kromatografi varyantlarının kapsamı tabloda verilmiştir. dört.
4. Adsorpsiyon kromatografisi. İnce tabaka kromatografisi
En yaygın adsorpsiyon kromatografi tekniklerinden biri, ince tabaka kromatografisi (TLC) - adsorbanın plaka üzerinde ince bir tabaka olarak kullanıldığı bir tip düzlem kromatografisidir.
TLC yönteminin prensibi ve temel kavramları. Temiz bir düz yüzeyde (cam, metal, plastik tabağı) tek yönde veya başka bir şekilde, çoğu zaman plakanın yüzeyine sabitlenir, bu da ıstırabın ince bir tabakası uygulanır. Plakanın boyutları farklı olabilir (uzunluk ve genişlik - gerekli olmasa da, 5 ila 50 cm'den). Plakanın yüzeyinde, dikkatlice, başlangıç \u200b\u200bçizgisinin (örneğin, bir kalem) özetlenen (örneğin, plakanın alt kenarından 2-3 cm mesafede) ve hattı Solvent bitirmek.
Bileşenlerin A ve TLC yönteminde ayrılması şeması
Başlangıç \u200b\u200bçizgisinde, plaka (mikro-gömlek, kılcal) numune ile uygulanır - bir ayrılabilir maddelerin bir karışımını içeren az miktarda sıvı, örneğin, iki maddelik A ve B uygun bir çözücü içinde kullanılır. Çözücüyü buharlaştırmak mümkündür, bundan sonra plaka, özel olarak seçilmiş bir çözücü veya belirli bir durum için bir çözücü karışımı olan PF'nin sıvı fazında kromatografik odaya batırılır. PF'nin kılcal kuvvetlerinin etkisi altında, nF'yi başlangıç \u200b\u200bçizgisinden solvent cephesinin çizgisine kadar, bunlarla farklı hızlarda hareket eden örneklerde özen gösteren NF boyunca hareket eder. Bu durumda, A'dan NF'nin bileşeninin afinitesi, B bileşeninin aynı fazı için daha az afinitedir, bu nedenle A bileşeni B bileşeninden daha hızlı hareket eder. Solvent hattının hareketli fazına (çözücü) ulaştıktan sonra, Kromatografi kesilir, plaka kromatografik hazneden çıkarılır, havada kurutulur ve a ve içine plakanın yüzeyinde bulunan maddelerin lekelerini belirleyin. Noktalar (bölgeler) genellikle oval veya yuvarlak bir şekle sahiptir. Dikkate alınmadıkça, leke bileşeni bir başlangıç \u200b\u200bsatırından mesafeye taşındı l. A. , nokta bileşeni - mesafe için l. İÇİNDEve çözücü mesafeden geçti L..
Bazen aynı anda, başlangıç \u200b\u200bçizgisindeki ayrılmış maddelerin örneklerinin uygulanmasıyla aynı anda, standart standardın standartlarının yanı sıra tanık maddelerinin yanı sıra (analiz edilen numunede bulunduğu iddia edilenler) uygulanır.
Paylaşılan bileşenleri karakterize etmek için, sistemde RF mobilitesi (veya RF faktörü) tanıtılır:
R. f.\u003d V. 1 / V. E.\u003d (L. 1 / T) / (L / T) \u003d L 1 / L. ,
nerede V. 1 = l. 1 / t. ve V. E.= L./ t. - buna göre hareket hızı bEN.- th bileşeni ve çözücü E; l. 1 veL. - yol geçti bEN.- sırasıyla bileşen ve çözücü, t çözücüyü başlangıç \u200b\u200bhattından solvent ön hattına taşımak için gereken süredir. Mesafe l. 1 başlangıç \u200b\u200bçizgisinden, karşılık gelen bileşenin yerinin merkezine sıkın.
Genellikle, hareketlilik katsayısı yeniden dağıtımda yatıyor R. f. =0 - 1. Optimum değer 0.3-0.7, kromatografi koşulları seçilir, böylece R f değerinin sıfırdan ve birimlerden farklı olmasıdır.
Mobilite katsayısı, sorbent sorbat sisteminin önemli bir özelliğidir. Tekrarlanabilir ve kesinlikle sabit kromatografi koşulları için R. f. = sabit.
RF mobilite katsayısı, bir dizi faktöre bağlıdır: çözücünün doğası ve niteliği, saflığı; Sorbent (ince tabaka), tanelerinin homojenliği, tabaka kalınlığı; sorbent'in aktivitesi (içten içeriği nem); deney teknikleri (kütle örnekleri, çözücünün ayın uzunluğu); Deneyatör beceri vb. Tüm bu parametrelerin pratikte çoğaltılmasının sabitliği bazen zordur. Sürecin koşullarının etkisini düzleştirmek için, göreceli hareketlilik faktörü tanıtılır Rs..
Rs \u003d l / l sanat\u003d R. f./ R. f ( sanat ) ,
nerede R. f. = l./ L.; R. f. (ST)= l. sanat/ L.; l. santimetre. - başlangıç \u200b\u200bçizgisinden standart noktanın ortasına olan mesafe.
RS Mobility'nin göreceli katsayısı, maddenin hareketliliğinin hareketlilik katsayısından daha objektif bir özelliğidir.
Standart olarak, böyle bir madde genellikle bu koşullarda R F olarak seçilir mi? 0.5. Kimyasal doğada, standart ayrılmış maddelere yakın seçilir. Standart kullanarak, RB'nin değeri genellikle Rs \u003d 0.1--10 içinde yatıyor, optimum limitler yaklaşık 0.5--2'dir.
Paylaşılan bileşenlerin daha güvenilir bir şekilde tanımlanması için, "tanıklar" - referans maddeleri, varlığı analiz edilen numunede varsayılır. R f \u003d r F (SvID) ise, sırasıyla R F ve R F (SVID) - bu bileşenin hareketliliğinin katsayıları ve bir tanık, daha sonra en büyük olasılıkla test maddesinin kromatografik karışımda bulunduğunu varsayabilir.
İki bileşenin ayrılmasını karakterize etmek için A ve bu koşullarda, R (A / B) ayrılmasının derecesi (kriteri) getirilir:
R (a / b) \u003d D l.(\u003d 2d l. ,
d nerede. l. - A ve B bileşenlerinin merkezleri arasındaki mesafe; A (A) ve A (B) - sırasıyla, A ve B noktalarının çapları kromatogramda.
R (a / b) değeri ne kadar büyükse, A ve B bileşenlerinin lekelerinin lekeleri kromatogramda ayrılır.
A ve B iki maddenin ayrılmasının seçiciliğini tahmin etmek için ayırma katsayısını kullanın. fakat:
a \u003d.l. B. / l. A.
Eğer bir a \u003d 1,a ve B bileşenlerinin bölünmemesidir.
A ve V bileşenlerinin ayrılması (A / B) derecesini belirlemek.
4.1 İnce tabaka kromatografisinde deneysel teknik:
fakat) Örnek uygulama. Analiz edilen sıvı numune, kılcal, mikro-bok, mikropipetler, sorbent katmanına dikkatlice dokunmadan başlama çizgisine uygulanır (başlangıç \u200b\u200bçizgisindeki lekenin çapı genellikle bir ila birkaç milimetredir). Başlangıç \u200b\u200bçizgisine birkaç numune uygulanırsa, başlangıç \u200b\u200bhattındaki numunelerin lekeleri arasındaki mesafe 2 cm'den az olmamalıdır. Mümkünse, konsantre çözeltiler kullanılır. Noktalar havada kurutulur, ardından kromatografi yapılır.
b) Kromatogramın gelişimi (kromatografi).İşlem, PF olarak kullanılan çözücü çiftleriyle doymuş kapalı kromatografik odalarda, örneğin bir kapağın üstüne kaplı bir cam kapta yapılır.
Hareketin yönüne bağlı olarak, PF ayırt edilir artan azalan ve yatay kromatografi.
Yükselen kromatografi formunda, sadece sabit bir sorbent tabakalı plakalar kullanılır. PF, haznenin altına dökülür (ikincisi, bir cam kapaklı bir cam kimyasal bardak kullanılabilir), kromatografik plaka, odaya dikey olarak veya eğik olarak yerleştirilir, böylece pf tabakası Kamera plakanın altını ıslatır (başlangıç \u200b\u200bçizgisinin altında ~ 1.5 - 2 cm). PF, kılcal kuvvetlerin dipten (yerçekimine karşı) nispeten yavaşça hareket etmesi nedeniyle hareket eder.
Azalan kromatografi varyantı içinde, sadece sabit bir tabakalı plakalar da geçerlidir. PF yukarıdan beslenir ve plaka sorbent katmanı boyunca aşağı doğru hareket eder. Yerçekimi gücü PF'nin hareketini hızlandırır. Bu düzenleme, bileşen içeren karışımları analiz ederken, yavaşça PF ile hareket ederken uygulanır.
Yatay kromatografi düzenlemesinde, plaka yatay olarak yerleştirilir. Dikdörtgen veya yuvarlak plakalar kullanabilirsiniz. Yuvarlak plakalar uygularken (yatay kromatografinin dairesel varyantı), başlangıç \u200b\u200bçizgisi, örneklerin uygulandığı uygun bir yarıçapın (~ 1.5-2 cm) bir dairesi olarak gösterilir. Yuvarlak plakanın ortasında, delik, fitilin PF'ye eklendiği şekilde kesilir. İkincisi, çemberin ortasından çevresinin ortasından çember katmanı boyunca hareket eder. Kromatografi, kapalı bir odada - kurutucuda veya Petri Ocaklarında gerçekleştirilir. Dairesel bir versiyonla, birkaç düzine örneğini eşzamanlı olarak analiz edebilirsiniz.
TLC yöntemlerinde, tek boyutlu, iki boyutlu, çoklu (Re-), step kromatografi kullanılır.
Bir kerelik kromatografide, analiz PF'nin hareket yönünü değiştirmeden gerçekleştirilir. Bu yöntem en yaygın.
İki boyutlu kromatografi genellikle karmaşık karışımları (proteinler, amino asitler vb.) Analiz etmek için kullanılır, karışım ilk önce ilk PF 1 kullanılarak gerçekleştirilir. Kromatogram, bireysel maddeler değil, birkaç ayrılmaz bileşenin karışımlarını elde edilir. Daha sonra, bu lekeler aracılığıyla, plaka 90 ° açılır ve tekrar kromatografiye tabi tutulur, ancak zaten ikinci PF 2 ile birlikte, lekeleri bireysel bileşenlerin lekelerinin lekeleri ile karıştırmaya çalışır.
Plaka kare ise, numune bu karenin köşegenine alt köşesine yakındır. Bazen iki boyutlu kromatografi, kare bir plaka üzerinde aynı pf ile gerçekleştirilir.
İki boyutlu kromatografi ilkesini gösteren şema:
a - PF1'den elde edilen kromatogram;
b - PF2'den elde edilen kromatogram
Çoklu (yeniden) kromatografide, işlem, karışım bileşenlerinin lekelerinin (genellikle - üç kereden fazla) olan (genellikle - üç kez) ayrılmasına kadar, aynı PF'den (her seferinde - bir sonraki kurutmadan sonra) birkaç kez sırayla birkaç kez gerçekleştirilir.
Basamak kromatografisi durumunda, işlem, temiz bir lekeye ulaşılana kadar, her seferinde her seferinde yeni bir PF kullanılarak aynı plakayla birlikte yapılır.
içinde) Kod çözme kromatogramları. Kromatogramdaki lekeler boyanırsa, plakaları kurutduktan sonra, başlangıç \u200b\u200bçizgisinden her noktanın ortasına olan mesafeyi belirleyin ve hareketlilik katsayılarını hesaplar. Analiz edilen numunenin bileşimi renksiz maddelerden oluşursa, boyasız, yani Kromatogramdaki görsel olarak belirlenmiş lekeler, harcamanız gerekir tespit etme hangi kromatogram için bu noktalar göstermek.
En yaygın algılama yöntemleri aşağıda açıklanmıştır.
Ultraviyole ışığı ile ışınlama.Floresan bileşikleri tespit etmek için kullanılır (Noktalar, UV ışık plakasının ışınımı sırasında parlayandır) veya petroliyoliyüler maddeler, ancak bir flüoresan göstergeli bir sorbent kullanmak (sorbent yanar, lekeler yanmaz). Böylece, örneğin alkaloitler, antibiyotikler, vitaminler ve diğer tıbbi maddeler tespit edildi.
Isı tedavisi.Plaka kromatografisinden sonra kurutulduktan sonra (~ 200 ° C'ye kadar), sorbentin kendisinin kararmasını önler (örneğin, sorbentin ince tabakası nişasta içerdiğinde). Aynı zamanda, lekeler genellikle kahverengi bölgeler biçiminde (organik bileşenlerin kısmi termasyonu nedeniyle) ortaya çıkmıştır.
Kimyasal işlem.Genellikle kromatogramlar sergiler, bunları, karışımların paylaşılan bileşenleriyle renkli bileşikler oluşturan reaktiflerle işleme koyar. Bu amaçlar için, çeşitli reaktifler kullanılır: bir çift iyot, amonyak, brom, kükürt dioksit, hidrojen sülfit, plakalarla tedavi edilen özel hazırlanmış çözeltiler. Hem evrensel hem de seçici reaktifleri uygulayın ("evrensel" kavramı yeterince şartlıdır).
Evrensel reagentamimogoot, örneğin konsantre sülfürik asit (ısıtıldığında, organik bileşiklerin karartması var), ekşi sulu bir potasyum permanganat çözeltisi (mor bir sorbent arka plan üzerinde kahverengi lekeler şeklinde), bir çözeltisi, Isıtma sırasında fosfor-molibden asit (mavi lekeler sarı arka planda görünür), vb.
Seçici kullanım olarak, örneğin, Dragendorf'un reaktifi; Zimmerman Reaktifi; Bakır sülfatın sulu amonyum çözeltisi (cuso'nun% 10'u, amonyada% 2,% 2'si); Etanol ve asetik asit ile ninhidrin C9 H4 o 3 H20 karışımı.
Dragandorf reaktifi, ana Bondo 3 yapıştırma nitrat, KJ potasyum iyodür ve sudaki asetik asidin bir çözeltisidir. Aminleri, alkaloitler, steroidleri belirlemek için kullanılır.
Zimmerman reaktifi, Alkali Solüsyonu KOH% 2 etanol çözeltisinin, ardından karışımın ~ 70-100 ° C'de ısıtılmasıyla hazırlanır. Steroidleri tespit etmek için başvurun.
Ningidrin'in yardımıyla, aminlerin lekeleri, amino asitler, proteinler ve diğer bağlantılar tespit edilir.
Spotların diğer bazı yolları kullanılmaktadır. Örneğin, radyoaktiviteleri, radyoaktiflerin ayrılan bileşenlerinin bir kısmı, karışımın ayrılmış bileşenlerinin bir parçası olan elemanların özel katkı maddeleri eklenmesi durumunda ölçülür.
Kromatogramdaki lekeleri tespit ettikten sonra, tanımlanırlar, yani. Bileşiğin buna veya bu noktaya karşılık geldiği belirlenir. Bu amaçla, "tanıkların" referans noktaları en sık kullanılır. Bazen lekeler, hareketlilik katsayılarının büyüklüğü ile tanımlanır ve bunları bu koşullar için bilinen R F'nin değerleriyle karşılaştırır. Bununla birlikte, R F'nin bu tür tanımlanması genellikle öndir.
Floresan lekelerinin rengi de tanımlama amacıyla kullanılır, çünkü çeşitli bileşikler çeşitli dalga boylarının (farklı renklerde) radyasyonla floresan olduğu içindir.
Noktaların kimyasal olarak tespit edilmesiyle, seçici reaktifler, tanımlama amacıyla da kullanılan belirli doğa bileşikleriyle boyanmış lekeler verir.
TLC yönteminin yardımıyla, yalnızca açılamaz, aynı zamanda bileşenlerin içeriğini karışımlardaki içeriğini ölçemezsiniz. Bunu yapmak için, kromatogramdaki lekeler analiz edilir veya kromatogramdan ayrılan bileşenler bir şekilde veya başka bir şekilde çıkarılır (ekstraksiyon, uygun çözücüler ile elüsyon).
Analiz edildiğinde, lekeler, lekeler alanı ile bu maddenin içeriği (örneğin, bir orantılı veya doğrusal bir bağımlılığın varlığı), bir mezuniyet grafiği oluşturma yöntemi ile oluşturulan, bu maddenin içeriği (örneğin, orantılı veya doğrusal bir bağımlılığın varlığı) arasında belirli bir bağlantının varlığını ima eder. "Şahitler" nin lekeleri, bileşenin bilinen bir içeriğiyle analiz ediliyor.
Bazen, lekelerin renginin yoğunluğunu karşılaştırırlar, renk lekelerinin yoğunluğunun bu boyalı bileşenin sayısıyla orantılı olduğuna inanıyorlar. Yoğunluğu ölçmek için, farklı teknikler kullanılır.
Ayrılmış bileşenleri kromatogramdan çıkarırken, bu bileşeni içeren bir çözelti elde edilir. İkincisi daha sonra bir veya başka bir analitik yöntemle belirlenir.
Maddenin TLC tarafından kantitatif olarak belirlenmesinin göreceli hatası% 5-10'dur.
TLC bir farmakope yöntemidir ve çeşitli ilaçların kalitesini analiz etmek ve kontrol etmek için yaygın olarak kullanılır.
5. Gaz kromatografisi
Gaz kromatografisinde (GC), gaz taşıyıcı adı verilen inert gaz (azot, helyum, hidrojen) mobil faz olarak kullanılır. Numune, bir buhar formunda beslenir, sabit bir faz servisi veya bir katı - bir sorbent (gaz-adsorpsiyon kromatografisi) veya katı bir taşıyıcı üzerinde ince bir tabaka (gaz-sıvı kromatografisi) uygulanan yüksek kaynar bir sıvı. Gaz-sıvı kromatografisi (GLC) seçeneğini düşünün. KIZELGUR (diatomit) bir taşıyıcı olarak kullanılır - bir tip hidratlanmış silika jel kullanılır, genellikle Si-OH gruplarını SI-O-O-O-OR grubundaki (CH3) 3'teki (CH3) 3'teki ( Solventlere göre taşıyıcı. Bunlar, örneğin, "kromosorb W" ve "gasohromq" taşıyıcılarıdır. Ayrıca, cam mikrosistler, teflon ve diğer malzemeler kullanılır.
5.1 Gazze- adsorpsiyon kromatografisi
Gaz pompası kromatografisi (GA) yönteminin tuhaflığı, sabit bir faz, yüksek spesifik bir yüzeye olan adsorbanlar (10-1000 m2 g -1) kullanılır ve sabit ve hareketli fazlar arasındaki maddelerin dağılımıdır. adsorpsiyon süreci tarafından belirlenir. Moleküllerin gaz fazından adsorpsiyonu, yani. Katı ve gaz aşamalarının ayrılmasının yüzeyinde konsantre edilmiş, elektrostatik yapıya sahip olan moleküler etkileşimler (dispersiyon, oryantasyon, indüksiyon) nedeniyle oluşur. Hidrojen bağlarının oluşumu mümkündür ve bu tür etkileşimin tutulan hacimlere katkısı, artan sıcaklık ile önemli ölçüde azaltılır.
Analitik uygulama için, sabit bir sıcaklıkta, yüzeydeki adsorbe edilen madde miktarı, bu maddenin bu maddenin konsantrasyonu ile m ile orantılı olduğu önemlidir:
C. s. = kC. m. (1)
şunlar. böylece dağılımın adsorpsiyonun doğrusal izotermine uygun olarak gerçekleşmesi (için - Sabit). Bu durumda, her bir bileşen, konsantrasyonundan bağımsız olarak sabit bir hızda sütun boyunca hareket eder. Maddelerin ayrılması, hareketlerinin farklı hızlarından kaynaklanmaktadır. Bu nedenle, adsorbanın, alanın ve yüzeyinin belirli bir sıcaklıkta seçiciliği (ayırma) belirleyen niteliğin seçimi, boşluklarda son derece önemlidir.
Adsorpsiyonun ısısı artan sıcaklıkla azalır DH / T.hangi algılama bağlıdır ve buna göre t. R. . Bu, analiz uygulamasında kullanılır. Bileşikler, sürekli bir sıcaklıkta oynaklığın yüksek oranda farklılaşması durumunda, düşük kaynama maddeleri hızlı bir şekilde elüe edilir, yüksek kaynamış, kromatogramdaki tepe noktaları daha düşük ve daha geniş olacaktır, analiz çok fazla zaman alır. Kromatografi işleminde, sütunun sıcaklığını sabit bir hız (sıcaklık programlaması) ile arttırırsa, kromatogram üzerindeki genişlikte kapanır zirveler eşit yerleştirilecektir.
GI için adsorbanlar, aktif kömürler, silika jeller, gözenekli cam, alüminyum oksit esas olarak kullanılır. Aktif adsorbanların yüzeyinin inhomojenitesi, GAH yöntemlerinin temel dezavantajlarından ve yüksek adsorbe edilen polar moleküllerin belirlenmesinin imkansızlığından kaynaklanmaktadır. Bununla birlikte, geometrik olarak ve kimyasal olarak homojen makro gözenekli adsorbanlar üzerinde, güçlü polar maddelerin karışımlarını analiz etmek mümkündür. Son yıllarda, yakın zamanda, gözenekli polimerler, makro gözenekli silika jeller (Satlohrom, vurulmuş, sprey), gözenekli gözlük, zeolitler gibi az ya da çok homojen bir yüzeye sahip adsorbanlar üretir.
En çok geniş gaz pompası kromatografisi yöntemi, gazların karışımlarını analiz etmek için ve aktif fonksiyonel gruplar içermeyen düşük kaynar hidrokarbonları analiz etmek için kullanılır. Bu tür moleküllerin adsorpsiyon izotermleri doğrusaldır. Örneğin, 2, N2, CO, CH4, CO2'nin ayrılması için CLAY tarafından başarıyla kullanılır. Sütun sıcaklığı, yüksek kaynar gazları azaltarak analiz süresini azaltmak için programlanır. Moleküler Sint'lerde - tüm gözeneklerin aynı boyutlara (0.4--1.5 nm) sahip olan tüm gözeneklerin (0.4--1.5 nm), - hidrojen izotopları ile bölünebilir. Avcılar denilen sorbentler, metal hidritleri ayırmak için kullanılır (GE, AS, SN, SB). Gözenekli polimerik sorbentler veya karbon moleküler boyutları olan sütunlardaki GA yöntemi, örneğin solventlerde inorganik ve organik malzemelerde suyu belirlemenin en hızlı ve en uygun yoludur.
5.2 Gazze- sıvı kromatografisi
Analitik uygulamada, gaz-sıvı kromatografisi (GLC) yöntemi daha sık kullanılır. Bu, bu, sıvı sabit fazların aşırı çeşitliliğinden kaynaklanmaktadır, bu, bu analiz için seçici bir faz seçmeyi kolaylaştıran, geniş örneklerle çalışmanıza olanak tanır ve kolayca tekrarlanabilir elde etmenizi sağlayan geniş bir konsantrasyon alanındaki dağıtım izoterminin doğrusallığı ile sütunlar.
Taşıyıcı ile sabit bir sıvı faz arasındaki bileşenlerin dağılımı mekanizması, bunların sıvı fazda çözülmesine dayanır. Seçicilik, iki faktöre bağlıdır: belirlenen maddenin buhar elastikiyeti ve sıvı fazda aktivite katsayısı. Raoul yasalarına göre, bir maddenin bir buharının esnekliğini bir çözüm üzerinde çözerken p. bEN. faaliyet katsayısı ile doğrudan orantılı G molar fraksiyonu N. bEN. saf maddenin buharının çözümü ve basıncında R ° bEN. Bu sıcaklıkta:
p i \u003d n ben p ° I (2)
I-TH bileşeninin denge buhar fazındaki konsantrasyonu, kısmi basıncı ile belirlendiğinden, bunu kabul edebilirsiniz.
P i ~ c m, ve n ~ c sonra
ve seçicilik katsayısı:
Böylece, maddenin kaynama noktasını düşürün (daha büyük P 0 I), daha zayıf olan kromatografik kolonda tutulur.
Kuvelenme maddelerinin puanı aynı ise, sabit bir sıvı fazlı etkileşimdeki farklılıklar bunları ayırmak için kullanılır: Etkileşimin daha da güçlendirilmesi, aktivite katsayısı ve daha fazla tutma.
Sabit sıvı fazlar . Sütunun seçiciliğini sağlamak için, sabit sıvı fazını doğru şekilde seçmek önemlidir. Bu aşama, karışım bileşenleri için iyi bir çözücü olmalıdır (çözünürlük küçükse, bileşenler kolondan çok hızlı bir şekilde uzanır), uçucu olmayan (bu nedenle kolonun çalışma sıcaklığında buharlaşmaz), kimyasal olarak inert, Hafif bir viskoziteye sahip (aksi halde difüzyon işlemi yavaşlar) ve taşıyıcıya uygulandığında üniforma filmi oluşturmak için sıkıca bağlanır. Bu numunenin bileşenleri için sabit fazın ayırma kapasitesi maksimum olmalıdır.
Üç tipin sıvı fazları ayırt edilir: kutupsuz olmayan (doymuş hidrokarbonlar, vb.), Orta derecede kutuplar (esterler, nitriller vb.) Ve kutuplar (poliglikoller, hidroksilamiye vb.).
Sabit bir sıvı fazın özelliklerini ve bir sınıf, yapı gibi ayrılabilir maddelerin niteliğini bilmek, bu karışımı ayırmak için hızlı bir şekilde seçici bir sıvı fazı seçmek mümkündür. Sabit fazın polaritesi ve analiz edilen numunenin maddeninin yakın olması durumunda, bileşenlerin tutma süresinin analiz için kabul edilebilir olacağı akılda tutulmalıdır. Yakın polariteye sahip çözünmüş maddeler için, elüsyon sırası genellikle kaynama sıcaklıkları ile ilişkilidir ve sıcaklık farkı yeterince büyükse, ayrımı tamamlamak mümkündür. Farklı polaritasyonun yakın kaynama maddelerinin ayrılması için, sabit faz kullanılır, dipol - dipol etkileşimi nedeniyle seçici bir şekilde bir veya daha fazla bileşeni tutarak kullanılır. Sıvı fazın kutuplarındaki bir artışla, polar bileşiklerin tutma süresi artar.
Sıvı fazı düzgün bir şekilde uygulamak için katı taşıyıcıya, eter gibi uçucu bir çözücü ile karıştırılır. Bu çözeltiye katı bir taşıyıcı eklenir. Karışım ısıtılır, çözücü buharlaşır, sıvı faz taşıyıcı üzerinde kalır. Bu şekilde uygulanan sabit bir sıvı fazlı kuru bir taşıyıcı, boşlukların oluşumunu önlemeye çalışırken bir sütunla doldurulur. Kolonun içinden tek tip ambalaj için, gaz akımı, paketleme contaları için kolonda eşzamanlı olarak geçirilir ve aynı anda dokunulmaz. Ardından, dedektöre takmadan önce, sütun kullanılması gereken birinin üzerinde 50 ° C'nin bir sıcaklığına ısıtılır. Bu durumda, sıvı fazın kayıpları olabilir, ancak sütun kararlı çalışma moduna dahil edilir.
Sabit sıvı fazların ortamı. Sabit bir sıvı fazın bir homojen ince film şeklinde dağılması için katı ortam, orta derecede spesifik bir yüzey alanı (20m2 / g), küçük ve eşit parçacık büyüklüğü ile mekanik olarak dayanıklı olmalıdır ve aynı zamanda yüzeyde adsorpsiyona yetecek kadar inert olmalıdır. katı ve gaz halindeki aşamalar En azdı. En düşük adsorpsiyon, silanize kromosorba, cam granüller ve floropak (florokarbon polimer) taşıyıcılarında gözlenir. Ek olarak, katı taşıyıcılar sıcaklıktaki bir artışa cevap vermemeli ve kolayca bir sıvı faz ile yapılması gerekir. Katı bir taşıyıcı olarak şelatların gaz kromatografisinde, silanered beyaz diyatomit taşıyıcıları en sık kullanılan - diatomitik silika veya kizelgour. Ditomitis, su, silikon dioksit içeren bir mikronomorfiktir. Bu tür taşıyıcılar arasında kromosorb W, Gasohrom Q, Chromaton n, et al. Ek olarak, cam topları ve Teflon kullanımı.
Kimyasal olarak ilgili fazlar. Genellikle bir sıvı faz ile kovalent olarak ilişkilendirilmiş modifiye taşıyıcılar kullanın. Bu durumda, sabit sıvı faz, en yüksek kolon sıcaklıklarında bile yüzeyde daha sıkı tutulur. Örneğin, diatomitik taşıyıcı, belirli bir polarite olan uzun zincirli bir sübstitüentli bir klorosilan ile muamele edilir. Kimyasal olarak bağlanmış sabit faz daha verimlidir.
6. Dağıtım kromatografisi. Kağıt Kromatografi (Kağıt üzerinde Kromatografi)
Dağıtım kromatografisi, dağıtılmış maddenin çözünürlüğündeki farklılıkların, tek bağlantısız sıvı fazlarla temas ettirilmesinde farklılıkların kullanımına dayanır. Hem fazlar - PF ve NF sıvı fazlardır. Sıvı PF'yi sıvı NF boyunca hareket ettirirken, her iki sıvı faz arasında kromatografik maddeler sürekli olarak yeniden dağıtılır.
Dağıtım kromatografisi anlamına gelir kağıt kromatugrafik (veya kağıda kromatografi) olağan seçeneklerinde. Bu yöntemde, TLC'de ince bir suybent tabakasına sahip plakalar yerine, özellikle emprenye edici olan özel bir kromatografik kağıdı kullanılır, sıvı PF, başlangıç \u200b\u200bhattından solvent bitiş çizgisine kadar kromatografi sırasında hareket eder.
Ayırmak normal faz ve sadık kağıt kromatografisi.
Düzenlemede normal faz sıvı NF'nin kağıt kromatografisi, lifler üzerinde ince bir tabaka şeklinde ve gözeneklerde sulanır, sudur. hidrofilik kağıt (ağırlıkça% 25'e kadar). Bu bağlı su, yapısındaki ve fiziksel durumundaki geleneksel sıvı sudan çok farklıdır. İçinde, paylaşılan karışımların bileşenleri çözülür.
PF'nin kağıttan hareket etmesi rolü, başka bir sıvı faz, örneğin, asitler ve su eklenmesiyle organik sıvı tarafından oynanır. Kromatografiden önce sıvı organik PF, suya doyurulur, böylece PF, hidrofilik kromatografik kağıdın lifleri üzerine suyu bozmaz.
Kromatografik kağıt endüstri tarafından üretilmektedir. Birkaç gereksinimi karşılamalıdır: Yüksek kaliteli fibröz pamuk çeşitlerinden, yoğunlukta ve kalınlıkta homojen olmak, liflerin oryantasyonu yönünde, NF'ye göre kimyasal olarak temiz ve inert.
Normal bir faz düzenlemesinde, çeşitli çözücülerden oluşan sıvı karışımları en sık PF olarak kullanılır. Böyle bir PF'nin klasik bir örneği, 1: 4: 5 hacim oranında asetik asit, N-bütanol ve su karışımıdır. Etil asetat, kloroform, benzen vb. Gibi çözücüler kullanılır.
Düzenlemede faithfulfazova kağıt kromatografisi Sıvı NF, organik bir çözücüdür, su, sulu veya alkolik çözeltiler ve alkollü alkol karışımları, bir sıvı PF olarak işlev görür. İşlem kullanarak gerçekleştirilir hidrofobik kromatografik kağıt. Naftalen, silikon yağlar, parafin, vb. İle tedavi edilerek (emprenye edilmesiyle) elde edilir. Kutupsuz ve düşük kutuplu organik çözücüler hidrofobik kağıt lifleri üzerine sıkılır ve ince bir sıvı NF tabakası oluşturur. Su böyle bir kağıt üzerinde tutulmaz onu ıslatmaz.
Kağıt kromatografisi tekniği Genel olarak, TLC yöntemiyle aynıdır. Genellikle, bir paylaşılan maddelerin karışımını içeren bir analiz edilmiş çözeltinin bir KASHPO, başlangıç \u200b\u200bçizgisindeki kromatografik kağıdın şeridine uygulanır. Çözücünün buharlaştırılmasından sonra, başlangıç \u200b\u200bçizgisinin altındaki kağıt, PF'ye batırılır, kağıdı dikey olarak yerleştirir (asılı). PF, kağıda belirlenmiş solvent cephesinin hattına ulaşana kadar bir kapak ve kromatografi ile kamerayı kapatın. Bundan sonra, işlem kesilir, kağıt havada kurutulur ve lekeleri tespit eder ve karışımın bileşenlerini tanımlamaktadır.
Kağıt kromatografisi, hem nitel hem de kantitatif analizde kullanılan TLC yöntemine benzer.
Bir veya başka bir karışım bileşeninin içeriğini ölçmek için, çeşitli yöntemler kullanılır:
1) Leke ve lekeler alanındaki madde miktarı arasındaki belirli bir bağımlılığın varlığından (orantılı, doğrusal) (genellikle kalibrasyon programı önceden belirlenmiştir);
2) Kesim lekesini madde ve bölgedeki aynı saf kağıtla tartın ve daha sonra farklılık açısından belirlenen maddenin bir kütlesini bulurlar;
3) Leke renginin yoğunluğu ile içinde içeriğin yoğunluğu arasındaki ilişkiyi dikkate alın, bu da leke rengini verir.
Bazı durumlarda, lekelerde bulunan maddeler herhangi bir çözücü ile ekstre edilir ve sonra ekstraktını analiz edilir.
Kağıt kromatografisi, hem inorganik hem de organik maddeleri içeren karışımları ayırmak için kullanılan bir farmakopoe yöntemidir. Yöntem mevcuttur, yerine getirilmesi basittir, ancak genel olarak, ısının ince bir tabakasının uygulandığı daha modern bir TLC yöntemine daha düşüktür.
7. Tortul kromatografi
Sediment kromatografisi yöntemi, esas olarak karışımları oluşturan inorganik iyonların ayrılması ve tanımlanması için kullanılır.
Yöntemin özü. Tortu kromatografisi, bir karışımın paylaşılan bileşenlerinin çökeltilmesinin kimyasal reaksiyonlarının, NF'nin bir parçası olan bir reaktif ışığı olan bir reaktif ışığı ile kullanılmasına dayanır. Ayrılma, farklı hızlarda hareketli bir faza aktarılan şekillendirilmiş bileşiklerin eşit olmayan çözünürlüğü nedeniyle gerçekleştirilir: daha az çözünür maddeler, PF'ye daha yavaş olandan daha yavaştır.
Analiz edilen sulu çözeltide eşzamanlı olarak bulunan, halojenin iyonlarının ayrılması örneği üzerindeki metodun kullanımını açıklayabilirsiniz. Aynı anda analiz edilmiş sulu çözeltide bulunur. Kl-iyon klorür, bromür iyonu-iyon iyonu Bunu yapmak için, bir kromatografik sütun kullanın (alttaki bir vinçli bir cam tüpü) bir sorbent ile doldurulur. İkincisi, taşıyıcı - alüminyum oksit A2 O 3 veya Si02 silikonundan oluşur, bir agno3'ün gümüş nitrat çözeltisi ile emprenye edilmiş (gümüş nitrat içeriği, taşıyıcı sorbent kütlesinden yaklaşık% 10'dur).
Paylaşılan anyonların bir karışımını içeren bir sulu çözelti kromatografik kolondan geçirilir. Bu anyonlar AG + Gümüş katyonlarıyla etkileşime girerek, çok çözünür gümüş halojenür rozeti oluşturur:
AG + + I -\u003e AGIV (Sarı)
AG + + BR -\u003e AGBRV (Krem)
AG + + CL -\u003e AGCLV (beyaz)
Suyun içinde gümüş halojenürlerin çözünürlüğü sırayla artar:
AGL (K ° \u003d 8.3 * 10 -17)< АgВг (К° = 5,3*10 -13) < AgCl (K°= 1,78*10 -10),
parantez içindeki parantezler, oda sıcaklığında çözünürlük ürünlerinin değerleridir. Bu nedenle, ilk önce, gümüş iyodürün sarı çökeltisi oluşturulacaktır, çünkü kromatogramdaki en az çözünen sarı (üstte) bir bölge gözlemlenecektir. Gümüş gümüş bromür (ara bölgesi) ekseni oluşturulur. Son olarak, gümüş klorürün beyaz bir çökeltisi oluşturulur - gümüş klorürün fotokimyasal ayrışması nedeniyle, ince beyaz bölge, ince metalik gümüş salınımı ile.
Sonuç olarak, birincil tortul kromatogram elde edilir.
Bölgelerin daha net bir ayrılması için, birincil kromatogramın elde edilmesinden sonra, temiz bir çökeltme bölgelerinin net bir ayrılması ile ikincil bir tortul kromatogram elde etmek için kolondan temiz bir çözücü geçilir.
Açıklanan örnekte, çökeltici NF'nin bir parçasıydı ve bir paylaşılan iyon karışımı içeren bir çözelti kolondan geçildi. Aksine, çökelticinin çözeltisini, kromatografik iyon olan NF'deki sütun içinden geçmesi mümkündür. Bununla birlikte, aynı zamanda, karma bölgeler oluşur.
Kromatografik sütundaki CL-, BR- ve iyonların ayrılma şeması tortul kromatografi yöntemiyle.
7.1 Deneme tekniği üzerinde tortul kromatografi yöntemlerinin sınıflandırılması
Genellikle ayırt edilir sütun kromatografik sütunlarda yapılan tortul kromatografi ve uçak Kağıt üzerinde veya ince bir sorbent katmanında uygulanan tortu kromatografisi.
Sedimana kromatografisinde sorbentler olarak, inert medyanın bir inspiratör ile karışımları kullanılır; çökelticileri iyon şeklinde (iyon değişim reçineleri) veya moleküller şeklinde (aktif karbon); Bir çökeltici çözelti ile emprenye edilmiş kağıt.
Taşıyıcılar en sık silika jeli, nişasta, alüminyum oksitler, kalsiyum, baryum sülfat, iyon değişim reçineleri, vb. Taşıyıcı, yaklaşık 0.02-0.10 mm boyutlarında ince dağıtır durumlarda kullanılır.
Çökeltekiler olarak, kromatografik iyonlara sahip düşük çözünen çökeltiler oluşturan bu tür reaktifler, örneğin, sodyum iyodür NAI, sülfit sodyum na 2 s, gümüş sülfat ag 2 S04, potasyum ferrosiyanür K4, oksikinolin, piridin vb.
Genellikle, saf bir çözücünün kolonundan geçtikten sonra sütun tortu kromatografisi yöntemini kullanırken, her biri sadece bir bileşen içeren (yağışın çözünürlüğü durumunda, en az üç kez farklılık göstermesi durumunda) açıkça ayrılmış bölgeler elde edilir. Yöntem, sonuçların iyi bir şekilde tekrarlanabilirliği ile karakterizedir.
Renksiz yağış alanlarının oluşumu durumunda, kromatogram, çökeltilerle boyanmış reaksiyon ürünleri ile veya hemen PF'de veya NF'de bir geliştiriciyi tanıtan bir sütun geliştirici geliştiriciden gösterilir veya geçer.
7.2 Kağıt üzerinde tortu kromatografisi
Bu yöntemin özünü, bakır katyonlarının bir karışımını içeren sulu çözeltinin analizi örneği üzerine dikkate alın. Demir Fe 3+ ve Alüminyum Al 3+.
Bir çökeltici çözelti ile emprenye edilmiş kağıt sayfasının ortasında - potasyum ferrosiyanür K4, kılcal, analiz edilmiş bir sulu çözelti ile uygulanır. CU 2+ ve demir iyonları Fe2 + zayıf çözünen çökeltme oluşumuyla ferrosiyanür iyonları ile etkileşime girer:
2CU 2 + + 4-\u003e Cu 2 (kahverengi)
4FE 3+ + 3 4-\u003e Fe4 (mavi)
Bakır (ii) ferrosiyanit, demir (iii) ferrokiyanürden daha az çözünür olduğundan, bakır (II) ferrosiyanidin çökeltisi, merkezi bir kahverengi bölge oluşturarak ayırt edilir. Daha sonra, mavi bölgeye veren ferrosiyanür demir (III) mavi çökeltisi oluşur. Alüminyum iyonları, boyalı bir alüminyum ferrosiyanür oluşturmadıkları için renksiz bir bölge vererek çevreye taşınır.
Bölüm şeması CU2 +, Fe3 + ve Al3 + tortul kromatografi yöntemiyle.
Bu şekilde, birincil kromatogram, yağış alanlarının kısmen örtüşüldüğü yerlerde elde edilir.
Sonra ikincil kromatogram elde edilir. Bunun için uygun bir çözücü (dikkate alınan durumda bir amonyak sulu çözeltisidir), kılcal tarafından primer kromatogramın ortasına uygulanır. Solvent, kağıdın merkezinden çevre merkezinden periferliğe taşır, kendisi ve çökeltilerle, farklı hızlarda hareket eden çökeltilerle taşınır: Ferrosiyanür demirin daha fazla çözünür tortusu bölgesi, bakır ferrosiyanürün daha az çözünür bir tortunun daha hızlı bölgesini hareket ettirir. Bu aşamada, yer değiştirme bölgelerinin hızlarındaki fark nedeniyle, daha net ayrılması meydana gelir.
Alüminyum iyonlarını açmak, renksiz bir periferik bölge, bir ikincil kromatogram sergi - sprey (spreyden) bir alizhar çözeltisi - alüminyum iyonları pembe reaksiyon ürünleri ile organik bir reaktif oluşumu. Harici bir gül yüzüğü alın.
8. İyon değişim kromatografisi
İyon değişim kromatografisinde, karışım bileşenlerinin ayrılması, iyon sorbent grupları ile iyonlaştırıcı maddelerin geri dönüşümlü etkileşimi ile elde edilir. Sorbanın e-tavsiyesinin korunması, yüzeye yakın bir konumda bulunan iyon değişimine sahip olan sezonların varlığı ile sağlanır. Tanıtılan numunenin iyonu, sorbent'in sabit yüküyle etkileşime giren, karşı değiş tokuş eder. Sabit bir ücret karşılığında farklı afiniteye sahip maddeler, anyoniklere veya katyona ayrılır. Anyonatlar, yüzeydeki olumlu bir şekilde yüklenmiş gruplar ve anyonların mobil fazından sorbit. Katyonlar sırasıyla, negatif bir şarjlı gruplar içerir, katyonlarla etkileşime girer.
Bir mobil faz olarak, sıvı amonyak tipinin asit tuzlarının, baz ve çözücülerin sulu çözeltileri kullanılır, yani. Dielektrik sabitinin yüksek anlamına sahip olan çözücüler ve bileşikleri iyonize etme eğilimi. Tipik olarak, pH değerinin ayarlanmasına izin veren tampon çözümleriyle çalışır.
Analiz edilen maddenin iyonlarının kromatografik ayrılması, elüentte bulunan iyonlarla rekabet ettiğinde, zincirsel olarak yüklü sorbent gruplarıyla etkileşime girmeyi istemek istiyor. İyon değişim kromatografisi, herhangi bir şekilde iyonize olabilecek bileşikleri ayırmak için kullanılabileceğini takip eder. Nötr şekerler moleküllerini, kompleksler formunda, borat iyonu ile analiz etmek mümkündür.
İyon değişim kromatografisi, Türevlere çeviri olmadan GLC tarafından analiz edilemeyen SUYU SUYUSU MADDELERİNİN BAĞLANTISI. Bu tür bileşikler amino asitler, peptidler, şeker içerir.
İyon-değişim kromatografisi, ilaç, biyoloji, biyokimyada, ilaçların içeriğini ve kan ve idrardaki metabolitlerini analiz ederken, gıda hammaddelerinin yanı sıra inorganik bileşiklerin ayrılması için de dahil olmak üzere, ilaç, biyoloji, biyokimyada yaygın olarak kullanılır. Radyoizotoplar, Lantanoidler, Aktinoidler vb.. Genellikle saatlerce veya günler harcanan biyopolimerlerin (proteinler, nükleik asitler vb.) Analizi, iyon değişim kromatografisi yardımı ile 20-40 dakika daha iyi bir ayrımla gerçekleştirilir. Biyolojide iyon değişim kromatografisi kullanımı, örneklerin doğrudan biyoçürlerde gözlemlemesini, yeniden gruplandırma veya izomerizasyon olasılığını azaltmayı mümkün kılmıştır, bu da nihai sonucun yanlış yorumlanmasına neden olabilir. Biyolojik sıvılarla meydana gelen değişiklikleri kontrol etmek için bu yöntemi kullanmak ilginçtir. Silika jel bazında gözenekli zayıf anyonik borsaların kullanılması, peptidleri bölmeyi mümkün kılmıştır. İyon değişim mekanizması aşağıdaki denklemler olarak gösterilebilir:
anyon Değişimi X - + R + Y - - Y - + R + X -
katyonik Değişim X + + R - Y + - Y + + R - X +
İlk durumda, X-Sample iyonu, taşınabilir faz y - iyon merkezleri R + iyon değiştiricisi için ve ikincisinde İyon Merkezleri için mobil faz Y + 'nın iyonları ile rekabet etmek için rekabet ediyor. Örnek X +'nin katyonları.
Doğal olarak, iyon değiştiriciyle zayıf bir şekilde etkileşime giren örnek iyonları, bu rekabetin sütun üzerinde zayıf bir şekilde tutulacak ve ilk önce ondan uzaklaştırılacak ve aksine, daha güçlü bir şekilde tutulan iyonlar en son sütundan elüt edecektir. Genellikle, iyonik olmayan doğanın ikincil etkileşimleri, matrisin iyonik olmayan kısmı olan veya örneğin hareketli fazda numunenin sınırlı çözünürlüğü nedeniyle, numunenin adsorpsiyonu veya hidrojen bağları nedeniyle ortaya çıkıyor.
Belirli maddelerin ayrılması, öncelikle en uygun sorbent ve mobil fazın seçimine bağlıdır. İyon değişim kromatografisinde sabit bir faz olarak, aşılanan iyonik gruplara sahip iyon değişim reçineleri ve silika jelleri kullanılır.
10 μm HPLC tahıl için polistiren iyon değişimi reçineleri ve daha az seçici ve kararlılığa sahip, ancak bunların örgü yapısı, silika jel için kullanılan gözeneklerin boyutundan önemli ölçüde az olan 1.5 nm örgü düğümleri arasındaki mesafe ile karakterize edilir. Adsorpsiyon kromatografisi (10 nm), kütle transferini yavaşlatır ve bu nedenle, verimliliği önemli ölçüde azaltır. HPLC'de kullanılan iyon değişim reçineleri, esas olarak stiren ve divinil benzenin kopolimerleridir. Tipik olarak ikincisinin% 8-12'sini ekleyin. Di-vinilbenzen içeriği ne kadar büyükse, polimerin sertliği ve gücü, kapasitenin üstünde ve bir kural, seçicilik ve daha küçük şişlik olarak arttırır.
Benzer belgeler
Kromatografi işleminin genel özellikleri. İnce tabakalı kromatografi fiziko-kimyasal temelleri, analiz yöntemlerinin sınıflandırılması. Faz eyaletleri ile kromatografi varyantları. TLC yöntemi, ekipman ile gıda ürünlerinin kalitesini kontrol edin.
dersin işi, 12/27/2009
Kromatografi sırasında oluşan fenomenler. Açıklamaya iki yaklaşım, teorik plakalar ve kinetik teorinin teorisidir. Gaz, sıvı, kağıt kromatografisi. İyon değişim yöntemi. İyon değişim kromatografisi uygulama vakaları. Gelkromatografi.
Özet, Eklenen 01/24/2009
Polimer sorbentlerinin kavramı ve yapısı, yaratma ve geliştirmelerinin tarihi, dağıtım kromatografisi sürecinde değer. Polimerik sorbentlerin türleri, özel kromatografide kullanımlarının olanakları. Sert jellerin kullanımının özellikleri.
ÖZET, 07.01.2010 eklendi
Kromatografinin ortaya çıkışı ve gelişimi. Kromatografik yöntemlerin sınıflandırılması. Katı sabit fazda kromatografi: gaz, sıvı (sıvı adsorpsiyon). Sıvı sabit fazdaki kromatografi: Gaz-sıvı ve jel kromatografisi.
ÖZET, 01.05.2009 eklendi
Kromatografi yönteminin özü, gelişimi ve türlerinin tarihi. Kromatografi kapsamı, kromatografik ayrılma için cihazlar veya tesisler ve maddelerin karışımlarının analizi. Gaz kromatografisinin şeması, ana sistemleri ve operasyon prensibi.
Özet, Eklenen 09/25/2010
İletilen kromatografi yönteminin temelleri. Gaz kromatografisi, karmaşık karışımların yüksek kaliteli ve kantitatif analizinin evrensel bir yöntemidir ve bireysel bileşenlerin saf formunda üretilmesi için bir yöntemdir. Yüzleşen gaz kromatografisi kullanımı.
dersin işi, eklendi 01/09/2010
İyon çift kromatografısinin özü ve içeriği, sıvı kromatografisinde kullanımı ve ilaçları ve metabolitlerini biyolojik sıvılardan organik faza çıkarmak için ekstraksiyonda kullanılır. İyon çift kromatografi, ayırt edici özelliklerin varyantları.
ÖZET, 07.01.2010 eklendi
Gaz kromatografisi, şu anda hızla gelişen en umut verici fizikokimyasal araştırma yöntemlerinden biridir. Kromatografik yöntemlerin sınıflandırılması. Sürecin çeşitli karakteristik belirtileri. Kromatografi yöntemlerinin özü.
Özet, eklendi 01/25/2010
Karmaşık safsızlıkları analiz etmek ve ayırmak için bir yöntem olarak yüksek verimli sıvı kromatografi (HPLC) özü. Sorbentler, Koordinasyon ve Doymuş Şelatlar; Ligand yapısının yapısının, şelatların virüslü kromatografi koşulları altında davranışlarının etkisinin kalıpları.
Özet, Eklendi 11/10/2011
Dışlama kromatografisi akışının konsepti ve ana aşamaları, ilkeli özelliği ve uygulama kapsamı, çeşitleri ve onların kendine özgü özellikleri. Özel kromatografi sürecinde kullanılan ekipmanın özellikleri.
Geçtiğimiz yüzyılın birçok keşifleri, Rus bilim adamı michail rengine ve kromatografik analiz yöntemine yöneliktir. Çok sayıda olağanüstü araştırmacı onların başarılarıyla ve birçok ve Nobel Ödülü'nü yapmalı!
"... Michael'in çalışması olmadan, tüm" pigmentler "ile ilgisi yok, yapacak bir şey olmazdı ..." - İşte ünlü İngiliz bilimcisinin görüşü.
Mikhail Semenovich rengi (1872-1919) - İtalyan ve Rus entelektüelinin oğlu. Torino'dan uzak olmayan Asti şehrinde İtalya'da doğdu. 1891'de Mikhail, Cenevre Gymnasium'dan mezun oldu ve Cenevre Üniversitesi Fizik ve Matematik Fakültesine girdi. Tezi "Hücrenin fizyolojisinin incelenmesini temsil ediyor. Protoplazmın hareketi, plazma membranlar ve kloroplastların hareketi bilgisi için materyaller" rengini 1896'da Doğal Bilimler Doktoru'nun doktoru aldı. Aynı yılın Aralık ayında St. Petersburg'a geliyor.
Mikhail, Cenevre Üniversitesi bursunun Rusya'da tanınmadığını bilmiyordu. Bu nedenle, ünlü Botanik Andrei Sergeyevich Famincin'de çalışması gerekiyordu, ayrıca klorofil okudu, kuş haklarında söylenebilir. Petersburg'da, renk, diğer seçkin botanik ve bitki fizyolojileri ile tanıştı: I.P. Borodin, M.S. Voronin, A.N. Beketovo. Düşünür ve yetenekli deneycilerin fikirleriyle zengin bir özgün zengin toplumdur. Renk, kloroplast araştırmalarını sürdürdü, aynı zamanda yeni ustanın sınavlarına ve tezi savunmak için hazırlanıyor. Sınavı 1899'da geçti ve 23 Eylül 1901'de Kazan Üniversitesi'ndeki Yüksek Lisans Tezini savundu.
Kasım 1901'den bu yana, renk Varşova Üniversitesi'nde Anatomi Bölümü ve Bitki Fizyolojisi'nin asistanı olarak çalışmaktadır. Xi Naturalistler ve Doktorlar Kongresi'nde, Mikhail Semenovich, ilk defa adsorpsiyon kromatografisi yönteminde bildirilen "Fizyolojik Araştırma Klorofilinin Yöntem ve Amaçları" raporunu yaptı.
Mikhail Semenovich, yeşil yaprak pigmentlerini ayırmanın problemini çözdü ve özellikleri ile çok yakınlar. Ayrıca, yapraklarda karotenoidler, diğer, çok parlak, pigmentler vardır. Karotenoidler ve sonbaharda sarı, turuncu, koyu kırmızı yapraklar sayesinde görünür. Bununla birlikte, klorofiller tahrip olmazken, onları karotenoidlerden ayırmak neredeyse imkansızdı.
Yu.g. Chirkov, "Görünüşe göre, rengin açılması, mevcut kaba ve katil yöntemlere ayırmalarının yöntemlerine bir tepkidi. İşte tekniklerden biri.
İlk olarak, klorofil alkol ekstresi mayınlı olarak, o zaman üç saati, güçlü alkali (kostik potasyum) ilavesiyle guil kaynardı. Sonuç olarak, klorofil bileşik parçalara ayrılır - yeşil ve sarı pigmentler.
Ancak bu iksir üretimi sürecinde (neredeyse simyasal manipülasyonlar), doğal klorofil çökebilir. Ve sonra araştırmacı pigment parçaları ile ve hatta kimyasal dönüşümlerinin ürünleri ile ilgileneceklerdi. "
Büyük keşif ne olduğu hakkında, S.E yazıyor. SHNOL: "Cam tüpü aldı, bir tebeşir tozu ile doldurdu ve üst tabakadaki yaprak ekstraktının küçük bir alkol özü döküldü ve tebeşir sütununun üst tabakası aynı renkteydi. Ve MS dökmeye başladı Tebeşir saf alkollü tüpte. Damla başına düşüş. Çözücünün bir başka kısmı, tüpü aşağı hareket ettiren tahıl tanelerinden pigmentlerle elüt edildi. Taze gram mezarları adsorbe edilen pigmentler ve sırayla yeni porsiyonlara verdi. Çözücü. Hareketli bir çözücü ile kaçırılan birkaç farklı adsorpsiyon kuvveti (elüsyon kolaylığı), farklı pigmentler, tebeşir sütunu boyunca farklı hızlarda hareket ettirildi ve tebeşir sütununda saf maddelerin homojen boyalı çizgilerini oluşturdu. Güzeldi. Parlak yeşil şerit, sarı sarı şeridi - bunlar iki tip klorofillerdir - ve parlak sarı-turuncu barotinoidlerdir. M.S. Bu resim kromatogramı olarak adlandırılır. "
"Renk gösterdi, - Chirkov'u yazıyor - Koyun çözünmüş sebze pigmentlerinin renksiz gözenekli bir sorbent tabakası boyunca, bireysel pigmentlerin boyalı bölgeler biçiminde bulunduğunda - her pigmentin kendi rengi veya en azından bir gölgede bulunur. Sorbent tozu ( Tebeşir, şeker tozu ...) adsorb olabilir (yüzeysel olarak emerler: Latin adsorbere "yutma" anlamına gelir) Eşitsiz güçlü farklı pigmentler: Bazıları bir çözelti akımı ile daha da "kayabilir", diğerleri daha da yakın tutulur. -Bir hukuk kromatogram adı verilen renk ukalalı renk ve yöntem - kromatografi. "
Böylece görünüşte inatçı görevi çözüldü. Yöntem ustaca basitti. Daha önce uygulanan çok sayıda reaktif kompleks prosedürü talep eden hacimli, hacimli benzer değil.
Belki bu basitlik, çağdaşların çoğunun çoğunun veya bu şaşırtıcı keşfi algılamadığı veya hala üzücü, yazarına karşı isyan ettiğine neden olmuştur.
Ama hepsi yerine oturdu. Renk klorofil çalışmaları için kromatografi icat etti. İlk önce klorofil alfa ve klorofil beta adlı bir madde tahsis etti. Sadece pigmentler değil, aynı zamanda renksiz, boyasız karışımların - proteinlerin, karbonhidratların da araştırılması için uygun olduğu ortaya çıktı. Yirminci yüzyıl kromatografısinin altmışlı yılları için, birkaç bin çalışma ayrıldı. Kromatografi evrensel bir yöntem haline geldi.
"Maddelerin kromatografik ayrılması ilkesi, M. rengiyle açık, çeşitli kromatografik analiz yöntemlerinin ayarlanmasının altında. Kullanımı olmadan, 20. yüzyılın bilim ve tekniğindeki başarıların çoğu imkansız olur .. .
Bütün bunların temeli bir ortak fikirdir. O basit. Bu esasen geometrik ilerleme fikridir. Tüm özelliklerinde iki maddeye çok yakın olmasına izin verin. Ne biriktirme ne de ekstraksiyon ne de adsorpsiyon, gözle görülür bir ölçüde ayrılır. Bir madde yüzeye, örneğin, kalsiyum karbonat (yani yüzde 1'den az) izin verin.
Başka bir deyişle, adsorban üzerindeki içeriği, diğerinin içeriğinden 0,99 olacaktır. Adsorbanı herhangi bir çözücü tarafından tedavi ediyoruz, böylece her iki maddenin de desorpsiyon (bağlantı kesilmesi) ve elüsyon (yıkama) ve her ikisinin de adsorbandan çözücüye taşınması ve bu sonuçtaki çözümü adsorbanın taze bir kısmına taşıyacağız. Daha sonra, adsorbanın yüzeyindeki ilk maddenin oranı, saniyenin içeriğinden yine 0,99 olacaktır, yani, yani, yani, ilk miktardan 0.99 x 0.99 \u003d 0.98'e eşittir, yani adsorbe edilir. Bir kez daha, elüsyon ve tekrar adsorpsiyon yapacağız - şimdi ilk maddenin payı, saniyenin içeriğinden 0.98 x 0.99 \u003d 0.97 olacaktır. İlk maddenin içeriği için, adsorbanın bir sonraki kısmına, saniyenin içeriğinin sadece yüzde 1'i, yaklaşık 200 kez emilim-elüsyon döngüsünü tekrarlamak için gerekli olacaktır ...
Maddelerin ayrılması için birden fazla konuşma fikri, kuru olmayan çözücüler sistemindeki maddelerin karışımının birden fazla yeniden dağıtılması halinde değiştirilebilir. Bu, dağıtım kromatografisinin temelidir. Aynı fikir, madde karışımı, elektrik alanındaki çeşitli adsorbanların farklı hızlarında hareket ettiğinde mevcut elektroforez yöntemlerinin geçerlidir.
1. GİRİŞ.
2. Kromatografinin ortaya çıkışı ve gelişimi.
3. Kromatografik yöntemlerin sınıflandırılması.
4. Katı sabit fazda kromatografi:
a) Gaz (gaz adsorpsiyonu) kromatografi;
b) Sıvı (sıvı adsorpsiyon) kromatografi.
5. Sıvı sabit fazda kromatografi:
a) Gaz-sıvı kromatografisi;
b) jel kromatografisi.
6. Sonuç.
Spektrumun ışınları olarak, pigment karışımının çeşitli bileşenleri doğal olarak karbondioksit kolonunda doğal olarak dağıtılır, nitel ve nicel tayini sağlar. Bu şekilde elde edilen ilaç, kromatogramı ve önerilen yöntemi - kromatografik olarak çağırırım.
M. S. RENK, 1906
Giriş
Maddelerin karışımını bölme ve analiz etme ihtiyacı ile, sadece kimyager değil, aynı zamanda diğer birçok uzmana da yüzleşmek gerekir.
Kimyasal ve fizikokimyasal ayırma yöntemlerinin güçlü bir cephesinde, analiz, bireysel kimyasal bileşiklerin yapısı ve özelliklerinin çalışması ve bunların karmaşık karışımlarının çalışması, önde gelen yerlerden biri kromatografiyi kaplar.
Kromatografi, iki faz arasındaki karışımların paylaşılan bileşenlerinin dağılımına dayanarak, gazların, buharların, sıvıların veya çözünürlüklerin karışımlarının, buharların, sıvıların veya çözünürlüklerin karışımlarının ve bireysel maddelerin fizikokimyasal özelliklerinin belirlenmesidir. Hareketli ve sabittir. Sabit fazı oluşturan maddeler sorbent olarak adlandırılır. Sabit faz katı ve sıvı olabilir. Mobil faz, sorbent katmanından süzülen bir sıvı veya gaz akışıdır. Mobil faz, çözücünün fonksiyonlarını ve analiz edilen madde karışımının taşıyıcısını, gaz veya sıvı duruma çevrilmiştir.
İki tür emme vardır: Adsorpsiyon - Katıların emilimi ve emilimini emme - Sıvı çözücülerde gazların ve sıvıların çözülmesi.
2. Ortaya çıktıkromatografi ve Geliştirme ve Geliştirme
Bilimsel bir yöntem olarak kromatografinin oluşması, 1903'teki 1903'te, güneş enerjisinin bitki pigmentlerinde güneş enerjisinin dönüşümü için mekanizmanın çalışması sırasında kromatografiyi açan olağanüstü Rus bilim adamı Mikhail Semenovich renklerinin (1872 - 1919) adıyla ilişkilidir. Bu yıl kromatografik yöntemin oluşturulma tarihi olarak kabul edilmelidir.
HANIM. Renk, analiz edilen maddelerin çözeltisini ve hareketli fazın bir cam tüpte bulunan AdSorbent sütunundan geçirdi. Bu bağlamda, yöntemi sütun kromatografisi adını aldı. 1938'de N.A. Izmailov ve M.S. Schreiber, renk yöntemini değiştirmeyi ve plakadaki maddelerin karışımının bir adsorbanın ince bir tabakası ile kaplı maddelerin ayrılmasını yapmayı teklif etti. Böylece, ince tabaka kromatografisi göründü, bu da maddenin mikrocolizmini analiz etmeyi mümkün kılar.
1947'de. TB Gapon, e.n. Gapon ve F.M. İlk defa Shemyakin, çözelti halinde bir iyon karışımının bir kromatografik ayrılması, çözeltide bulunan sorbent iyonları ve iyonlar arasında bir değişim reaksiyonunun varlığını açıklar. Böylece, bir başka kromatografi yönü açıldı - iyon değişim kromatografisi. Şu anda, iyon değişim kromatografisi, kromatografik yöntemlerin en önemli yönlerinden biridir.
E.n. ve G. B. Gapon, 1948'de M.S. Sert çözünür çökeltmenin çözünürlüğünde fark dayalı maddelerin bir karışımının kromatografik ayrılması olasılığı fikri. Bir tortu kromatografisi vardı.
1957'de M. Golay, kılcal boru - kılcal kromatografi iç duvarları üzerinde bir sorbent uygulamayı önerdi. Bu varyantı, çok bileşenli karışımların mikrocolizmini analiz etmenizi sağlar.
60'larda, kesinlikle tanımlanmış gözenek boyutları olan hem iyonik hem de yüklü jelleri sentezlemek için bir fırsat vardı. Bu, bir kromatografi seçeneği geliştirmeyi mümkün kılmıştır, bu, maddenin karışımını, jel - jel kromatografısinin nüfuz etme kabiliyetlerinde farklılığa dayanarak ayrılmaktan oluşur. Bu yöntem, maddelerin karışımlarını farklı moleküler ağırlıkla ayırmanıza izin verir.
Halen kromatografi, önemli bir gelişme kazanmıştır. Günümüzde, çeşitli kromatografi yöntemleri, özellikle diğer fiziksel ve fizikokimyasal yöntemlerle birlikte, araştırmacıların ve mühendislerin en farklı, genellikle çok karmaşık işleri bilimsel araştırma ve tekniğin çözmelerine yardımcı olur.
3. Clasfikkromatografik Yöntemler
Kromatografi yönteminin modifikasyonlarının ve varyantlarının çeşitliliği sistematizasyonlarını veya sınıflandırmalarını gerektirir.
Sınıflandırmanın temeli, yani çeşitli işaretlere konulabilir:
1. Aşamaların toplam durumu;
2. Ayırma mekanizması;
3. İşlemi iletme yöntemi;
4. Sürecin amacı.
Aşamaların toplam haliyle sınıflandırma:
gaz (hareketli faz - gaz), gaz-sıvı (mobil faz - gaz, sabit faz - sıvı), sıvı (hareketli faz - sıvı) kromatografi.
Ayrılma mekanizması ile sınıflandırma.
Adsorpsiyon kromatografisi, karışık karışımın bireysel bileşenlerinin seçici adsorpsiyonuna (absorpsiyon), uygun adsorbanlar ile dayanmaktadır. Adsorpsiyon kromatografisi sıvıya (sıvı adsorpsiyon kromatografisi) ve gaza (gaz adsorpsiyon kromatografisi) ayrılmıştır.
İyon değişim kromatografisi, analitin çözeltisi, iyon değişim maddesi (iyonit) ile doldurulmuş sütun boyunca analiz edildiğinde, adsorbanın hareketli iyonları ile elektrolit iyonları arasında meydana gelen iyon değişim işlemlerinin kullanımına dayanır. İyonitler çözünmeyen inorganik ve organik yüksek moleküler ağırlıklı bileşiklerdir. Alüminyum oksit iyonitler, permütit, sulfouggol ve çeşitli sentetik organik iyon değişim maddeleri - iyon-değişim reçineleri olarak kullanılır.
Sedimanter kromatografi, analiz edilen karışımın bileşenlerinin özel reaktifleriyle oluşturulan farklı yağışların farklı çözünürlüğüne dayanır. Örneğin, NG (II) ve PB tuzlarının karışım çözeltisi, Ki çözeltisi ile önceden emdirilmiş bir taşıyıcı olan bir kolondan geçirildiğinde, 2 renkli katman oluşur: üst, turuncu kırmızı (HGI 2) boyanmış, ve alt, sarı boyalı (PBI 2).
Süreci yürütme sürecine göre sınıflandırma.
Sütun kromatografisi, bir sütunun sabit bir çözücü için bir taşıyıcı olarak kullanıldığı bir kromatografi türüdür.
Kağıt kromatografisi, bir hoparlör yerine sabit bir çözücü için bir taşıyıcı olarak bir taşıyıcı olarak, mineral safsızlıklar içeren filtre kağıdının veya tabakaların kullanıldığı bir kromatografi türüdür. Bu durumda, örneğin bir test çözeltisi, örneğin, FE Tuzları (III) ve CO (II) çözeltilerinin bir karışımının, kağıt şeritlerinin kenarına uygulanır. Kağıt, kapalı bir odada (Şek. 1), kenarı, bir test çözeltisinin bir damlası ile hareketli bir çözücüye sahip bir kabın içine düşürülür, örneğin N-bütil alkol ile. Hareketli çözücü, kağıda hareket ettirin, kazanır. Bu durumda, analiz edilen karışımda bulunan her madde, içine özgü oranla, çözücü ile aynı yönde hareket eder. İyonların ayrılmasının tamamlanmasından sonra, kağıt kurutulur ve daha sonra bir reaktif ile püskürtülür, bu durumda, ayrılabilir maddelerle boyanmış bileşikler (mavi - demir iyonları, yeşili - kobalt iyonları olan) ile boyanmış bileşikler oluşturur. Boyalı lekeler biçiminde tüm bunlarla oluşan bölgeler, bireysel bileşenlerin varlığını belirlemenizi sağlar.
Kağıt kromatografisi organik reaktiflerin kullanımı ile birlikte, karmaşık katyon ve anyonların karmaşık karışımlarının nitel bir analizini gerçekleştirmeyi mümkün kılar. Bir kromatogramda, bir reaktifin yardımı ile bir dizi madde tespit edilebilir, çünkü sadece karşılık gelen boyama değil, aynı zamanda kromatogramdaki belirli bir yer konumuyla da karakterize edilir.
İnce tabaka kromatografisi, kağıt kromatografisine benzer ayırma mekanizmasında bir tür kromatografidir. Aralarındaki fark, kağıt tabakalar yerine, ayırma, pudralı alüminyum oksit, selüloz, zeolitler, silika jel, kizelur vb. Yapılan ince bir sorbent tabakası ile kaplanmış plakalar üzerinde yapılır. ve sabit bir çözücü tutuyor. İnce tabakalı kromatografinin temel avantajı, ekipmanın kolaylığı, sadeliği ve deneyin yüksek hız, maddelerin karışımının ayrılmasının yeterli netliği ve maddenin ultramikrokolizmini analiz etme kabiliyetine sahiptir.
Kromatografik işlemin amacı için sınıflandırma.
Kromatografi, maddelerin karışımlarının nitel ve kantitatif analizi yöntemi olarak en büyük değere sahiptir (analitik kromatografi).
Hazırlayıcı kromatografi - maddelerin karışımının hazırlayıcı amaçlarla üretildiği kromatografi türü, yani. Saf, safsızlıklardan arınmış, daha az veya önemli miktarda madde için. Hazırlayıcı kromatografi görevi de konsantre olabilir ve ardından mikrostrum formunda bulunan maddelerin ana maddeye bağlı olarak serbest bırakılabilir.
Analitik olmayan kromatografi, bilimsel araştırma yöntemi olarak kullanılan bir tür kromatografidir. Çözümler, kimyasal işlemlerin kinetiği, katalizörlerin ve adsorbaların özellikleri gibi sistemlerin özelliklerini incelemek için kullanılır.
Bu nedenle, kromatografi, maddelerin karışımlarını analiz etmek, saf formda maddeler üretme ve sistemlerin özelliklerini incelemek için bir yöntemdir.
4. Kromatografsağlam bir sabit fazda düzelt
fakat)Gaz (G.azo Adsorboverik) Kromatografi
Gaz kromatografisi - mobil fazın gaz olduğu bir kromatografik yöntem. Gaz kromatografisi, maddelerin ve karışımlarının ayrılması, analiz edilmesi ve araştırılması için en büyük uygulamayı aldı, buhar durumuna ayrışma olmadan hareket ediyor.
Gaz kromatografisi değişkenlerinden biri gaz adsorpsiyon kromatografisidir - bu, sabit fazın katı bir adsorban olduğu bir yöntemdir.
Mobil faz (gaz taşıyıcı) olarak gaz kromatografisinde inert gaz kullanır: helyum, azot, argon, hidrojen ve karbondioksitten önemli ölçüde az. Bazen taşıyıcı gaz bir çift uçucu sıvı sunar.
Gaz kromatografik işlemi genellikle gaz kromatografları adı verilen özel cihazlarda gerçekleştirilir (Şekil 3). Her birinde, bir gaz taşıyıcı akış sistemi, karışımın çalışma altında bir hazırlık ve yerleştirme sistemi, sıcaklık kontrol sistemine sahip bir kromatografik sütun, sistemi (dedektör) ve ayrılma sonuçlarını kaydetmek için bir sistem analiz etmek için bir gaz taşıyıcı akış sistemi vardır. Analiz (Kaydedici).
Gaz adsorpsiyon kromatografisinde sıcaklık bir sıcaklığa sahiptir. Rolü öncelikle gaz sistemindeki emilim dengesini değiştirmede - bir katı. Kolonun sıcaklığının doğru seçiminden, karışımın bileşenlerinin ayrılmasının derecesine ve kolonun verimliliği ve toplam analiz oranına bağlıdır. Kromatografik analizin optimal olduğu kolonun bir miktar sıcaklık aralığı vardır. Tipik olarak, bu sıcaklık aralığı, kimyasal bileşiğin kaynama noktasına yakın bir bölgede bulunur. Karışımın kaynama noktaları, kendileri arasında büyük ölçüde farklılık gösterdiğinde, kolon sıcaklığının sıcaklığını uygulayın.
Kromatografik sütun ayrımı, tüm gaz kromatografik analiz sürecinin en önemli ancak ön işlemidir. İkili karışımların üzerinde (gaz taşıyıcı gaz - bileşen) tespit cihazına düşer. Burada, zaman içinde bileşenlerin konsantrasyonlarındaki değişikliklerin bir elektrik sinyaline dönüştürülmesi, kromatogram olarak adlandırılan bir eğri şeklinde özel bir sistem kullanılarak kaydedilen bir elektriksel sinyal. Tüm deneyimin sonuçları büyük ölçüde, tasarımı, dedektör türünün doğru seçimine bağlıdır. Dedektörlerin birkaç sınıflandırması vardır. Farklı diferansiyel ve integral dedektörler. Diferansiyel dedektörler, zaman içinde özelliklerden birinin (konsantrasyon veya akış) anlık değerini kaydedin. İntegral dedektörler, belirli bir süre için madde miktarını özetlemektedir. Dedektörler ayrıca eylem, duyarlılık ve amaç ilkesinde kullanılır: termosonductometrik, iyonizasyon, spektroskopik, kütle spektrometrik, katülometrik ve diğerleri.
Gaz adsorpsiyon kromatografisi uygulaması
Gaz adsorpsiyon kromatografisi, kimyasal ve petrokimya sentezinin ürünlerini, yağ fraksiyonlarının bileşimini analiz etmek için kimyasal ve petrokimya endüstrisinde, reaktiflerin saflığını belirleyen ve teknolojik işlemlerin farklı aşamalarındaki kilit ürünlerin içeriğini belirlemek için kullanılır.
İkametler de dahil olmak üzere kalıcı gazların ve hafif hidrokarbonların analizi, gaz kromatografisi 5 ila 6 dakika işgal eder. Önceden, geleneksel gaz analizörlerinde, bu analiz 5 ila 6 saat sürmüştür. Bütün bunlar, gaz kromatografisinin sadece araştırma enstitülerinde ve kontrol ve ölçme laboratuarlarında değil, aynı zamanda kapsamlı sanayi işletmelerinin kapsamlı otomasyon sistemine de dahil edilmesine yol açtı.
Günümüzde, gaz kromatografisi, petrol ve gaz alanlarını aramada kullanılır ve toprak örneklerinden seçilen yağ ve gaz alanlarının yakınlığını gösteren organik maddelerin içeriğini belirlemenizi sağlar.
Gaz kromatografisi, kan lekeleri, benzin, yağlar, sahte pahalı gıdalar vb. Numunelerinin kimliğini belirlemek için kullanıldığı suçluistalisterlerde başarıyla kullanılır. Çok sık, gaz kromatografisi, araba sürücülerinin kanındaki alkolün içeriğini belirlemek için kullanılır. Parmağından birkaç damla kan, ne zaman ve ne zaman ve ne kadar alkoldığı içtiğini bulmak için yeterince kan.
Gaz kromatografisi, peynir, kahve, havyar, brendi, vb. Gıda kokularının bileşimi hakkında değerli ve benzersiz bilgiler almanızı sağlar. Bazen gaz kromatografik analizi ile alınan bilgiler mutlu değildir. Örneğin, genellikle gıda ürünlerinde, pestisitlerden veya meyve suyundan, yasakların aksine, meyvelerden, vs.den karoten derecesini arttırmak için kullanılan trikloretilenden dolayı gereksizdir. Ancak insan sağlığını koruyan bu bilgilerdir.
Ancak, insanlar yalnızca alınan bilgileri ihmal ettiğinde genellikle durumlar vardır. Her şeyden önce sigara içmek anlamına gelir. Detaylı bir gaz kromatografik analizi uzun zamandır duman sigaralarının ve sigaranın 250 farklı hidrokarbon içerdiğini ve bunların yaklaşık 50'sinin kanserojen bir etkiye sahip olduğunu belirlemiştir. Bu nedenle sigara içenlerin 10 kat daha sık akciğer kanseri var, ancak yine de milyonlarca insan kendilerini, meslektaşlarını ve akrabalarını zehirlemeye devam ediyor.
Gaz kromatografisi, çok sayıda ilacın içeriğini belirlemek, yağ asitleri, kolesterol, steroidlerin vb. Düzeyini belirlemek için ilaçlarda yaygın olarak kullanılır. Hastanın vücudunda. Bu tür analizler, insan sağlığının, hastalığının seyri, bazı ilaçların kullanımının etkinliği hakkında son derece önemli bilgiler sağlar.
Metalurji, mikrobiyoloji, biyokimya, bitki koruma ve yeni ilaçların geliştirilmesinde, yeni polimerlerin oluşturulmasında, inşaat malzemeleri ve diğer birçok farklı insanda insan pratik faaliyetlerinde bilimsel araştırma, gaz kadar güçlü bir analitik yöntem olmadan hayal etmek imkansızdır. kromatografi.
Gaz kromatografisi, polisiklik aromatik bileşiklerin içeriğini, insan sağlığı, suda ve havada tehlikeli, benzin istasyonlarının uçaklarının havasında benzin seviyesini, havada vb. Araç egzoz gazlarının bileşimi, vb.
Bu yöntem, çevrenin saflığını izlemek için ana yöntemlerden biri olarak yaygın olarak kullanılır.
Gaz kromatografisi hayatımızda önemli bir yer kaplar, bize devasa miktarda bilgi sağlar. Ulusal ekonomide ve araştırma organizasyonlarında, daha fazla karmaşık görevi çözmede, araştırmacılardan ve mühendislerden kaynaklanan birçok karmaşık görevi çözmede vazgeçilmez asistanlar olan 20 bin'den fazla çeşitli gaz kromatografisi kullanılmaktadır.
b)Sıvı (Sıvı Adsorpsiyon)kromatografi
Sıvı kromatografisi, hareketli fazın sıvı olduğu bir grup kromatografi varyantlarıdır.
Sıvı kromatografinin bir düzenlemesi sıvı adsorpsiyon kromatografisidir - bu, sabit fazın katı bir adsorban olduğu bir yöntemdir.
Her ne kadar sıvı kromatografisi gazdan daha erken açılsa da, sadece yirminci yüzyılın ikinci yarısında sadece yoğun gelişme dönemi girmiştir. Şu anda, kromatografik süreç teorisinin geliştirilmesi ve enstrümantal tasarım tekniklerinin geliştirilmesi derecesine göre, verimliliğe ve ayırma oranına göre, gaz kromatografik ayırma yöntemine yol açması pek mümkün değildir. Aynı zamanda, bu iki ana kromatografinin her biri kendi birincil kapsamına sahiptir. Gaz kromatografisi, çoğunlukla 500 - 600 moleküler ağırlığa sahip kimyasalların analizi, ayrılması ve araştırılması için uygunsa, polimerlerin, proteinlerin son derece karmaşık makromolekülleri de dahil olmak üzere, birkaç yüz ila birkaç milyon moleküler ağırlığa sahip maddeler için sıvı kromatografi kullanılabilir. ve nükleik asitler. Aynı zamanda, çeşitli kromatografik yöntemlerin muhalefeti, doğal olarak sağduyudan yoksundur, çünkü kromatografik yöntemler birbirleri tarafından başarıyla tamamlanır ve belirli bir çalışmanın çok görevi için, farklı, yani hangi kromatografik yöntemle yaklaşmak gerekir. Daha fazla hız, bilgiler ve daha az maliyetle çözmenizi sağlar.
Gaz kromatografisinde olduğu gibi, dedektörler, modern sıvı kromatografisinde, belirlenen maddenin konsantrasyonunu, kolondan akan sıvı akışında sürekli olarak sabitleyebilen dedektörler kullanılır.
Sıvı kromatografi için evrensel dedektör yoktur. Bu nedenle, her bir durumda, en büyük birlik dedektöründe seçilmelidir. Ultraviyole, refraktometrik, mikro ilaç dedektörleri, kırılma ionizasyon dedektörleri en iyiydi.
Spektrometrik dedektörler. Bu tür dedektörler, çok hassas seçici cihazlardır, sıvı fazın akışında çok küçük maddeler konsantrasyonlarına izin verir. Tanıkları, sıcaklık dalgalanmalarına ve ortamın diğer rastgele değişikliklerine çok az bağlıdır. Spektrometrik dedektörlerin önemli özelliklerinden biri, dalga boylarının çalışma alanında sıvı-adsorpsiyon kromatografisinde kullanılan en çözücülerin şeffaflığıdır.
En sık kullanılan UV'de, IR bölgesinde daha az sıklıkla emilim. UV bölgesinde, geniş bir yelpazede çalışan aletler kullanılır - 200 nm'den spektrumun görünür kısmına veya en sık 280 ve 254 nm'de belirli dalga boylarında kullanılır. Merkür düşük basınçlı ampuller (254 nm), orta basınç (280 nm) ve karşılık gelen filtreler radyasyon kaynakları olarak kullanılır.
Mikro piyonma dedektörleri. Mikro amaçlı dedektörlerin temeli, maddenin adsorban üzerindeki adsorpsiyon sırasında, dedektör hücresi ile doldurulmuş olan ısının serbest bırakılmasına dayanır. Bununla birlikte, ısınmaz, ancak adsorbanın sıcaklığı, adsorpsiyonun bir sonucu olarak ısıtıldığı ölçülür.
Bir mikro amaçlı dedektör oldukça hassas bir araçtır. Hassasiyeti öncelikle adsorpsiyonun ısısından bağlıdır.
Mikro perseter dedektörleri, hem organik hem de inorganik maddeleri tespit etmek için uygundur, evrenseldir. Aynı zamanda, özellikle karışım bileşenlerinin eksik ayrılması ile oldukça net kromatogramlar elde etmek zordur.
5. Kromatografsıvı sabit fazda ati
a) Gaz-sıvı kromatografisi
Gaz-Sıvı Kromatografisi - Sabit fazın, katı bir taşıyıcıya uygulanan genç bir sıvı olduğu bir gaz kromatografik yöntemi.
Bu tip kromatografi, sıvıların gazlarını ve buharlarını ayırmak için kullanılır.
Gaz-sıvıdaki gaz-sıvıdaki ana fark, ilk durumda, yöntemin çözünme işleminin kullanımına ve daha sonra gazın veya buharın, katı inert taşıyıcı tarafından tutulan sıvı filmden buharlaştırılmasına dayanmasıdır; İkinci durumda, ayırma işlemi adsorpsiyona ve daha sonra, katı - adsorban yüzeyinde gaz veya buhar desorpsiyonuna dayanır.
Kromatografik işlem şimdiye kadar aşağıdaki gibi gösterilebilir. Bir gaz karışımı veya uçucu sıvıların buharları bir taşıyıcı gaz akışı ile, uçucu olmayan bir sıvının dağıtıldığı (sabit faz), sabit bir inert taşıyıcı ile doldurulmuş bir kolona bir taşıyıcı gaz akışı ile enjekte edilir. Çalışılan gazlar ve çiftler bu sıvı tarafından emilir. Daha sonra, paylaşılan karışımın bileşenleri, sütundan belirli bir sırayla seçici olarak yerinden edilmiştir.
Gaz-sıvı kromatografisinde, belirli bir organik maddeye veya spesifik bir fonksiyonel gruba sahip organik maddelere özel olarak reaksiyona giren bir dizi dedektör kullanılır. Bunların iyonlaşma dedektörleri, elektronik yakalama dedektörleri, termal, spektrofotometrik ve diğer bazı dedektörler bulunur.
Alev-iyonizasyon dedektörü (PID). PID'nin çalışması, hidrojen brülörünün alevine düşen organik maddelerin iyonizasyonun aynı anda bir iyonizasyon odası olan bir iyonizasyon odası olan bir iyonizasyon odası olduğu bir iyonizasyon olduğu gerçeğine dayanır. yüklü parçacıkların sayısı.
PID sadece organik bileşiklere duyarlıdır ve hava, kükürt ve karbon oksitler, hidrojen sülfür, amonyak, karbon, su buharı ve bir dizi diğer inorganik bileşikler gibi bu gazlara duyarlı veya çok hassas değildir. PID'nin havaya duyarsızlık, çeşitli organik maddelerden hava kirliliğini belirlemeye izin verir.
PID ile çalışırken, 3 gaz kullanılır: gaz taşıyıcı (helyum veya azot), hidrojen ve hava. Tüm 3 gaz yüksek derecede saflığa sahip olmalıdır.
Argon dedektörü. Argon dedektöründe, iyonlaşma, belirlenen maddenin moleküllerinin, radyoaktif radyasyonun etkilerinden kaynaklanan metastabilen argon atomları ile çarpışmasından kaynaklanır.
Termal dedektör. Termo-iyon dedektörünün ilkesi, alev brülöründe buharlaşan alkali metal tuzlarının, halojenler veya fosfor içeren bileşiklerle seçici olarak reaksiyona girmesidir. Dedektörün iyonlaşma odasındaki bu tür bileşiklerin yokluğunda, bir alkali metal atomu bir denge oluşturulmuştur. Alkali metal atomlu reaksiyonları nedeniyle fosforlu atomların varlığı bu dengeyi ihlal eder ve iyonik akım odasındaki görünüme neden olur.
Termal dedektör, fosfor içeren bağlantılara en yüksek hassasiyete sahip olduğundan, fosfat adını aldı. Bu detektör esas olarak fosforodinorganik böcek ilacı, böcek öldürücüleri ve bir dizi biyolojik olarak aktif bileşik analiz etmek için kullanılır.
b)Jel kromatogra.fia
Jel Kromatografisi (Jel Filtrasyon) - Analiz edilen çözeltiyi enine çapraz bağlanmış hücresel jellerle filtreleyerek farklı moleküler ağırlıklara sahip maddelerin karışımlarının ayrılması yöntemi.
Maddelerin karışımının ayrılması, bu maddelerin moleküllerinin boyutlarının farklı olması durumunda ortaya çıkar ve jel tanelerinin çapı sabittir ve sadece bu moleküllerin geçebileceği, boyutlarından daha küçük olan jel gözenekleri. Karışımın bir karışımının çözeltisini filtrelerken, jelin gözeneklerine girilen daha küçük moleküller, bu gözeneklerde bulunan çözücü içerisinde geciktirilir ve jel tabakası boyunca, gözeneklere nüfuz etme yeteneğine sahip olmayan büyük moleküllerden daha yavaş hareket eder. Böylece, jel kromatografisi, bu maddelerin parçacıklarının boyutuna ve moleküler ağırlığına bağlı olarak maddelerin karışımını ayırmanıza olanak sağlar. Bu ayırma yöntemi oldukça basit, hızlı ve en önemlisi, maddelerin karışımlarını silt koşullarında diğer kromatografik yöntemlerden daha ayırmanıza izin verir.
Jel granülleri sütunu doldurursa ve daha sonra farklı moleküler ağırlığa sahip çeşitli maddelerin bir çözeltisini dökünse, çünkü çözelti kolondaki jel katmanı boyunca hareket ettirildiğinde, bu karışım gerçekleşecektir.
İlk deneyim süresi: Analiz edilen karışımın çözeltisinin kolondaki jel katmanına uygulanması. İkinci aşama - jel, gözeneklerdeki küçük moleküllerin difüzyonunu etkilemez, en büyük moleküller jel granüllerini çevreleyen çözeltide kalır. Saf bir çözücüye sahip bir jel tabakası ile yıkandığında, büyük moleküller çözücü hareketinin hızına yakın bir hızda hareket etmeye başlarken, küçük moleküller ilk önce jelin iç yaşından önce tahıllar arasındaki hacmin içine önceden belirlenmesi gerekir. Bunun sonucu ertelenir ve daha sonra çözücü ile yıkanır. Moleküler ağırlıklarına göre bir madde karışımı meydana gelir. Moleküler ağırlıklarını azaltmak için sütundaki maddeler yıkama meydana gelir.
Jel kromatografisi kullanımı.
Jel kromatografisinin temel amacı, yüksek moleküler bileşiklerin karışımlarının ayrılması ve polimerlerin moleküler kütle dağılımının belirlenmesidir.
Aynı zamanda, orta moleküler ağırlık ve hatta düşük moleküler ağırlık bağlantılarının maddelerinin karışımını ayırmak için eşit bir jel kromatografisi kullanılır. Bu durumda, jel kromatografısinin oda sıcaklıklarında ayrılmasını mümkün kılar, bu da analiz edilen maddeleri buhar aşamasına aktarmak için ısıtma gerektiren gaz-sıvı kromatografisinden ayırmayı mümkün kılar.
Maddelerin karışımının jel kromatografi ile ayrılması mümkündür ve analiz edilen maddelerin moleküler ağırlıkları çok yakın veya hatta eşit olduğunda. Bu durumda, çözünenlerin jel ile etkileşimi kullanılır. Bu etkileşim çok önemli olabilir, bu da moleküllerin boyutlarında farklılıkları azaltır. Farklı maddeler için jel ile etkileşimin niteliği IDAS değildirse, bu farkın çıkarının karışımını ayırmak için kullanılabilir.
Bir örnek, tiroid hastalıklarının tanısı için jel kromatografisinin kullanımıdır. Tanı, analiz sırasında tanımlanan iyodin sayısına göre belirlenir.
Jel kromatografisi kullanımının yukarıdaki örnekler, çok çeşitli analitik görevleri çözmek için geniş fırsatlarını göstermektedir.
Sonuç
Etrafımızdaki bilimsel bir yöntem olarak, kromatografi sürekli gelişiyor ve geliştiriyor. Bugün, kromatografinin kullanılmayacağı bilgi alanını bulmak çok zor olan bilimsel araştırma, tıp, moleküler biyoloji, biyokimya, teknoloji ve ulusal ekonomide bu kadar sık \u200b\u200bve çok yaygın olarak uygulanır.
Olağanüstü yetenekleriyle bir çalışma yöntemi olarak kromatografi, karmaşık bir dünyanın, gezegenimizde kabul edilebilir insan yaşam alanı koşulları yaratmanın çıkarlarına bilgi ve dönüşümünde güçlü bir faktördür.
P ile veL ve t ve n ve n
1. ivazov B.V. Kromatografiye giriş. - m.: Daha yüksek. SK., 1983 - s. 8-18, 48-68, 88-233.
2. Kreszkov A.P. Analitik kimya temelleri. Teorik temel. Nitel analiz, ilk kitap, Ed.4-e, rekreasyon. M., "Kimya", 1976 - s. 119-125.
3. Sakodynsky K.i., Orekhov B.i. Bilim ve teknolojide kromatografi. - M.: Bilgi, 1982 - s. 3-20, 28-38, 58-59.