Konstrukcija zone energetskog spektra elektroničkih stanja. Konstrukcija zone energetskog spektra elektrona
Poglavlje 10. Koncept teorije zone krutina
Ideja valente kao atomske sposobnosti formiranja kemijskih veza s određenim brojem drugih atoma u primjeni na krutu tvar gubi njegovo značenje, jer je mogućnost kolektivne interakcije ovdje. Dakle, u molekuli valencije atoma i jednake su jednoj, au kristalu je svaki atom okružen s 6. atomima i obrnuto.
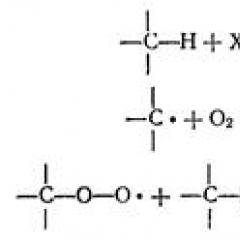
Energetski spektar izoliranog atoma određen je interakcijom elektrona s jezgrom i diskretna. Energetske stanja elektrona u krutom tijelu određene su njegovom interakcijom i sa svojom jezgrom i jezgrama drugih atoma. U suzgrenim atomima kristala nalaze se povremeno duž bilo kojeg smjera (sl. 56). Stoga se elektron kreće u periodičnom električnom polju (u blizini jezgre potencijalna energija elektrona je manja nego u intervalu između zrna). To dovodi do činjenice da umjesto diskretne razine atomske energije u kruti N.atomi se pojavljuju N.usko smještene energetske razine koje se nalazi odvojene jedna od druge, koja tvore energetsku zonu. U tom smislu, oni govore o cijelosti energetske razine u energetsku zonu. Susjedne razine energije u zoni odvojene su jedni od drugih za 10 -23 ev. Za usporedbu, ukazujemo na prosjek termalna energija elektroni na temperaturi T. \u003d 300 K je ~ 10 -2 ev. Kao rezultat toga, elektronski spektar može se razmatrati u kvazi-sušnoj zoni.
Broj država u zoni jednak je proizvodu broja atoma u kristalu do mnoštva razine atomske energije, iz kojeg je nastala zona. Pod mnoštvom razine energije shvaća se kao broj elektrona koji mogu biti na ovoj razini u skladu s principom Paula.
Zone dopuštenih energija odvojene su zonama zabranjenih energija. Njihova širina usporediva se s širinom zona dopuštenih energija. Uz povećanje energije, širina dopuštenih zona se povećava, a zabranjeno - smanjuje (sl. 57).
§2. Metali, poluvodiči, dielectrics
Razlike u električnim svojstvima krutog tijela objašnjene su raznim punjenjem elektrona dopuštenih energetskih zona i širine zabranjenih zona. Kako bi tijelo proveo električna energija Potrebno je imati slobodne razine energije u dopuštenim zonama koje se elektroni mogu nastaviti pod djelovanjem električnog polja.
Metali
Razmotrite natrijev kristal. Njegovu elektroničku formulu. Dijagram natrijevog energije prikazan je na Sl. 58.
Izolirani atom ima diskretni energetski spektar. Pod približavanjem atoma, počevši od određene interatomske udaljenosti, razina energije se uvlakavaju u zonu. Prije svega, vanjske razine su podijeljene: upražnjeno 3 rzatim pola ispunjena razina 3 s., S smanjenjem udaljenosti r.prije r. 1 kreće 3 r-i 3. s.- - izražena zona. Na udaljenosti r \u003d r. 0 (r. 0 je ravnotežna interatomska udaljenost u kristalu) približavanje atoma prestaje. Valentinovo 3. s.elektroni mogu zauzeti bilo koji uvjet unutar ove zone. Razine 1. s.i 2 s.može se podijeliti samo kada r.< r 0 i kemijskoj vezi ne sudjeluju. Kolegiranje se provodi kolektiv valentnih elektrona, čija je energetska stanja koja tvore zajedničku zonu dobivenu kao rezultat preklapanja.
U zoni dopuštenih energija formiranih valencijskim razinama, bit će 8 N. Države (broj s.Trošak 2 N.; broj rTrošak 6. N.). Atom ima jedan valentski elektron, tako da će u ovoj zoni biti N.elektroni, uvjeti zauzimanja u skladu s načelom Paula i načelom najmanje energije. Prema tome, dio država u slobodnoj zoni.
Kristali u kojima je zona formirana razinama elektrona valencija djelomično ispunjena, pripadaju Metali. Ova se zona naziva zona provođenja.
Poluvodiči i dielektrici
Razmotrite strukturu energije poluvodiča i dielektrika na tipičnom poluvodičkom silicij (Z \u003d 14), čija elektronička formula. U obrazovanju kristalna rešetkapočevši od neke interatomske udaljenosti r. 1 \u003e R. 0 (r. 0 - javlja se ravnotežna interatomska udaljenost u kristalu sp. 3-hibridizacija silicija elektroničkih stanja, koja ne dovodi samo na preklapanje 3 s.i 3. rzone i spajanje i formiranje jednog 3 sp. 3 Zona hibrida valencije (sl. 59), u kojoj je maksimalni broj elektrona 8 N., U kristalnom silicij, svaki atom oblikuje 4 tetraedralne veze, dovršavajući svoju valenciju školjku do osam elektrona. Kao rezultat toga, sve 8 u zonu valencije N.države su zauzete. Tako, u poluvodičima i dielektricima zona formirana razinama valentnih elektrona - Valentna zona (pt) - potpuno napunjena. Sljedeći upražnjeno 4. s.-Zone se ne preklapa s zonom valencije tijekom interatomske udaljenosti r. 0 i odvojio se od zone zabranjenih energija (Zz) . Elektroni koji se nalaze u valencijskoj zoni ne mogu sudjelovati u provodljivosti, budući da su zauzete sve države u zoni. Da bi se pojavili u kristalu, potrebno je prevesti elektrone iz zone valencije u sljedeću slobodnu zonu dopuštenih energija. Prva besplatna dopuštena zona koja se nalazi iznad zonu valence zovezona provodljivosti (ZP). Zove se energetski jaz između dna zone provođenja i stropa zone valencije Širinu zabranjene zone W g..
Ovisno o širini zabranjene zone, svi kristalna tijela podijeljena u tri razreda:
1. Metali - 0.1 EV;
2. poluvodiči -;
3. Dielectrics - ‰ 4 Ev.
Prema tome, tijelo ima takve specifične vrijednosti otpora:
1. Metali - ρ \u003d 10 -8 10 -6 ohm · m;
2. poluvodiči - ρ \u003d 10 -6 10 8 ohm · m;
3. Dielectrics - ρ\u003e 10 8 ohm · m.
Na temperaturi T. \u003d 0 poluvodiča su dielektrici, ali s povećanjem temperature, njihov otpor se oštro smanjuje. Dielectrics tijekom grijanja ranije taljenje nastaje od elektroničke vodljivosti.
Energetski spektar elektrona u krutom tijelu značajno se razlikuje od energetskog spektra slobodnih elektrona (koji je kontinuiran) ili elektronski spektar koji pripada pojedinačnim izoliranim atomima (diskretan s određenim skupom dostupnih razina) - sastoji se od odvojene dopuštene energije zone odvojene zonama zabranjenih energija.
Prema kvantnim mehaničkim postulatima bora, u izoliranom atomu, energija elektrone može biti strogo diskretne vrijednosti (elektron je na jednom od orbitalnih). U slučaju sustava od nekoliko atoma, u kombinaciji s kemijskom vezom, elektronske orbitale se podijeli u količini proporcionalnom broju atoma, formirajući takozvane molekularne orbitele. Uz daljnje povećanje sustava na makroskopsku razinu, broj orbitalija postaje vrlo velika, a razlika u elektronima u susjednoj orbitalnoj razini, odnosno, vrlo male energetske razine podijeljene su do dva gotovo kontinuirana diskretna seta - energetske zone.
Najveće dopuštene energetske zone u poluvodičima i dielektrici, u kojima se na temperaturi od 0 do svih energetskih stanja zauzimaju elektroni, naziva se valencija, nakon toga - zona provođenja. U vodičima, zona provođenja naziva se najveća dopuštena zona u kojoj se elektroni nalaze na temperaturi od 0 K. uzajamno mjesto Te su zone sve krutine i podijeljene u tri velike skupine (vidi sl.):
- vodiči - Materijali u kojima se zona provođenja i zona valencije preklapaju (bez energetskog razmaka), formiranje jedne zone koja se naziva zona provođenja (dakle, elektron se može slobodno kretati između njih, nakon što je primio bilo koju dopuštenu nisku energiju);
- dielectrics - materijali u kojima se zone ne preklapaju, a udaljenost između njih je više od 3 ev (kako bi se preveo elektron iz zone valencije u zoni vodljivosti zahtijeva značajnu energiju, tako da se dielektrična struja praktično ne provodi);
- poluvodiči - materijali u kojima se zone ne preklapaju i udaljenost između njih (širina zabranjene zone) leži u rasponu od 0,1-3 ev (kako bi se prevelo elektron iz zone valencije u zonu provođenja, energija je potreban manji nego za dielektrično, tako da čisti poluvodiči slabo preskoči struju).
Teorija zone je osnova suvremena teorija krutina. Mogla je razumjeti prirodu i objasniti najvažnija svojstva metala, poluvodiča i dielektrika. Veličina zabranjene zone (energetska jaza između zona valente i provodljivosti) je ključna vrijednost u teoriji zone i određuje optička i električna svojstva materijala. Na primjer, u poluvodičima, provodljivost se može povećati stvaranjem dopuštene razine energije u zabranjenoj zoni dopingom - dodatkom pripravak početnih baznih materijala nečistoća za promjenu njegove fizičke i kemijska svojstva, U ovom slučaju, kažu da je poluvodič je nečistoća. Stoga se stvaraju svi poluvodički uređaji: solarne ćelije, diode, čvrsto stanje i drugi. Prijelaz elektrona iz zone valencije na zonu provođenja naziva se proces stvaranja nosača naboja (negativni - elektron i pozitivne - rupe) , a obrnuti prijelaz je proces rekombinacije.
Teorija zone ima granice primjenjivosti, koje se odvijaju od tri glavne pretpostavke: a) potencijal kristalne rešetke je strogo periodična; b) interakcija između slobodnih elektrona može se reducirati na jedan-elektronski samo-konzistentni potencijal (i ostatak se razmatra metodom teorije poremećaja); c) Interakcija s fononima je slaba (i može se smatrati teorijom poremećaja).
Ilustracije
Autor
- Razumovsky Alexey sergeevich
Primijenjene promjene
- Nimushina Daria Anatolyevna
Izvori
- Fizički enciklopedijski rječnik, T. 2. - M.: Velika Ruska enciklopedija, 1995. - 89 str.
- Gurov V. A. Elektronika u čvrstom stanju. - m.: Tehnografija, 2008. - 19 s.
|
|||||||||||||||||||||
Konstrukcija zone elektroničkog energetskog spektra u krutim tvarima. Modeli slobodnih i visoko povezanih elektrona
3.2. Konstrukcija zone energetskog spektra u snažnom komunikacijskom modelu
3.2.1. Formiranje strukture zone energetskog spektra.
Dakle, u formiranju odnosa između dva atoma dviju atomskih orbitala, nastaju dva molekularna: vezanja i kidanje s različitim energijama.
Da vidimo sada ono što se događa u formiranju kristala. Ovdje su moguće dvije različite opcije: Kada rapprochet atoma nastaje metalno stanje i kada dođe do poluvodiča ili dielektričnog stanja.
Metalno stanje Može se pojaviti samo kao rezultat preklapanja atomskih orbitala i formiranja višestrukih orbitala, što dovodi do potpune ili djelomične kolektivizacije valentnih elektrona. Dakle, može se predstavljati metal, ako se postupak od pojma izvorno povezanih atomskih elektroničkih orbitala može biti predstavljen kao sustav pozitivno nabijenih iona u kombinaciji u jednu divovsku molekulu s jednim sustavom višestrukih molekularnih orbitala.
U prijelaznim i rijetkim zemljanim metalima, uz kolektivu elektrona metalnih komunikacija koje proizlaze iz kolektivizacije elektrona, također mogu postojati kovalentne usmjerene veze Između susjednih atoma s potpuno napunjenim vezanjem orbitalija.
Elektronska kolektiva, koja osigurava povezivanje svih atoma u rešetki, dovodi do pristupa atoma do 2n-više (uzimajući u obzir spin) cijepanje razine atomskih energije i formiranje konstrukcije zone elektroničkog energetskog spektra.
Visokokvalitetna ilustracija promjene diskretnih razina izoliranih atoma () s smanjenjem interatomske udaljenosti prikazana je na slici 30A, gdje se prikazuje cijepanje razine energije energetska zonakoji sadrže 2N (uzimajući u obzir spin) različitih energetskih stanja (Sl. 30A).
 |
| Sl. trideset. |
Širina energetskih zona (), kao što će biti prikazano u nastavku, ovisi o stupnju preklapanja valnih funkcija elektrona susjednih atoma ili, drugim riječima, po vjerojatnosti prijelaza elektrona na susjedni atomu. Općenito, energetske zone su odvojene zabranjenim energetskim intervalima zabranjene zone (Sl. 30A).
Na preklapanju S- i Pologisti formiraju se nekoliko "vezanja" i "pecivo" zona. Metalno stanje s ove točke gledišta događa se ako postoje zone koji nisu potpuno ispunjeni elektronima. Međutim, za razliku od slabe veze (modeli gotovo slobodnih elektrona), u ovom slučaju, elektronske valne funkcije se ne smatraju ravnim valovima, što uvelike komplicira postupak za izgradnju izoenergijskih površina. Priroda konverzije valnih funkcija lokaliziranih elektrona u valne funkcije tipa Bloch Tip koji opisuje kolektivne elektrone ilustriran je na slici 30b, u.
Ponovno bi trebalo naglasiti da je to kolektivizacija elektrona, odnosno mogućnost kretanja u kristalnoj rešetki, dovodi do cijepanja energetskih razina država i formiranje energetskih zona (sl. 30b).
Poluvodič (i Dielectric) stanje Koje pružaju usmjerene kovalentne veze. Gotovo svi atomski poluvodiči Oni imaju dijamantnu rešetku tipa, u kojoj svaki par atoma ima kovalentno-β-bljeskalicu formiran kao rezultat SP3-hibridizacije [n.Kuzmenhenko i sur., 2000]. Na svakom SP 3 postoje dva elektrona u svakom SP 3, postoje dva elektrona, tako da su sve obvezujuće orbitale u potpunosti napunjene.
Imajte na umu da u modelu lokaliziranih obveznica između parova susjednih atoma, formiranje kristalne rešetke ne bi trebalo dovesti do razdvajanja energetskih razina vezajućih orbitala. Zapravo, jedan sustav preklapanja SP3 formira se u kristalnoj rešetki, budući da je gustoća elektrona elektrona na-sredstva koncentrati ne samo u području prostora između atoma, već se razlikuje od nule i izvan tih područja , Kao rezultat preklapanja valnih funkcija, energetska razina vezanja i pečenja orbitala u kristalu su podijeljene u uske ne-preklapajuće zone: potpuno napunjena veza vezanja i energija koja se nalazi iznad - slobodna labava. Te su zone odvojene energetskom jazom.
Uz ne-nulte temperature pod djelovanjem toplinskog gibanja atoma atoma, kovalentne veze mogu se razbiti, a pušteni elektroni se prenose u gornju zonu na suznim orbitalima, na kojima se nisu lokalizirane elektroničkim stanjima. Tako se događa delokalizacija Pridruženi elektroni i formiranje određenog broja, ovisno o temperaturi i širini zabranjene zone, kolektivizirani elektroni. Kolektivizirani elektroni mogu se kretati u kristalnoj rešetki, formirajući zonu provođenja s odgovarajućim pravom disperzije. Međutim, sada, kao iu slučaju prijelazne metaleKretanje ovih elektrona u rešetki opisan je ne-ravnim valovima, ali s složenijim valnim funkcijama koje uzimaju u obzir valne funkcije vezanih elektroničkih stanja.
Kada je elektron uzbuđen iz jedne od kovalentnih veza, formira se rupa - prazno elektroničko stanje pripisuje se naplati+q. Kao rezultat prijelaza bilo kojeg elektrona iz susjednih veza s ovim stanjem rupe nestaje, ali u isto vrijeme se pojavljuje na susjednoj komunikaciji. Dakle, rupa se može kretati na kristalu. Kao i elektroni dezokalizirane rupe čine njihov spektar zone s odgovarajućim pravom disperzije. U vanjskom električnom polju, prijelazi elektrona na slobodnoj vezi prevladavaju u smjeru prema polju, tako da se rupe pomaknu duž polja, stvarajući električnu struju. Dakle, s termalnom uzbuđenjem u poluvodičima postoje dvije vrste strujnih nosača - elektrona i rupa. Njihova koncentracija ovisi o temperaturi, koja je karakteristična za poluvodičku vrstu vodljivosti.
Književnost: [U. Kharison, 1972, Ch. II, 6,7; DG Bnora i sur., 1990; K.V.Shalimova, 1985, 2.4; J. Zaimana i sur., 1972, Gl.8, 1]
3.2.2. Funkcija elektronske elektrone u kristalu
U modelu snage, funkcija elektrona vala u kristalu može biti predstavljena kao linearna kombinacija atomskih funkcija:
gdje r. - RADIUS-Vector Electron, r. j. - Radius-vektor j.Atomi tokara.
Budući da funkcija valova kolektiviziranih elektrona u kristalu treba imati bloka oblik (2.1), tada koeficijent IZ _ (J) s atomskom funkcijom j.Čvor kristalne rešetke treba imati oblik faze faktora, to jest
proporcionalno: n ~ t. Prema tome, koeficijent toplinske vodljivosti treba biti obrnuto proporcionalan temperaturi, koja je kvalitativno dosljedna s iskustvom. Na temperaturama u nastavku, Debaturevskayal praktično ne ovisi o OTT-u, a toplinska provodljivost je u potpunosti određena ovisnost o toplinskom kapacitetu kristala v. 3. Dakle, na niskim temperaturama3. Karakteristična ovisnost toplinske vodljivosti na temperaturi prikazana je na slici 9.
Osim toplinske vodljivosti rešetke, potrebno je uzeti u obzir toplinsku vodljivost zbog prijenosa topline s besplatnim elektronima. Upravo je ona objašnjava visoku toplinsku vodljivost metala u usporedbi s ne-metalima.
3. elektronička struktura kristala.
3.1. Elektronska generacija u povremenom polju. Konstrukcija zone elektronskog energetskog spektra u kristalu. Funkcije buve. Krivulje disperzije. Učinkovita masa.
U čvrstom tijelu udaljenosti između atoma usporedivi su s njihovim dimenzijama. Stoga elektronske školjke susjednih atoma djelomično se preklapaju jedni s drugima i barem valentne elektrone svakog atoma pokazuju da su u dovoljno snažno polje susjednih atoma. Točan opis Pokreti svih elektrona, uzimajući u obzir interakciju elektrona međusobno i s atomskim jezgri, iznimno je složen zadatak čak i za zasebni atomu. Stoga se obično koristi metoda samo-konzistentnog polja, u kojoj se zadatak svede na opis kretanja svakog pojedinog elektrona u području učinkovitog potencijala generira atomske jezgre i prosječno polje preostalih elektrona.
Prvi mi razmatramo strukturu energetske razine kristala, na temelju aproksimacije jake veze, u kojoj energija elektrona vezanja s njegovim atomom značajno prelazi kinetičku energiju njegovog pokreta od atoma na atom. Za velike udaljenosti Svaki od njih ima sustav uskih razina energije koji odgovara pripadajuće stanja elektrona s ionom. Pod približavanjem atoma, širina i visina potencijalnih barijera između njih se smanjuju, a zbog efekta tunela, elektroni se mogu preseliti
jedan atom na drugi, koji je popraćen širenjem razine energije i pretvarajući ih energetska zona, (Sl. 10). Konkretno, to se odnosi na slabo povezane valentirane elektrone koji se mogu lako premjestiti na kristal od atoma na atom, a do određene mjere postaju slični slobodnim elektronima. Elektroni dubljih razina energije su mnogo jači nego povezani s njihovim atomom. Oni čine uske energetske zone sa širokim intervalima zabranjenih energija. Na sl. 10 uvjetno predstavljene potencijalne krivulje i razine energije za na kristal. Ukupna priroda energetskog spektra elektrona ovisno o intersticijskoj udaljenosti, D, prikazana je na slici 11. U nekim slučajevima, gornje razine su izvezene toliko da se susjedne energetske zone preklapaju. Na sl. 11 Ovo se odvija u d \u003d d1.
Na temelju omjera nesigurnosti Heisenberg - Borona, širine energetske zone, Δε je povezan s vremenom elektrona boravka u određenoj sklop rešetke od strane odnosa: Δε τ\u003e h. Zbog efekta tunela, elektron može propuštati potencijalnu barijeru. Prema procjeni, s interatomskom udaljenosti D-1Aτ-10 -15 ° C i stogaδε / ~ 10-10 -19 j ~ 1 ev, tj. Širina zabranjene zone je oko jednog ili više EV. Ako se kristal sastoji od N atoma, onda svaka energetska zona sastoji se od N sublevela. Kristal od 1 cm3 je sadržan s N ~ 1022 atoma. Prema tome, uz širinu zone ~ 1 EV, udaljenost između stupova je ~ 10 -22 EV, koja je znatno manja od energije toplinskog pokreta u normalnim uvjetima. Ova udaljenost je tako beznačajna da se u većini slučajeva zone može smatrati gotovo kontinuiranim.
U savršenom kristalu atoma atoma koji se nalaze u čvorovima kristalne rešetke, formirajući strogo periodičnu strukturu. U skladu s tim, potencijalna energija elektrona, v (R), također periodično ovisi o prostornim koordinatama, tj. opsjednut emitirana simetrija:
rešetke, i (i \u003d 1,2,3, ...) - vektori glavnih emisija.
Funkcije valova i razine energije u periodičnom polju (1) određuju se rješavanjem Schrödingerove jednadžbe
predstavljajući proizvod jednadžbe ravnog trčanja vala, EI KR na periodičnom faktoru, u K (R) \u003d U K (R + A N), s periodom rešetka. Funkcije (3) pod nazivom Flea funkcije.
Kada je v (r) \u003d 0, jednadžba (2) ima otopinu u obliku ravnog vala:
gdje je m masa čestica. Označena je energetska ovisnost E iz valne piletine krivulja disperzije, Prema (5), u slučaju slobodnog elektrona, to je parabola. Po analogiji s slobodnim kretanjem, vektor u jednadžbi (3) naziva se valni vektor, AP \u003d H K - kvazi-impuls.
U aproksimaciji slabe povezanosti razmatra se kretanje gotovo slobodnih elektrona, što djeluje na neregnuto polje periodičnog potencijala ionskih jezgri. Za razliku od slobodnog kretanja, u periodičkom polju V (R), jednadžba (2) ima rješenje na svim vrijednostima. Područja dopuštenih energija izmjenjuju se s zonama zabranjenih energija. U modelu slabe komunikacije objašnjava se odraz electrona u kristalu.
Razmotrite ovo pitanje više. Stanje maksimalnog refleksije elektronskih valova u kristalu (stanje Wulf - Bragg) određuje se formulom (17) od CH.I. S obzirom na to da g \u003d n g, dobivamo:
Razmotrite sustav konačnih intervala koji ne sadrže vrijednosti k zadovoljavajućeg odnosa (7):
(- n g / 2 Područje promjene u trodimenziji - prostor koji daje formula (8) Za sve moguće smjerove određuje granice zone n - oh brillouin. Unutar svake Brilluene zone (n \u003d 1,2,3, ...), Electron Energy je kontinuirana funkcija, a na granicama zona će rastrgati jaz. Doista, prilikom izvođenja uvjeta (7) amplituda pada, ψ K (R) \u003d UK (R) EI KR i odražava se ψ -K (r) \u003d u - k (r) e -i valovi će biti isti, u K (R) \u003d U -K (R). Ovi valovi daju dva rješenja za jednadžbu Schrödingera: Ova značajka opisuje akumulaciju negativnog naboja na pozitivnim ionima, gdje je potencijalna energija najmanja. Slično tome, dobivamo iz formule (9b): ρ 2 (R) \u003d | ψ 2 (R) | 2 \u003d 4 U g / 2 2 (r) grijeh 2 (gr / 2) Ova funkcija opisuje takvu raspodjelu elektrona u kojima se nalaze uglavnom u područjima koja odgovaraju srednjim udaljenostima između iona. U isto vrijeme, potencijalna energija će biti veća. Funkcije ψ 2 će odgovarati E2\u003e E1 energiji. zabranjene zone npr širine. Energija E`1 određuje gornju granicu prve zone, a energija E2 je donja granica druge zone. To znači da u širenju elektronskih valova u kristalima postoje područja energetskih vrijednosti za koje nema rješenja jednadžbe Schrödingera koja ima valnu prirodu. Budući da priroda energetske ovisnosti o valnom vektoru značajno utječe na dinamiku elektrona u kristalu, od interesa je da razmotrimo, primjerice najjednostavniji slučaj linearnog lanca atoma koji se nalazi na udaljenosti i jedan od drugog duž x os. U ovom slučaju g \u003d 2π / a. Slika 12 prikazuje krivulje disperzije za tri prve jednodimenzionalne briline zone: (- π / A.< k <π
/a), (-2π
/a < k < -π
/a; π/
a < k < 2π
/a), (-3π/
a < k < -2π
/a; 2π
/a < k < 3π
/a). К запрещенным зонам относятся области энергии Е`1
< E < E2
, E`2
< E.< E3
и т.д. Na sl. 12 prikazano shema proširene zone, u kojoj su razne energetske zone smještene u prostoru u raznim briljinim zonama. Međutim, to je uvijek moguće, a često i prikladno, odaberite val vektora tako da kraj njega leži unutar prve briline zone. Pišemo funkciju buha u obliku: leži u prvoj brillskoj zoni. Zamjena formule (11), dobivamo: ima oblik funkcije buha s faktorom Bloch (13). Indeks n sada ukazuje na broj energetske zone na koju ova funkcija pripada. Nazvan je postupak za donošenje proizvoljnog vektora valova u prvu brilin zonu sheme smanjenih zona, U ovoj shemi, vektor prihvaća vrijednosti -G / 2< k < g/2
, но одному и тому же значениюк
будут отвечать различные значения энергии, каждое из которых будет соответствовать одной из зон. На рисунке 13 представлена схема приведенных зон для одномерной решетки, соответствующая расширенной зонной схеме на рисунке 12. Stoga je postojanje energetskih zabranjenih zona posljedica bragg odraz elektroničkih valova de broglyl iz kristalnih zrakoplova. GAP bodovi se određuju uvjetima za maksimalno odraz valova. Prema zakonima kvantne mehanike, progresivno kretanje elektrona smatra se kretanjem valnog paketa s valnim vektorima blizu vektora. Brzina grupe valnog paketa, V je određena izrazom. Najvrednija izjava u modernoj fizici koja je dovoljna za razumijevanje svi Svojstva krutih tijela - hipoteza o njihovoj atomskoj strukturi .
Razmotrite na temelju atomske hipoteze o ideji kretanja elektrona u krutim tijelima. Odlično je pokušati povezati svojstva čvrstog tijela sa svojstvima jednog atoma. Svojstva atoma su dobro proučavana eksperimentalno i teoretski interpretirana kvantnom mehanika. Mogu se sažeti kako slijedi. 1. Elektron se kreće oko atomske jezgre, može biti ne u bilo kojem stanju, ali samo u jednom od takozvani stacionarne države. 2. Status karakterizira određena distribucija energetske i elektronske gustoće. Agregat stacionarnih stanja oblikuje elektronski energetski spektar u atomu. Energetski spektar je apsolutno individualan za svaki atom, ovo je vrsta otiska prsta. Distribucija elektronske gustoće pokazuje u kojima se područja oko elektronskog atoma pretežno, to jest, s vjerojatnošću blizu 1. Energetski spektar je napravljen u obliku dijagrama energije (Sl. 1.1). Država s minimalnom energijom naziva se glavna. Elektron se nalazi najbliži kernelu. Sl.1.1. Energetski spektar atoma vodika. definirana su elektronska svojstva kristala, kao i svojstva atoma, dva čimbenika - energetski spektar elektrona u kristalu i njihove statistike, odnosno, to jest, zakon o distribuciji od strane država. Struktura energetskog spektra kristala je kvalitativno razjašnjena, na temelju spektra odvojenog atoma. Zamislite sebe N. Isti atomi uklonjene na tako velike udaljenosti koje ne utječu jedni na druge. Energetski spektar takvog ansambla neovisnih atoma sastojat će se od N. Slučajni atomski spektri. Svako atomsko stanje bit će istovremeno status ansambla. Takve države čije se energiju podudaraju se nazivaju n - višestruka degenerirana. Počnimo zatvaranje atoma. Na određenoj interatomskoj udaljenosti bit će vidljive elektrostatičke sile elektro-nuklearne atrakcije i elektron-e-odbijanja. Ukupno prevladavanja privlačenja, ali odbijanja će dovesti do činjenice da se prethodno poklopilo atomske razine energije uplit N. pojedinačne razine (sl.1.4). Kada se dostigne interatomska udaljenost, formira se kristal. Daljnje približavanje ometaju velike prednosti. Sl.1.4. Obrazovanje energetskog spektra kristala Svaka atomska razina se tako uključuje zonu riješenih energija elektrona u kristalu širina. Ako je zbroj polu-širine susjednih zona manji od udaljenosti između odgovarajućih atomskih razina, tada se dopuštene zone su odvojene zabranjena zona , Ako količina polususa prelazi udaljenost između razina, susjedne dopuštene zone preklapaju se, tvoreći jednu, širu, dopuštenu zonu. Opisana slika formiranja energetskog spektra primjenjiv je na metalne kristale, poluvodiči i dielektrike. Koji tip pripada određenom kristalu, određenom brojem elektrona Z u atomu. Ako a Z- Mlađi broj, zatim Z / 2. Najniže dopuštene zone bit će potpuno ispunjene, a ostatak je prazan. Pojam "ispunjena zona" treba shvatiti u smislu da postoji točno u kristalu N. elektroni s energijama koje pripadaju ovoj dopuštenoj zoni. Najviše ispunjene zone naziva se zona valencije, a sljedeće je prazna zona provođenja. Kristali s takvim punjenjem zona nazivaju se dielectrics.