Glicerin reagira s bakrom. Kvalitativna reakcija na glicerin - specifična, pomaže u otkrivanju
Glicerin ili prema međunarodnoj nomenklaturi propantriol -1,2,3 - složena tvar, koji spada u polihidrične alkohole, točnije je trohidrični alkohol, jer ima 3 hidroksilne skupine - OH. Kemijska svojstva glicerol su slični onima od, međutim, izraženiji su zbog činjenice da ima više hidroksilnih skupina i međusobno utječu.
Glicerin je, kao i alkoholi s jednom hidroksilnom skupinom, vrlo topljiv u vodi. To je, moglo bi se reći, i kvalitativna reakcija na glicerin, budući da se otapa u vodi u gotovo bilo kojem omjeru. Ovo svojstvo koristi se u proizvodnji antifriza - tekućina koje ne smrzavaju i ne hlade motore automobila i zrakoplova.
Također, glicerin je u interakciji s kalijevim permanganatom. Ovo je kvalitativna reakcija na glicerin, koji se također naziva Scheele vulkan. Za njegovu provedbu potrebno je dodati 1-2 kapi bezvodnog glicerina u prah kalijevog permanganata, koji se u obliku tobogana s udubljenjem ulijeva u porculansku zdjelu. Nakon minute, smjesa se spontano zapali. veliki broj topline, kao i raspršiti vruće čestice produkta reakcije i vodene pare. Ova reakcija je redoks.

Glicerin je higroskopan, tj. sposobni zadržati vlagu. Na tom se svojstvu temelji sljedeća kvalitativna reakcija na glicerin. Izvodi se u dimnoj haubi. Za njegovu provedbu ulijte oko 1 cm3 kristalnog kalijevog hidrogen sulfata (KHSO4) u čistu, suhu epruvetu. Dodajte 1-2 kapi glicerina, a zatim zagrijavajte dok se ne pojavi oštar miris. Kalijev hidrogen sulfat ovdje djeluje kao tvar koja upija vodu, koja se počinje očitovati kada se zagrije. Glicerin, koji gubi vodu, pretvara se u nezasićeni spoj - akrolein, koji ima oštar neugodan miris. C3H5 (OH) 3 - H2C = CH-CHO + 2 H2O.
Reakcija glicerina s bakrenim hidroksidom je kvalitativna i služi za određivanje ne samo glicerina, nego i drugih.Za njezino izvođenje u početku je potrebno pripremiti svježu otopinu bakrenog (II) hidroksida. Da biste to učinili, dodajte i dobijete bakrov hidroksid (II), koji stvara plavi talog. U ovu epruvetu s sedimentom dodajte nekoliko kapi glicerina i primijetite da je sediment nestao, a otopina je postala plava.

Dobiveni kompleks naziva se bakrov alkoholat ili glicerat. Kvalitativna reakcija za glicerin s bakrenim (II) hidroksidom koristi se ako je glicerin u čistom obliku ili u vodenoj otopini. Za provođenje takvih reakcija u kojima je glicerin prisutan s nečistoćama, potrebno ga je prethodno pročistiti od njih.
Kvalitativne reakcije na glicerin pomažu ga otkriti u bilo kojem okruženju. Aktivno se koristi za određivanje glicerina u hrani, kozmetici, parfemima, lijekovima i antifrizima.
DEFINICIJA
Glicerol je bezbojna, viskozna, sirupasta tekućina slatkog okusa. Nije otrovno. Glicerin je bez mirisa.
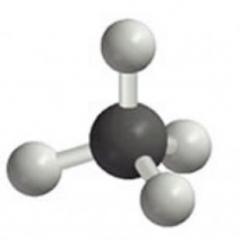
Njegove točke taljenja i vrelišta su 18°C odnosno 290°C. Glicerin je higroskopan, dobro se miješa s vodom i etanolom. Apsolutno čisti bezvodni glicerin skrući se na +18 o C, ali ga je iznimno teško dobiti u čvrstom obliku. Struktura molekule glicerola prikazana je na Sl. 1.
Riža. 1. Struktura molekule glicerola.
Glicerin je široko rasprostranjen u prirodi. Ima važnu ulogu u metaboličkim procesima u životinjskim organizmima, dio je većine lipida – masti i drugih tvari sadržanih u životinjskim i biljnim tkivima i obavljajući bitne funkcije u živim organizmima.
Dobivanje glicerina
Najstarija metoda za proizvodnju glicerina je hidroliza masti i ulja:

Trenutno se glicerin sintetički proizvodi iz propilena, koji nastaje tijekom pucanja ulja. U ovom slučaju koriste se različiti načini pretvaranja propilena u glicerin. Metoda koja najviše obećava je oksidacija propilena atmosferskim kisikom u prisutnosti katalizatora i na visokim temperaturama (kat = Cu, t 0 = 370). Proces prolazi kroz nekoliko faza.
Kemijska svojstva glicerina
Glicerin je predstavnik trihidričnih alkohola, za koje su, kao i za spojeve koji sadrže hidroksil, karakteristične iste reakcije kao i za monohidratni alkoholi.
Glicerin reagira s aktivnim metalima (kalij, natrij itd.) koji zamjenjuju vodik u svim hidroksilnim skupinama, reagiraju s vodikovim halogenidima (HCl, HBr, itd.), u reakciji dehidracije, tvoreći različite etere.
Glicerin također ima specifična svojstva koja ga razlikuju od monohidričnih alkohola: reagira ne samo s alkalnim metalima, već i s nekim bazama, uključujući netopive, na primjer, s bakrovim (II) hidroksidom:

Rezultat reakcije glicerina s bakrovim (II) hidroksidom je bakrov glicerat (složen kompleksni spoj svijetlo plave boje). Ova reakcija je kvalitativna reakcija na polihidrične alkohole.
U praktičnom smislu najvažnija je reakcija nitriranja glicerina, koja rezultira stvaranjem trinitroglicerina C 3 H 5 (ONO 2) 3:

Korištenje glicerina
Glicerin je sastavni dio mnogih namirnica, krema i kozmetike.
Primjeri rješavanja problema
PRIMJER 1
U epruvetu se stave 2 kapi otopine bakrenog sulfata, 2 kapi otopine natrijevog hidroksida i pomiješaju - nastaje plavi želatinasti talog bakrenog (II) hidroksida. Dodajte 1 kap glicerina u epruvetu i protresite sadržaj. Talog se otapa i pojavljuje se tamnoplava boja zbog stvaranja bakrenog glicerata.
Procesna kemija:
Bakar glicerat
Glicerin je trihidrični alkohol. Njegova kiselost je veća od kiselosti monohidričnih alkohola: povećanje broja hidroksilnih skupina pojačava kiseli karakter.
Glicerin lako stvara glicerate s hidroksidima teških metala. Međutim, njegova sposobnost stvaranja metalnih derivata (glicerata) s viševalentnim metalima objašnjava se ne toliko njegovom povećanom kiselošću, koliko činjenicom da u tom slučaju nastaju intrakompleksni spojevi, koji su posebno stabilni. Spojevi ove vrste nazivaju se keliranim (od grčkog "hela" - kandža).
Reakcija s bakrenim hidroksidom je kvalitativna reakcija za polihidrične alkohole i omogućuje njihovo razlikovanje od monohidričnih alkohola.
Oksidacija etil alkohol bakreni oksid
Stavite 2 kapi etilnog alkohola u suhu epruvetu. Držeći pincetom spiralu od bakrene žice, zagrijavajte je u plamenu alkoholne lampe dok se ne pojavi crni premaz bakrenog oksida. Još vruća spirala umoči se u epruvetu s etilnim alkoholom. Crna površina zavojnice odmah postaje zlatna zbog redukcije bakrenog oksida. Istodobno se osjeća karakterističan miris acetaldehid(miris jabuke).
Stvaranje acetaldehida može se otkriti reakcijom boje sa sumpornom kiselinom. Da biste to učinili, stavite 3 kapi otopine fuksin sumporne kiseline u epruvetu i pipetom dodajte 1 kap dobivene otopine. Pojavljuje se ružičasto-ljubičasta boja. Napišite jednadžbu za reakciju oksidacije alkohola.
Oksidacija alkohola smjesom kroma
U suhu epruvetu stavite 2 kapi etilnog alkohola, dodajte 1 kap otopine sumporne kiseline i 2 kapi otopine kalij-dikromata. Narančasta otopina zagrijava se nad plamenom alkoholne lampe dok boja ne promijeni plavkasto-zelenu. Istodobno je karakterističan miris acetaldehida.
Provedite sličnu reakciju koristeći izoamil alkohol ili drugi dostupni alkohol, primjećujući miris nastalog aldehida.
Objasnite kemiju procesa kemiju procesa pisanjem jednadžbi odgovarajućih reakcija .
Oksidacija etilnog alkohola otopinom kalijevog permanganata
U suhu epruvetu stavite 2 kapi etilnog alkohola, 2 kapi otopine kalijevog permanganata i 3 kapi otopine sumporne kiseline. Pažljivo zagrijte sadržaj epruvete nad plamenom plamenika, ružičasta otopina postaje bezbojna. Postoji karakterističan miris acetaldehida, koji se također može otkriti reakcijom boje s fuksin sumpornom kiselinom.
Procesna kemija : (napišite jednadžbu reakcije).
Alkoholi se lakše oksidiraju od odgovarajućih zasićenih ugljikovodika, što se objašnjava utjecajem hidroksi skupine prisutne u njihovoj molekuli. Primarni alkoholi se oksidacijom pretvaraju u aldehide u blagim uvjetima, a u kiseline u težim uvjetima. Sekundarni alkoholi oksidacijom daju ketone.
Iskustvo 4. Interakcija glicerina s bakrovim (II) hidroksidom
Reagensi i materijali: glicerin; bakreni sulfat, 0,2 N. riješenje; kaustična soda, 2 n otopina.
Objavljeno na ref.rf
Stavite u epruvetu 2 kapi otopine bakrovog sulfata, 2 kapi otopine natrijevog hidroksida i promiješajte - nastaje plavi želatinasti talog bakrenog (II) hidroksida. Dodajte 1 kap glicerina u epruvetu i protresite sadržaj. Talog se otapa i pojavljuje se tamnoplava boja zbog stvaranja bakrenog glicerata.
Procesna kemija:

Glicerin je trihidrični alkohol. Njegova kiselost je veća od kiselosti monohidričnih alkohola: povećanje broja hidroksilnih skupina pojačava kiseli karakter.
Objavljeno na ref.rf
Glicerin lako stvara glicerate s hidroksidima teških metala.
Istodobno, njegova sposobnost stvaranja metalnih derivata (glicerata) s viševalentnim metalima objašnjava se ne toliko njegovom povećanom kiselošću, koliko činjenicom da u tom slučaju nastaju unutarkompleksni spojevi, koji su posebno stabilni. Veze ovog tipa često se nazivaju kelirani(od grčkog ʼʼhelaʼʼ - kandža).
Iskustvo 4. Interakcija glicerina s bakrovim (II) hidroksidom - pojam i vrste. Klasifikacija i značajke kategorije "Iskustvo 4. Interakcija glicerina s bakrenim (II) hidroksidom" 2017., 2018.
Lekcija br. 5 Kočni sustav Tema br. 8 Upravljački mehanizmi O uređaju automobilske tehnologije Izvođenje grupni sat Plan - sinopsis Nastavnik ciklusa POPON, potpukovnik Fedotov S.A. "____" ....
Iz položaja I mirno okrećemo ključ za 180° u položaj II. Čim dođete u drugu poziciju, neka svjetla na instrument ploči će se sigurno upaliti. To mogu biti: lampica upozorenja za punjenje baterije, lampica za hitni pritisak ulja, ....
12. ; CA - toplinski kapacitet [voda + metal] prvog dijela hladnjaka 3. Linearizacija. se prevodi u jednadžbu dinamike kapaciteta "A". Jednadžba konačnog oblika: u relativnom obliku. II. Jednadžba kontrolnog objekta, čija se kontrola također provodi ....
Selektivno je zaštitno djelovanje u kojem se isključuje samo oštećeni element ili dio. Selektivnost je osigurana kako različitim postavkama zaštitnih uređaja, tako i upotrebom posebnih sklopova. Primjer osiguravanja selektivnosti s...
U eri helenizma u kiparstvu postoji pojačana žudnja za pompom i groteskom. U nekim djelima prikazane su pretjerane strasti, u drugima je uočljiva pretjerana bliskost s prirodom. U to su vrijeme počeli marljivo kopirati kipove ranijih vremena; zahvaljujući kopijama, danas mnoge poznajemo....
U XI stoljeću. u Francuskoj su se pojavili prvi znakovi oživljavanja monumentalne skulpture. Na jugu zemlje, gdje je bilo mnogo antičkih spomenika i tradicija kiparstva nije potpuno izgubljena, nastala je ranije. Tehnička opremljenost majstora na početku ere bila je ...
Počeci francuske gotičke skulpture postavljeni su u Saint Denisu. Tri portala zapadnog pročelja slavne crkve ispunjena su skulpturalnim slikama, u kojima se najprije očitovala želja za strogo promišljenim ikonografskim programom, javila se želja ...
ISTANBULSKA DEKLARACIJA O NASELJAMA. 1. Mi, šefovi država i vlada i službena izaslanstva zemalja, okupili smo se na Konferenciji Ujedinjenih naroda o ljudskim naseljima (Habitat II) u Istanbulu, Turska, od 3. do 14. lipnja 1996., ....
Fantastične glave vrlo su cijenili njegovi suvremenici, talijanski je majstor imao mnogo imitatora, ali se nitko od njih nije uspio usporediti po živosti i inventivnosti s Archimboldovim portretnim kompozicijama. Giuseppe Arcimboldo Hilliard, ....