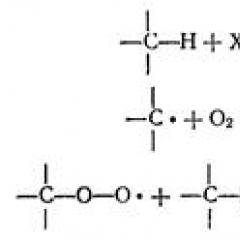
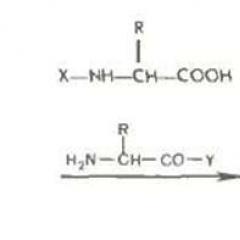
Общи и специфични метаболитни пътища. Основните биохимични пътища на микробиологичната трансформация на замърсителите
Въведение в метаболизма (биохимия)
Метаболизмът или метаболизмът е комбинация от химични реакции в организма, които осигуряват неговите вещества и енергията, необходима за живота. Процесът на метаболизъм, придружен от образуването на по-прости съединения от комплекс, се обозначава с термина - катаболизъм. Процесът идва в обратна посока и водещ, в крайна сметка, до образуването на сложен продукт от сравнително по-опростен - анаболизъм. Анаболните процеси са придружени от консумация на енергия, катаболен - освобождаване.
Анаболзът и катаболизмът не са проста реакция на реакции. Анаболните пътища трябва да се различават от пътните пътеки най-малко една от ензимните реакции, които трябва да бъдат регулирани независимо и поради контролиране на активността на тези ензими, общата скорост на разпадане и синтеза на вещества се регулира. Ензимите, които определят скоростта на целия процес като цяло, се наричат \u200b\u200bключ.
Освен това, пътят, по който катаболизмът на една или друга молекула може да бъде неподходяща за нейния синтез за енергийни съображения. Например, глюкозното разцепване на глюкоза към пируват е процес, състоящ се от 11 последователни етапа, катализирани чрез специфични ензими. Изглежда, че синтезът на глюкоза от Пируват трябва да бъде прост призив на всички тези ензимни етапи от нейното разпадане. Такъв път се появява на пръв поглед и най-естествения и най-икономичен. В действителност обаче биосинтезата на глюкозата (Glukegenesis) в черния дроб тече по различен начин. Тя включва само 8 от 11-те ензимни етапа, участващи в неговата гниене, и 3 липсващи етапа се заменят в нея чрез напълно различен набор от ензимни реакции, присъщи на този биоситинтетичен път. В допълнение, отговорите на катаболизма и анаболизма често са разделени от мембраните и продължават в различни клетки.
Таблица 8.1. Допълване на някои метаболитни пътеки в хепатоцит
|
Допълнение |
Метаболитни пътеки |
|---|---|
|
Цитозол |
Glycoliz, много реакции на глюконеогенеза, активиране на аминокиселина, синтез на мастни киселини |
|
Плазмената мембрана |
Енергийни транспортни системи |
|
ДНК репликация, синтез на различни видове РНК |
|
|
Рибозоми |
Протеин от синтез |
|
Лизозоми |
Изолация на хидролитични ензими |
|
Голджи Комплекс |
Образуване на плазмената мембрана и секреторни мехурчета |
|
Микромомери |
Локализация на оксидазите на каталаза и аминокиселини |
|
Ендоплазмения ретикулум |
Синтез Липид |
|
Митохондрия |
Цикъл на трикарбоксилна киселина, дишане на тъкани, окисление на мастни киселини, окислително фосфорилиране |
Метаболизмът изпълнява 4 функции:
1. снабдяване на организма на химическата енергия, получена чрез разделяне на богатата енергия на хранителните вещества;
2. преобразуването на хранителни вещества в строителните блокове, които се използват в клетката за биосинтеза на макромолекули;
3. сглобяване на макромолекулярни (биополимери) и супрамолекулни структури на жив организъм, пластмаса и енергийно поддържане на неговата структура;
4. Синтез и унищожаване на тези биомолекули, които са необходими за извършване на специфични характеристики на клетката и тялото.
Метаболитният път е поредица от химически трансформации на конкретно вещество в тялото. Междинните продукти, образувани по време на процеса на трансформация, се наричат \u200b\u200bметаболити, а последната връзка на метаболитната пътека е крайният продукт. Пример за метаболитен път е гликолис, синтез на холестерол.
Метаболитният цикъл е такъв метаболитен път, един от крайните продукти е идентичен с една от връзките, свързани с този процес. Най-важните метаболитни цикли в човешкото тяло са цикълът на трикарбоксилни киселини (цикъл на Krebs) и цикъла на орнитин.
Почти всички метаболитни реакции са в крайна сметка, тъй като продуктът на една ензимна реакция служи като субстрат за друг, който в този процес играе ролята на следващия етап. Така метаболизмът може да бъде представен като изключително сложна мрежа от ензимни реакции. Ако потокът от хранителни вещества в някаква част от тази мрежа намалява или се прекъсва, тогава промените могат да възникнат в друга част на мрежата в отговор, за да може тази първа промяна да бъде някак балансирана или компенсация. Освен това, както катаболическите, така и анаболните реакции се коригират по такъв начин, че те да продължат най-икономично, т.е. с най-ниската енергия и вещества. Например, окисляването на хранителните вещества в клетката се извършва със скорост, достатъчно достатъчно, за да задоволи енергийните нужди в момента.
Специфичен и споделен катаболизъм
Три етапа се различават в катаболизма:
1. Полимерите се превръщат в мономери (протеини - в аминокиселини, въглехидрати в монозахариди, липиди - в глицерол и мастна киселина). Химичната енергия се разсейва под формата на топлина.
2. Мономерите се превръщат в общи продукти, в огромното мнозинство в ацетил-кола. Химичната енергия се разсейва частично под формата на топлина, частично се натрупва под формата на възстановени коефициентни форми (NADB, FADN2), частично източници в макроергичните връзки на АТР (фосфорилиране на субстрат).
Първият и 2-ри етап от катаболизма принадлежат към специфичните пътища, които са уникални за метаболизма на протеини, липиди и въглехидрати.
3. Крайният етап на катаболизма се намалява до окисляването на ацетил-охладите до С02 и Н20 в реакциите на цикъла на трикарбоксилната киселина (CREC цикъл) - общия път на катаболизма. Окислителни реакции Общият път на катаболизма е конюгат с дишаща верига на тъканта. В същото време, енергията (40-45%) е под формата на АТР (окислително фосфорилиране).
В резултат на специфичните и общи пътища на катаболизма, биополимери (протеини, въглехидрати, липиди) се разпадат до СО2, Н20 и NH3, които са основните ограничени катаболни продукти.
Метаболити нормално и с патология
В жива клетка се образуват стотици метаболити всяка секунда. Въпреки това, техните концентрации се поддържат на определено ниво, което е специфична биохимична постоянна или референтна стойност. По време на заболявания има промяна в концентрацията на метаболитите, която е в основата на биохимичната лабораторна диагностика. Нормалните метаболити включват глюкоза, урея, холестерол, обикновен серумен протеин и редица други. Изходът на концентрацията на тези вещества извън границите на физиологичните норми (увеличаване или спад) показва нарушение на техния обмен в организма. Освен това, редица вещества в организма здравословен човек Той се намира само в определени биологични течности, което е причинено от спецификата на техния метаболизъм. Например, серумните протеини обикновено не преминават през бъбречния филтър и съответно не са открити в урината. Но с възпалението на бъбреците (гломерулонефрит), протеините (предимно албумин) проникват в солената капсула, се появяват в урината - протеинурия и се интерпретират като патологични компоненти на урината.
Патологични метаболити са миеломни протеини (протеини от бен-джоунс), парапротеини в макроглобулинемия на Valden пръчки, натрупване на аномален гликоген по време на гликогенази, различни фракции на сложни липиди по време на сфинголипидо и др. Те се срещат само за болести и за здраво тяло не е характерно.
Нива, изучаващи метаболизма
Нива на учебния метаболизъм:
1. Целият организъм.
2. Изолирани органи (перфлусируеми).
3. тъканни участъци.
4. Клетъчни култури.
5. Хомогенати на тъканите.
6. Изолирани клетъчни органели.
7. Молекулно ниво (пречистени ензими, рецептори и др.).
Много често, радиоактивни изотопи (3 Н, 32 р, 14С, 35 s, 18 О) се използват за изследване на метаболизма, които са обозначени вещества, въведени в тялото. След това можете да проследите клетъчната локализация на тези вещества, за да определите полуживота и техните метаболитни пътеки.
Фиг. 8.1. Специфични и общи катаболни пътища
Глава 9. Биологични мембрани
Клетката представлява биологичната система, като основата на която е мембранната структура, разделяща клетката от външната среда, образувайки отделенията (отделенията), както и осигуряване на получаването и отстраняването на метаболитите, възприятието и предаването на сигнали и са структурни организатори на метаболитни пътеки.
Договореното функциониране на мембранните системи - рецептори, ензими, транспортни механизми помага за поддържане на клетъчната хомеостаза и в същото време бързо реагира на промените във външната среда.
Мембраните са нейлъсовни супрамолекулни структури. Протеините и липидите в тях се държат заедно от много нековалентни взаимодействия (кооперация по природа).
Основните функции на мембрани могат да бъдат приписани:
1. разделяне на клетките от околната среда и образуването на вътреклетъчни отделения (отделения);
2. контрол и регулиране на транспортирането на огромно разнообразие от вещества чрез мембрани (избирателна пропускливост);
3. участие в предоставянето на междуклетъчни взаимодействия;
4. Предаване на възприятие и сигнала в клетката (приемане);
5. локализация на ензимите;
6. Функция за трансформиране на енергия.
Мембраните са асиметрични в структурната и функционална връзка (въглехидратите винаги са локализирани навън и не са от вътрешната страна на мембраната). Това са динамични структури: Протеинът и липидите, включени в техния състав, могат да се движат в мембранната равнина (странична дифузия). Въпреки това, има и преход от протеини и липиди от едната страна на мембраната към друга (напречна дифузия, флип флоп), който се случва изключително бавен. Мобилността и плавността на мембрани зависят от неговия състав: съотношенията на наситени и ненаситени мастни киселини, както и холестерол. Плавността на мембраната е по-ниска от по-високата наситеност на мастните киселини във фосфолипидите и повече съдържание холестерол. В допълнение, мембраната се характеризира със самостоятелност.
Общи свойства на клетъчните мембрани:
1. лесно пропускливи за вода и неутрални липофилни съединения;
2. в по-малка степен, пропускливи за полярни вещества (захар, амиди);
3. Лошо пропусклив за малки йони (Na +, Cl - et al.);
4. характеризираща висока електрическа устойчивост;
5. асиметрия;
6. може спонтанно да възстанови целостта;
7. ликвидност.
Химичен състав на мембрани.
Мембраните се състоят от липидни и протеинови молекули, относителното количество, от което различни мембрани са широко променени. Въглехидратите се съдържат под формата на гликопротеини, гликолипиди и са 0.5% -10% от веществата на мембраната. Според течния мозаечен модел на структурата на мембраната (Senjer и Nicholson, 1972) основата на мембраната е двоен липиден слой, при образуването на фосфолипиди и гликолипиди. Липидният двуслой е оформен от два реда липиди, чиито хидрофобни радикали са скрити вътре и хидрофилните групи се изключват и в контакт с водната среда. Протеинови молекули, сякаш се разтварят в липид и сравнително свободно "плуват в липидното море под формата на айсберги, на които растат дърветата на глицикалите."
Мембрани за липиди.
Мембранните липиди са амфифилни молекули, т.е. Молекулата има и хидрофилни групи (полярни глави) и алифатни радикали (хидрофобни опашки), спонтанно оформящи двуслойни, при които липидните опашки са адресирани един към друг. Дебелината на един липиден слой е 2.5 пМ, от която 1 nm отчита главата и 1,5 nm върху опашката. Има три основни вида липиди в мембрани: фосфолипиди, гликолипиди и холестерол. Средното моларно съотношение на холестерола / фосфолипидите е 0.3-0.4, но в плазмената мембрана това съотношение е много по-високо (0.8-0.9). Наличието на холестерол в мембраните намалява подвижността на мастните киселини, намалява страничната дифузия на липидите и протеините.
Фосфолипидите могат да бъдат разделени на глицеосфолипиди и сфингофосполипиди. Най-често срещаните глицеофолипиди мембрани - фосфатидилхолини и фосфатидилтатоламоламини. Всеки глицелипид, например фосфатидилхолин, е представен от няколко десетки фосфатидилхолини, различаващи се един от друг чрез структурата на остатъците от мастни киселини.
Делът на глицеосфолипидите представлява 2-8% от всички мембранни фосфолипиди. Най-често е фосфатидилозит.
Специфични фосфолипиди на вътрешната мембранна митохондрии - кардиолипини (дифосфатидглицери), изградени на базата на глицерол и две остатъци от фосфатидна киселина, са около 22% от всички фосфолипиди митохондрични мембрани.
В миелинът на нервните клетки в значителни количества съдържат шпингомиелини.
Мембраните гликолипиди са представени от мозъчни и ганглиозиди, в които хидрофобната част е представена от керамид. Хидрофилната група е въглехидратна остатък - гликозидна връзка, прикрепена към хидроксилната група на първия въглероден атом на керамида. При значителни количества гликолипиди са в пещи на мозъчни клетки, епител и червени кръвни клетки. Ганглозиди на еритроцити от различни индивиди се различават по структурата на олигозахаридните вериги и проявяват антигенни свойства.
Холестеролът присъства във всички мембрани на животинските клетки. Неговата молекула се състои от твърда хидрофобна ядро \u200b\u200bи гъвкава въглеводородна верига, една хидроксилна група е полярна глава.
Функции на мембранни липиди.
Мембрани за фосфо и гликолипиди, в допълнение към участието в образуването на липид двуслой, изпълняват няколко други функции. Мембрани липидите образуват среда за функциониране на мембранните протеини, които приемат естествена конформация в нея.
Някои мембранни липиди са предшественици на вторични посредници при прехвърляне на хормонални сигнали. Така фосфатидилиндалд фосфат под влиянието на фосфолипаза с хидролизиран към диацилглицерол и иноситатрипосфат, които са вторични хормонни посредници.
Редица липиди участват в фиксирането на здрави протеини. Пример за припокриващ протеин е ацетилхолинестераза, който е фиксиран върху постсинаптична мембрана към фосфатитининозитол.
Мембранни протеини.
Мембранните протеини са отговорни за функционалната активност на мембрани и техните дялове варират от 30 до 70%. Мембънните протеини се различават по положение в мембраната. Те могат дълбоко да проникнат в липидния двуслой или дори пронизващи го - интегрални протеини, по различни начини за прикрепване към мембраната - повърхностни протеини, или, до ковалентно контакт с него - привлечени протеини. Повърхностните протеини са почти винаги гликозилирани. Олигозахаридните остатъци защитават протеиновия протеин, участват в разпознаване на лиганди и адхезия.
Протеини, локализирани в мембраната, изпълняват структурни и специфични функции:
1. транспорт;
2. ензимно;
3. рецептор;
4. Антигенен.
Механизми на мембранните транспортни вещества
Има няколко начина за прехвърляне на вещества през мембраната:
1. Просто дифузия - Това е прехвърлянето на малки неутрални молекули към градиента на концентрация без разходи за енергия и носители. Най-лесно е простата дифузия през липидната мембрана на малки неполярни молекули, като 2, стероиди, хормони на щитовидната жлеза. Малки полярни незаредени молекули - СО2, NH3, Н20, етанол и карбамид - също дифузно с достатъчна скорост. Дифузията на глицерол е много по-бавна и глюкозата е практически неспособна да минава през мембраната. За всички заредени молекули, независимо от размера, липидната мембрана не е пропусклива.
2. Лека дифузия - прехвърляне на вещество към градиент на концентрация без разходи за енергия, но с носител. Характерни за водоразтворими вещества. Леката дифузия се различава от проста по-голяма скорост Прехвърляне и насищане. Разграничаване на две разновидности на лека дифузия:
Транспорт по специални канали, образувани в трансмемежните протеини (например катиолективни канали);
Използването на протеин-транслаци, които взаимодействат с специфичен лиганд, осигурете дифузията му чрез градиент на концентрация (Ping-pong) (трансфер на глюкоза към червени кръвни клетки, използвайки Glut-1 протеин).
Кинетичният трансфер на вещества от лека дифузия прилича на ензимна реакция. За транслоказа има консервация на лиганда, в която са заети всички протеинови свързващи центрове с лиганд, а протеините се управляват при максимална скорост. Следователно скоростта на превозното средство на улесния дифузия зависи не само от градиента на концентрациите на преносимото вещество, но и на броя на носителите на Beack в мембраната.
Проста и лека дифузия се отнася до пасивния транспорт, тъй като се случва без енергийни разходи.
3. Активен транспорт - транспортиране на вещество спрямо концентрационния градиент (незаредени частици) или електрохимичен градиент (за заредени частици), изискващи разходи за енергия, най-често АТР. Различават се два вида: Първичният активен транспорт използва енергията на ATP или Redox потенциала и се извършва с помощта на транспорт ATP-AZ. Най-често срещаната в плазмената мембрана на човешките клетки Na +, K + - ATP-AZA, СА 2 + -aza, N + -TF-Aza.
Със средно активен транспорт, градиентът на йоните, създаден на мембраната поради работата на основната система активен транспорт (абсорбция на глюкозни чревни клетки и реабсорбция от първичната уринова глюкоза и аминокиселините чрез бъбречни клетки, извършвани, когато Na + йоните се движат по градиента на концентрацията).
Прехвърляне през макромолекулната мембрана. Транспортните протеини се прехвърлят през клетъчната мембрана на полярни молекули с малък размер, но не могат да транспортират макромолекули, като протеини, нуклеинови киселини, полизахариди или отделни частици.
Механизми, с които клетките могат да абсорбират такива вещества или да ги отстрани от клетката, се различават от механизмите на транспортиране на йони и полярни съединения.
1. Ендоцитоза. Това прехвърляне на вещество от средата в клетка, заедно с част от плазмената мембрана. Чрез ендоцитоза (фагоцитоза) клетките могат да абсорбират големи частици, като вируси, бактерии или клетъчни фрагменти. Абсорбцията на течността и веществата, разтворени в нея, използвайки малки мехурчета, се нарича пиноцитоза.
2. Екоцитоза. Макромолекули, като кръвни плазмени протеини, пептидни хормони, храносмилателни ензими се синтезират в клетки и след това се секретират в междуклетъчното пространство или кръвта. Но мембраната не е пропусклива за такива макромолекули или комплекси, тяхната секреция се случва чрез екзоцитоза. Тялото има както регулируем, така и нерегулиран екзоцитозен път. Нерегулираната секреция се характеризира с непрекъснат синтез на секретираните протеини. Пример за това е синтезът и секрецията на колагенови фибробласти за образуването на междуклетъчна матрица.
За регулируема секреция са характерни съхранение на молекули, приготвени за транспортни мехурчета. С помощта на регулируема секреция се появява изборът на храносмилателни ензими, както и секрецията на хормони и невротрансмитери.
Глава 10. Енергиен обмен. Биологично окисление
Живите организми от гледна точка на термодинамиката са отворени системи. Енергията е възможна между системата и околната среда, която се среща в съответствие със законите на термодинамиката. Всяко органично съединение, влизащо в тялото, има определен резерв на енергия (д). Част от тази енергия може да се използва за използване на полезна работа. Такава енергия се нарича свободна енергия (G). Посоката на химичната реакция се определя от стойността на ГД. Ако тази стойност е отрицателна, реакцията протича спонтанно. Такива реакции се наричат \u200b\u200bупражнения. Ако DG е положителен, тогава реакцията ще продължи само когато свободната енергия е получена отвън - това са ендоргонални реакции. В биологични системи Термодинамично неблагоприятните енгорични реакции могат да се появят само поради енергията на упражнените реакции. Такива реакции се наричат \u200b\u200bенергиен конюгат.
Най-важната функция на много биологични мембрани е превръщането на една форма на енергия в друга. Мембраните с такива функции се наричат \u200b\u200bенергоспестяване. Всяка мембрана, изпълняваща енергийна функция, може да конвертира химическата енергия на окислени субстрати или АТР в електрическа енергия, а именно до трансмембранната разлика на електрическите потенциали (dy) или в енергията на разликата в концентрацията, съдържаща се в разделените мембранни разтвори и заместник \\ t Versa. Сред енергоспестяващите мембрани най-голямата стойностВъзможно е да се назове вътрешната мембранна митохондрия, външната цитоплазменова мембрана, мембраната на лизозомите и комплекса Golgi, саркоплазмен ретикулум. Външната мембрана митохондрия и ядрената мембрана не могат да превърнат една форма на енергия в друга.
Конвертирането на енергия в жива клетка е описано по следната обща схема:
Енергийни ресурси → ΔμI → работа
когато ΔμI е трансмембранната разлика на електрохимичните потенциали на Йон I. Следователно процесите на използване на енергията и Комисията поради нейната работа се оказват конюгат чрез образуването и използването на ΔμI. Затова този йон може да се нарече чистач йон. Главният йон на чифтосване в клетката EUKARYOT е Н + и, съответно, Δμ N + е основната конвертируема форма на енергия. Вторият по големина носач е Na + (ΔμNN +). Докато ca 2+, k + и cl - не се използват за извършване на работа.
Биологичното окисление е процес на дехидрогениране на субстрата, като се използват междинните носители на водород и неговия последен акцептор. Ако кислородът се появи в ролята на крайния акцептор, процесът се нарича аеробно окисление или дишане на тъкани, ако крайният акцептор не е представен от кислород - анаеробно окисление. Анаеробното окисление има ограничена стойност в човешкото тяло. Основната функция на биологичното окисление е осигуряването на енергийни клетки в достъпна форма.
Дишането на тъкани е процес на окисление на водород чрез кислород към водните ензими на тъканна дихателна верига. Тя тече съгласно следната схема:

Веществото се окислява, ако електроните и протоните (водородни атоми са едновременно) или се свързва с кислород. Способността на молекулата да дава електрони от друга молекула се определя от потенциала на Redox (Redox потенциал). Всяко съединение може да даде електрони само вещество с по-висок потенциал за окисление и намаляване. Окислението и редуциращият агент винаги образуват конюгатна двойка.
Изберете 2 вида окислени субстрати:
1. Сипиридин-зависим - алкохол или алдехид - изоцитрат, а-кетоглутарат, пируват, малат, глутамат, р-хидроксиацил-СОА, Р-хидроксибутират, - свръхзависимите дехидрогенази са включени в дехидрогенирането им.
2. В зависимост от флавин - са въглеводородни производни - сукцинат, ацил-СОА, глицерол-3-фосфат, холин - по време на дехидрогениране предава водород към FD-зависимата дехидрогеназа.
Схемата на дишане на тъкани е последователност от водородни протонни носители (Н +) и електрони от окислен субстрат за кислород, локализиран върху вътрешната мембрана митохондрии.

Фиг. 10.1. Схема за CTD.
Компоненти на CTD:
1. Презаредени дехидрогеназни дехидратирани субстрати, зависими от пиридин и ускоряване на 2ē и един h +.
2. Прищявка (FMN) зависими дехидрогенис ускоряват 2 водородни атома (2N + и 2ē). FMN зависима дехидрогеназа дехидратира само NADB, докато постепенното дехидрогеназа окислява оксизирането на оксидните субстрати, зависими от плоска.
3. Мастните разтворимият носител ubiquinon (коензим Q, Kaq) - плавно се движи през митохондриалната мембрана и ускорява два водородни атома и се превръща в Coqh2 (възстановена форма - убиквинол).
4. Система на цитохром - прехвърля само електрони. Цитохроми, съдържащи желязо протеини, от които се напомня протезната група, от която се напомня от скъпоценен камък. За разлика от хемката, железният атом в цитохром може да се премести от две към тривалентното състояние (Fe 3+ + ē → Fe 2+). Това осигурява участието на цитохром в електронния транспорт. Законът за цитохромас по ред на увеличаване на своя редуксен потенциал и в дихателната верига са разположени както следва: B-C1 -C-A-A3. Две последната работа във връзка като един цитохромаксидаза AA 3 ензим. Цитохромексидазата се състои от 6 субединици (2 - цитохром А и 4 - цитохром А 3). При цитохром А 3, в допълнение към желязото, има медни атоми и предава електрони директно към кислород. Кислородният атом се зарежда отрицателно и придобива способността да взаимодейства с протони с образуването на метаболитна вода.
Pranteins (FES) - съдържат незащитено желязо и участват в редокс процеси, които се срещат в един електронен механизъм и са свързани с флавопротеини и цитохром b.
Структурна организация на веригата от дишане
Компонентите на дихателната верига във вътрешната мембранна mihochondria формират комплекси:
1. I Комплекс (NADN-Kokh 2-Heductase) - отвежда електроните от митохондриалния NADP и ги транспортира до Kaq. Протоните се транспортират в интермамбранно пространство. Междинен акцептор и носител на протони и електрони са FMN и желязо и железни катерици. I Комплекс споделя потока на електрони и протони.
2. Комплекс - SUCCINAT - COQ - REDUDASE - Включва зависими от фад дехидрогенази и железни сухоземни протеини. Той транспортира електрони и протони от адахин-зависими субстрати за убиквинон, с образуването на междинна FADN 2.
Ubiquinon лесно се движи през мембраната и предава електрони в комплекса III.
3. Комплекс III - Kokh 2 - цитохром С - редуктаза - има в състава си цитохром В и С1, както и железни протеини. Функционирането на COQ с III комплекс води до отделяне на потока на протони и електрони: протоните от матрицата се изпомпват в интермебреновото пространство на митохондриите и електроните се транспортират по-нататък по CTD.
4. IV комплекс - цитохром А - цитохромен оксидаза - съдържа цитохромен оксидаза и транспортира електрони до кислород от междинния носител на цитохром С, който е подвижен компонент на веригата.
Има 2 разновидности на CTD:
1. В нея и водородните атоми са предадени за над-зависими дехидрогенизи.
2. Непълна (съкратена или намалена) CTD, в която водородните атоми се предават от постепенните зависими субстрати, заобикаляйки първия комплекс.
ATF оксидативно фосфорилиране
Окислително фосфорилиране е процес на образуване на АТР, конюгат с транспортирането на електрони в зависимост от дишането на тъканта от окислен субстрат за кислород. Електроните винаги се стремят да се преместват от електронални системи към електроелогични, така че транспортирането им на CTD е придружено от намаление на свободната енергия. В дихателната верига на всеки етап намаляването на свободната енергия възниква щандо. В този случай могат да се разграничат три области, при които прехвърлянето на електрони е придружено от относително голямо намаление на свободната енергия. Тези етапи са в състояние да осигурят енергия. синтез ATF.Тъй като количеството освободена свободна енергия е приблизително равно на енергията, необходима за синтеза на АТР от ADF и фосфат.
За да се обяснят механизмите на респираторното конюгиране и фосфорилиране, се поставя редица хипотези.
Механичен или конформационен (зелен котел).
В процеса на трансформация на протони и електрони, конформацията на протеините-ензимите се променя. Те отиват в ново, богато на енергийно конформационно състояние, а след това когато се връщат в първоначалната конформация, дават енергия на синтеза на АТР.
Хипотеза за химическо сдвояване (липман).
В конюгиране на дишане и фосфорилиране се включват "конюгат" вещества. Те ускоряват протоните и електроните и взаимодействат с H 3 PO 4. По време на връщането на протони и електрони фосфатната връзка става макроестерска и фосфатна група, предадена на ADP, за да образува АТР чрез субстратно фосфорилиране. Хипотезата е логична, но все още не е разпределена "конюгат" вещества.
Химосмотична хипотеза Петър Мичъл (1961)
Основните постулати на тази теория:
1. вътрешната мембранна митохондрия е непроницаема за йон N + и IT -;
2. Поради електронната транспортна енергия чрез I, III и IV протони на комплексите за дихателна верига се купуват от матрицата;
3. На мембраната се осъществява електрохимичен потенциал, е междинна форма на енергийно снабдяване;
4. Връщането на протони в матрицата на митохондриите през протонния канал ATP Synthase е енергиен доставчик за ATP синтез съгласно схемата
ADF + N3 RO 4 → ATP + N2
Доказателство за хемоосмотична теория:
1. На вътрешната мембрана има градиент Н + и може да бъде измерен;
2. Създаването на градиент Н + в митохондриите е придружен от синтез на АТР;
3. йонофори (сепаратори), унищожаване на протонния градиент, инхибира синтеза на АТР;
4. Инхибитори, които блокират протоните, транспортират по протечни канали на АТР синтаза, инхибират синтеза на ATP.
АТР-синтазната структура
АТР-синтаза - интегрален протеин на вътрешната мембрана митохондрия. Намира се в непосредствена близост до дихателната верига и е обозначена като комплекс V. АТР-синтазата се състои от 2 субединици, обозначени като F 0 и F 1. Хидрофобният комплекс F 0 е потопен във вътрешната мембрана митохондрия и се състои от няколко протера, образуващи канала, по който протоните се прехвърлят към матрицата. Субединица F 1 действа в митохондриалната матрица и се състои от 9 протера. Освен това три от тях се свързват с субединицата F 0 и F 1, образувайки един вид крак и са чувствителни към олигомицин.
Същността на химиооосмотичната теория: поради енергията на електронния трансфер чрез CTD, протоните се движат през вътрешната митохондриална мембрана в интермембранно пространство, където се създава електрохимичен потенциал (Δμ N +), който води до конформационна издатина на. \\ T Активен ATP-синтазен център, което води до възможно обратен транспорт на протони през протонните канали на АТР-синтаза. При връщането на протони, електрохимичният потенциал се трансформира в енергията на ATP макроергичната комуникация. Полученият АТФ с протеин на превозвач Translocase се премества в цитозолни клетки и в замяна на матрицата, ADP и FN arr.
Коефициентът на фосфорилиране (р / О) е броят на атомите на неорганичен фосфат, включени в ATP молекулите, по отношение на един атом, използван абсорбиран кислород.
Точки на фосфорилиране - зони в дихателната верига, където избирателната транспортна енергия се използва за генериране на протонния градиент, а след това в хода на фосфорилиране, под формата на ATP:
1. 1 точка - между пиридин-зависими и зависими от флавин дехидрогенази; 2 елемент - между цитохромас В и С1; 3 артикул - между цитохромас А и А3.
2. Следователно, когато окисляващи зависими субстрати, R / O коефициентът е 3, тъй като електроните от NADB се транспортират с участието на всички CTD комплекси. Окислението на постепенните зависими субстрати се появява около I комплекс I на дихателната верига и P / O е 2.
Нарушения на енергийния обмен
Всички живи клетки непрекъснато се нуждаят от ATP за прилагане на различни дейности. Нарушаването на всеки етап на метаболизма, което води до прекратяване на синтеза на АТФ, е катастрофално за клетката. Тъкани с високо енергийни нужди (ЦНС, миокарда, бъбреците, скелетните мускули и черния дроб) са най-уязвими. Щатите, в които синтезът на АТФ се намалява, за да комбинира термина "хипоенергетик". Причините за тези държави могат да бъдат разделени на две групи:
Алиментарен - гладно и хиповитаминоза B2 и RR - Налице е нарушение на доставянето на окислени субстрати в КТД или синтеза на коензимите.
Хипоксично - възниква в нарушаване на доставката или използването на кислород в клетката.
Регулиране на КТД.
Се извършва с помощта на респираторен контрол.
Респираторният контрол е регулирането на електронната скорост на трансфера чрез респираторна верига от ATP / ADP. Колкото по-малко това отношение, толкова по-интензивно се движи и АТТ е активно синтезиран. Ако ATP не се използва и концентрацията му в клетката се увеличава, потокът на електронния поток на кислород престане. Натрупването на ADP увеличава окисляването на субстратите и абсорбцията на кислород. Механизмът за контрол на дихателните пътища се характеризира с висока точност и е важен, тъй като в резултат на неговото действие процентът на синтеза на АТФ съответства на нуждите на клетката в енергия. АТР резервите в клетката не съществуват. Относителните концентрации на АТР / ADF в тъканите се променят в тесни граници, докато консумацията на енергия от клетката може да варира в десетки пъти.
Американският биохимик Д. Chans предложи да се разгледат 5 състояния на митохондрии, в които тяхната респираторна скорост е ограничена от някои фактори:
1. Недостатък SH 2 и ADP - скоростта на дишане е много ниска.
2. Недостатък SH 2 в присъствието на ADP - скоростта е ограничена.
3. Има SH 2 и ADF - дишането много активно (ограничено само от скоростта на транспортирането на йони през мембраната).
4. Липсата на ADP, ако има SH 2 - дишане се инхибира (състояние на дихателна контрола).
5. Липса на кислород, ако има SH 2 и ADP - състояние на анаеробиоза.
Митохондриите в клетка за почивка е в състояние на 4, при което скоростта на дишане се определя от количеството на ADP. По време на подсилена работа може да бъде в състояние 3 (възможностите на респираторната верига са изчерпани) или 5 (липса на кислород) - хипоксия.
CTD инхибиторите са лекарства, които блокират прехвърлянето на електрони от CTD. Те включват: барбитурати (абат), които блокират електроните, транспортиращи се през I комплекс от дихателната верига, антибиотичен антимицин блокира окисляването на цитохром В; Въглеродният оксид и цианидите инхибират цитохромоксидаза и блок електронния транспорт до кислород.
Инхибитори на окислително фосфорилиране (олигомицин) са вещества, които блокират транспортирането на Н + по протечния канал на АТР-синтаза.
Окислителни фосфорилиращи увреждания (йонофори) са вещества, които потискат оксидативното фосфорилиране, без да се засягат процеса на прехвърляне на електрони чрез CTD. Механизмът на действие на сепараторите се свежда до факта, че те са тъмни разтворими (липофилни) вещества и имат способността да свързват протони и да ги прехвърлят през вътрешната мембрана на митохондриите в матрицата, заобикаляйки протонния канал на АТР-синтаза. Освободената енергия се разсейва под формата на топлина.
Изкуствени увреждания - динитрофенол, витамин К производни (Dicumurol), някои антибиотици (валин олиномицин).
Естествените увреждания са продуктите на липидните пероксидации, мастни киселини с дълга верига, големи дози йод-съдържащи щитовидни хормони, термогенни протеини.
Терморегулаторната функция на тъканното дишане се основава на неподчинени и фосфорилиране. Митохондриите на кафява мастна тъкан произвеждат повече топлина, тъй като протеинът на термогенон присъства в тях отхвърля окисляването и фосфорията. Важно е за поддържане на телесната температура.
За разлика от разнообразието на макромир (светът на големите и видими за голото око на същества), светът на микробите се характеризира с относително монотонност. Понастоящем съществуват повече от 3000 различни вида бактерии, но външният му вид е разделен на 3 основни форми:
Символ или елипс (cocci) размери от 1 до 2 микрона (фиг. 1.3). Cockki принадлежат към най-лесната форма на бактерии; Те могат да се свързват помежду си, образуващи диплококи (две), Tetra-Kokki (четири) и стрептококи (вериги); - нарязани или цилиндрични размери от 1 до 5 микро (фиг. 1.4). Те също са способни да се присъединят помежду си в двойно върба верига и да дадат голямо разнообразие от форми на бактерии (Diplobacteria, Diplobacilla, Streptobacillia, Streptobacteria); - Извинения или спистри с размери от 1 до 30 микрона.
Микроорганизми Деструкторите. Водещата роля в трансформацията и минерализацията на органични ксенобиотици принадлежи към хеморготрофни (хетеротрофични) микроорганизми, особено бактерии, синтезират различни ензимни системи.
На бактериите, които нарушават органичните ксенобиотици, в честотата на възникване, броят на типовете (около 30) и спектърът на унищожените съединения е първото място заемат псевдомонади.
Биоразградската дейност на общността на микроорганизмите зависи от нейния състав, растеж и обмен между видовете хранителни вещества и генетичен материал. Достъпните метаболити могат да бъдат токсични за един компонент на Общността и могат да бъдат погълнати от други микроорганизми, които ускоряват в процеса на разлагане (явлението детоксикация).
Като се имат предвид начините за получаване на биологични обекти - деструктори на ксенобиотици, има два варианта на биохимика и биоредиаза. Първият вариант е за обекти със старо замърсяване, където дивата, аборигенната микрофлора почти винаги живее, способна да ги трансформира. Такова замърсяване може да бъде изтрито на място.(на място) без да се правят биопрепарати. В същото време биоразграждането е ограничено от фактори на околната среда и замърсяването, като съдържанието на кислород в средата, разтворимостта на замърсителното вещество и др. Вторият вариант е предварително получен чрез биологично активен щам, жизнеспособните клетки се натрупват които са приведени под формата на биопрепарация в замърсена среда. Тази опция е препоръчително да се прилага в северните региони и при обработката на места с незавършено замърсяване;
Способността на микроорганизмите да унищожи ксенобиотичната или друга замърсител зависи от присъствието на гени в клетки, които определят синтеза на ензимите, участващи в разграждането на съединението. Дизайнът на рекомбинантните щамове - деструкторите на ксенобиотици е да се комбинират няколко гена или техните блокове, отговорни за първичния метаболизъм на съединенията. Предимството на такава асоциация е генетично модифицираните микроорганизми (GMMOS), могат да синтезират различни ензимни системи, което дава възможност за ефективно и бързо да се унищожи широк спектър от химическо замърсяване.
Биологично пречистване на отпадъчни води. Концепции на схеми за пречистване на отпадъчни води. Основни принципи на работа, методи и структури на аеробни и анаеробни биологични отпадъчни води и преработка на промишлени отпадъци.
Класификация на биологичните методи за почистване. Биологични методи Пречистването се използва за пречистване на домакинствата и промишлените отпадъчни води (фиг.2.1) от много разтворени органични и някои неорганични вещества (водороден сулфид, сулфиди, амоняк, нитрати и др.). Процесът на почистване се основава на способността на микроорганизмите да използват тези вещества за хранене. Контакт с органични вещества на микроорганизмите частично унищожават, превръщайки се във вода, въглехидратен диоксид, нитрит, сулфации и др. Органични вещества за микроорганизми са източник на въглерод. Унищожаването на органични вещества с микроорганизми се нарича биохимично окисление.
Анаеробните микробиологични процеси се извършват с минерализация на разтворените органични вещества и твърди фази на отпадъчни води. Анаеробните процеси текат в бавни темпове на движение, отиват без достъп на кислород, се използват главно до ревностно утаяване. Аеробният метод за почистване се основава на използването на аеробни групи микроорганизми, за жизнената активност, от която са необходими постоянен приток на кислород и температура от 20-40 ° С.
Наличността на всяко биологично окисление може да бъде оценено чрез стойността на биохимичния индикатор, при който съотношението на стойностите на пълния BOD (BOD е пълно) и CODs. Биохимичният индикатор е параметърът, необходим за изчисляването и експлоатацията на промишлени биологични структури за пречистване на отпадъчни води. С голяма степен на биохимичния индикатор, равен на или повече от 0.5, вещества са биохимично окисление. Мащабът на биохимичния индикатор варира значително за различни канализационни групи. Индустриалните отпадъчни води имат нисък индикатор (0.05 - 0.3), битови отпадъчни води - над 0.5.
Изграждане на биологично пречистване на отпадъчни води. Основните структури на биохимичното почистване са аеротейни и вторични шахти.
Аеротенк е апарат с постоянно течащи отпадъчни води, в по-дебелия аеробни микроорганизми, които консумират субстрат, се развиват, т.е. "Замърсяване" на тези отпадъчни води. Биологично третиране на отпадъчни води в аеротанките се осъществява в резултат на жизнената активност на микроорганизмите на активните бала. Отпадъчните води непрекъснато се смесват и насочват към насищане на въздушния кислород. Active IL е суспензия на микроорганизми, способни на флокулация.
Има и класификация на аеротаните в мащаба на "натоварването" на активна IL: високо натоварени (аеротанки за непълно почистване), конвенционални и ниско натоварени (аеродини на удължена аерация). Системата за аеризация има голямо значение в изграждането на аеротанки. Системите за аерация са предназначени да снабдяват и разпространяват кислород или въздух в аеротана, както и поддържане на активни рали в суспензията.
Аеротейни миксери (Аеротени с пълно смесване, Фиг. 2, Мартиза) се характеризират с равномерна храна в дължината на конструкцията на източника на вода и активната йла и равномерното докосване на силозната смес. Пълната смес от отпадъчни води в тях с сместа от утайки осигурява подравняването на концентрациите на утайката и скоростите на биохимичния процес на окисление, така че аерографските смесители са по-адаптирани за почистване на концентрираните производствени отпадъчни води (BPK пълен до 1000 mg / л) с остри колебания в тяхното потребление, състав и количество замърсяване.,
Аеротейни-безарти. За разлика от аеротените на други типове (аеротеланови смеси и аеротани на междинния тип), аеротеле-осцилати (фиг. 2, брошури) са структури, при които пречистените отпадъчни води постепенно се движат от мястото на входа до неговото разположение. В този случай практически няма активно смесване на входящите отпадъчни води с получените по-рано. Процесите, които се срещат в тези съоръжения, се характеризират с променлива скорост на реакцията, тъй като концентрацията на органично замърсяване намалява по движението на водата. Аеротенк-осцилатите са много чувствителни към промяна на концентрацията на органични вещества в входящата вода, особено за Volleal приходи с токсични вещества за отпадъчни води, поради което тези структури се препоръчват да се използват за почистване на градските и близките в състава на домакинските промишлени отпадъчни води.
Аеротенци с разпръснати входа (Фиг.2, разпределител) на отпадъчни води заемат междинно положение между миксери и дисплеи; Те се използват за пречистване на смеси от промишлени и градски отпадъчни води.
Аеротените могат да бъдат комбинирани с отделни вторични шахти или да се комбинират в блока, когато правоъгълна форма. И двете структури по отношение на. Най-компактните комбинирани съоръжения са аеротан-шахта. В чужбина този вид конструкция е кръг от гледна точка на формата с механични аератори са получили името на аерозакса. Редуването на аеротан с картер ви позволява да увеличите рециклирането на силозната смес без използването на специални помпени станции, да подобрите режима на кислород в картера и да увеличите дозата на утайка до 3-5 g / l, съответно нарастваща окислителната сила на структурата.
Сорт aerotenka-Sump. - Aero-selection е кръгло строителство. Изяснените отпадъчни води се вливат в долната част на зоната на аерация, която въздухът се подава към пневматичния или пневмомеханичен метод, който осигурява процеса на биохимично окисление и също така създава движение на циркулацията на течността в тази зона и утайката на иконата смес от циркулиращата зона на картера. От зоната на аерацията, сместа чрез наводнени регулируеми преливни прозорци влиза в сепаратора на въздуха и след това към зоната на циркулация на картера. Значителна част от силозната смес през процепа се връща в зоната на аерацията и разпределените пречистени отпадъчни води през слой от претеглена утайка се въвежда в съблазната зона.
Вторични шахти . \\ t част от Биологичните пречиствателни съоръжения са разположени в технологичната схема веднага след биоокислите и служат за отделяне на активните винали от биологично пречистена вода, излизащи от аеротани, или за пустинята биологичен филм, идващ с вода от биофилтри. Ефективността на работата на вторични септични ями определя крайния ефект от пречистването на водата от суспендираните вещества. За технологични схеми на биологично третиране на отпадъчни води в аеротани, вторичните септични ями също са определени до известна степен обема на въздушните структури, в зависимост от концентрацията на точката на връщане и степента на рециклиране, способността на уреждането да се отдели ефективно силно концентрирани смеси от утайки.
Сместа Ilovaya, идваща от аеротаните в вторични септични ями, е хетерогенна (мултифазната) система, в която дисперсионната среда обслужва биологично пречистени отпадъчни води, а основният компонент на диспергираната фаза е памукът на активната суспензия, образувана под формата на комплекс Тристепенна клетъчна структура, заобиколена от екзосулиране на веществото на биополимерния състав.
Анаеробното пречистване се използва за отстраняване на замърсителите на отпадъчни води, като първи етап от пречистване на отпадъчни води с висока концентрация на органично замърсяване (N\u003e 4-5 g / l), както и за обработка на активни бала, други валежи и твърди отпадъци. Много твърди отпадъци съдържат целулоза, по-лека от анаеробното разлагане с образуването на биогаз, отколкото аеробно окисление.
В хода на генерирането на метаногенеза (метаногенеза) - анаеробният процес с образуването на метан - органични замърсители се превръща в биогаз, съдържащ главно СН 4 и С02. Може да се използва като гориво. Размерът на изолирания биогаз е достатъчен не само за компенсиране на енергийните разходи за анаеробно разлагане, но и за използване от потребители на трети страни - в котли или нагреватели за производство на пара и топла вода, в стационарни газови генератори за получаване на електричество с топлинна енергия Възстановяване, в процеса на топлинни седалки и изгаряне на валежи и д-р
Биоценози и био химически процеси с анаеробно почистване. Формирането на цено. Анаеробни биоценози при почистването на отпадъчни води могат да бъдат флукули, биофилми и гранули. Те се развиват в екосистеми с господство на аноксигенни и анаеробни състояния, при които ферментационните процеси, аноксигенно окисление (анаеробно дишане) и поток на метано.
Аноксигенното окисление на органични субстрати включва процеси на деактитизиране и сулфатеризирани поколения, които се появяват в присъствието на йони N03, N02 -, S0 4 2- и като правило, при липса на кислород. Тези процеси се използват за отстраняване на азотни и серни съединения от отпадъчни води.
Основният процес, който се среща в анаеробни условия и се използва за разлагане и отстраняване на органичното замърсяване и отпадъците - метаногенеза. В процеса на генериране на металиране (често наричан "метан ферментация"), органични субстрати и замърсяване, дезинфекция и детоксикация на отпадъчни води. В природата този процес продължава в различни среди с анаеробни условия, в каучук от преживни животни, в Frachers.
Methange Generation е сложен, многостъпен процес, в който първоначалното органични вещества Последователно се превръща в по-прост с прехода на значителна част от въглерода в метан и въглероден диоксид и в течността на утайката. Разлагането на метан включва три етапа на анаеробната ферментация (Фиг. 5.1): хидролиза, кисела (ацидогенна), ацетогенна и четвърта, етап от ъгъл на метан (етап на образуване на газ).
В първия етап на ферментация, микроорганизми - хидролитици, притежаващи целулолитни, протеолитични, амилолитни, липолитни, амониеви дейности, участват. Нитратите и сулфатите, съдържащи се в средата, се възстановяват от бактериалните денитрицери и сулфатериектопродуци. В резултат на ензимна хидролиза на целулоза и хемицелулоза, протеини, мазнини и други компоненти се хидролизират за образуване на мастни киселини, глицерин, пептиди, аминокиселини, моно- и дискусии и в малки количества оцетна киселина, метанол, амоняк, водород. PP бактериите участват в хидролиза. Clostridium, Bacillus, както и бактерии, бутиривибио, мобилобактерия, EBAXACAXIUM, BIFIDOBAXACTIUM, LACTOBACALLUS, SELENOMONAS. На ациогенен етап, различни ферментационни триони поток: алкохол, мазна киселина, ацетон-бутил, пропионови, и други, по време на които бактерии-ацидогени ферментират получените хидролиза, като глюкоза, към органични киселини:
Консумиране на моно и олигозахариди, аминокиселини и други междинни продукти от хидролиза, тези бактерии предотвратяват инхибитора на хидролизата на хидролитични ензими, участващи в първата фаза на ферментация.
В резултат на разделяне на първите два етапа, 70-80% от образуваните органични продукти съставляват по-високи мастни киселини, до 20% - ацетат и 3-5% - водород. Сред другите продукти са изомаслянски, фенилоксис, бензоена, индолилбензоена киселина, NH4 +, Н, S, бутанол, пропанол, С02 и др.
При ацетогенния етап на ферментация, хетероацетогенни бактерии (Acethegens) pp. Clostridium, Syntrophus и други превод на органични киселини, като пропионично и масло, други продукти на ациогенеза в оцетна киселина:

Основната роля в разлагането на метан се играе от последния етап, извършен от строги анаероби - с метановидни бактерии. Те са по-чувствителни към условията на околната среда. Времето на генериране на метаногенни клетки е няколко дни. Тяхната активност е максимална при рН на средата от 6.8 до 7.5. На по-нисък и високи стойности РН развитието на метаноген се забавя или изключва изобщо.
Продукт на реакции на метаногенен етап - СН4. Неговото образование е възможно по два начина. Метаногенни бактерии-литотрофи (стр. Метанокок, метанобактерия, метаноспирилум, метаномикробий, метаногений, метанотермус, метанобревибакер) се консумират като субстрат Н2 и С02, както и СО и се образуват:
C0 2 + 4N 2 → CH4 + 2N 2 0
4Noxone → CH 4 + Z0 2 + 2N, 0
4CO + 2N 2 0 → CH4 + Z0 2
Ацетотрофични микроорганизми (стр. Метаносарцина, мелханозаета, метаноплав) Използвайте ацетат, метанол, метиламин:
CH 3 Soam → CH 4 + CO 2
4cn 3 Oh → Zos 4 + C0 2 + 2N 2 0
4ч 3 NH2 + 2N 2 0 → ZOS 4 + 4NH 3 + сътрудничество
Благодарение на унищожаването на органични киселини, средата на средата се увеличава, реакцията на средата става коприна, така че метаногенен етап понякога се нарича "алкална ферментация".
При разлагане на оцетна киселина се образуват 70-75% метан, а останалите 25-30% в резултат на синтез на въглероден диоксид и водород и поток от други реакции. Съотношението на крайните продукти в процеса на ферментация на метан зависи от състава на средата, условията на ферментация и съдържанието на микрофлора.
Голям стимул за развитието на много от съвременните методи на анаеробно почистване беше откриване в средата на 70-те години. Способността на микроорганизмите, включени в метаногенната общност за образуване на агрегати - гранули (пелети) с растеж в анаеробнен реактор при увеличаващите се условия на потока (Фиг. 5.2 Машини).
Methanosaeta Concilii (Methanothrix Soehngenii), както и метаносарцина SPP, се извършва специална роля в образуването и функционирането на гранулите. Бактерии p. Метанозаета образуват безчеткови и платнени структури (Фиг. 5.3), в която се групират метаносарсина бактерии микроколота (фиг. 5.4). Благодарение на това, агрегатите се образуват под формата на плътно лесно уреждане на гранули с размер от 1-5 mm.
Конструкциите на традиционните структури включват септември, агенти, презареждащи се, реактори за контакт, анаеробни лагуни, метиенки, анаеробни биофилници с възходящ поток на флуида (виж картера, фиг. 3.5).
Септилетът (септична яма) е устройство, състоящо се от две части: септична и септична (фиг. 6.1). В първата част има изясняване на водата поради движението му при ниска скорост, а във втората част, разположена под първата, е претоварването на седимента по време на съхранението си за 6-12 месеца. Септичните и септични части на Септика не са разделени един от друг. Продължителността на мястото на водата в септите е 3-4 дни. Септиките се използват, ако количеството отпадъчни води не надвишава 25 m 3 / ден.
Септицизалите често се използват за ферментация на активната рали от вторични сезон, утаяване на първични сезон и пени, за да се натрупат утайка, намаляване на обема му, зло мирис и броя на патогенната микрофлора. Септиките са най-често срещаните лечебни заведения за отделните домакинства, защото те могат да работят самостоятелно и да не трябва да бъдат изключени.
Реффекти за непреодолимост, които могат да се считат за вид на пречистване, се използват при пречиствателни станции за отпадъчни води с честотна лента до 30 000 m 5 / ден. На фиг. .2 показва дизайна на изчисления - претоварване, направен под формата на комбинирана структура, състояща се от прелификатор, концентрично разположен вътре в претоварването.
Анаеробният метод за почистване в реактора за контакт е един от първите, широко използвани в индустрията от 1930-те години. По-специално, за обработка на източници захар, алкохол и дрожди. В сравнение с нуждите, реакторът за контакт е много по-продуктивен, тъй като осигурява среда за смесване с анаеробна IL и по-висока концентрация на алеята се поддържа поради връщането на него от вторичния картер (виж специалния материал на лекция3, \\ t Фиг. 3.5), т.е. обаче, се прилага в аеротана с вторичен картер. За да се увеличи ефективността на разделянето, течността на МОТ преди вторичното утаяване може допълнително да дегазира (в отделен контейнер) или охлаждане. В случай на дегазиране газът се отстранява чрез механичен (хидравличен) метод или действие на вакуум. Охлаждането води до забавяне на процесите на образуване на метан и в резултат на това образуването на нови мехурчета, което подобрява седиментационните свойства на анаеробната RAL.
Традиционните и най-често срещани устройства за анаеробното разлагане са methyenks. Те се използват за ферментиране на отпадъчни води с висока концентрация на замърсяване и разлагане на органични отпадъци, по-специално активни бала на съоръженията за пречистване на отпадъчни води.
Methentenki работи с отопление, като правило, в периодичния начин на натоварване на отпадъци или отпадъчни води, с постоянна селекция от биогаз и разтоварване на твърда утайка, тъй като процесът е завършен. Изработени са от стомана, бетон, пластмаси, тухли; Те се различават в резервоара, броя на ферментационните камери, метода на натоварване, разтоварване на субстрата, методи за нагряване и смесване.
Големите обем метаненец са направени под формата на вертикални цилиндрични или елипсоидни резервоари с принудително смесване на отвъд масата, те са предназначени за свръхнатискане на налягането на газ до 5 kPa. Малките биогазови инсталации могат да бъдат цилиндрични хоризонтални или вертикални биореактори с механично разбъркване, частично или напълно замъглено в земята, за да се намали загубата на топлина. Дизайнът на биореакторите трябва да осигури възможност за пълно изпразване на резервоара, така че дъното често се извършва скосено, полусферично или под формата на конус.
Mixtenki с фиксирано дефицитно припокриване има недостатък, характеристика на твърди етажи - непостоянството на налягането в реактора. При разтоварване на седимента вътре в метиенка може да се образува вакуум и при натоварване увеличава налягането. Това води до унищожаване на структури, образуването на пукнатини.
Предимства на плаващ припокриващ се метиенка: 1) експлозивна безопасност, тъй като независимо от пълнежа на метиенка в нея се поддържа положително налягане на газ, което елиминира възможния въздушен проникване в конструкцията; 2) на позицията на плаващото припокриване, можете да извършите дозиране на товарене и разтоварване; 3) улеснява борбата срещу образуването на кора.
Ролята на смесването и температурния режим В Метапетите. Мутанти от всички видове могат да работят в мезофил (20-45 ° С, обикновено 30-35 ° С) и термофилни (50-60 ° C) температурни режими. Режимът на избор се избира, като се вземат предвид методите за последваща обработка и обезвреждане на валежите, както и санитарните изисквания. Мезофилен режим се използва от чаша, тъй като е по-малко енергоемка и по-икономически полезна, позволявайки съществуването на по-голям брой видове микроорганизми и следователно е по-стабилен, по-малко чувствителен към промените в условията на околната среда; Утайките в този режим след обработката се дехидратират по-добре в сравнение с термофилния процес. Въпреки това, с термофилен режим, скоростта на разпадане на органични съединения е по-висока (около 2 пъти) и над степента на техния колапс се постига почти пълна деглиране на утаяването, което е важно, ако утаяването се използва като рекултивиране или торове за. \\ T почва. Продължителност на ферментацията с мезофилен режим 20-30 дни, с термофилен - около 10 дни. Газова калорична стойност с термофилна ферментация от 5% по-ниска, отколкото при мезофил.
За по-пълен процес на генериране на метанди е необходимо да се смеси напълно съдържанието на метиенка, за да се осигури равномерно разпределение на съдържанието на реактора, необходимите условия за маса и топлообмен, минимизиране на залепването, образуването на пяна и. \\ T Обелете, образуването на дънната утайка, отстранете газовете. За разбъркване, механични бъркалки, циркулационни помпи, хидроенергийни асансьори или комбинация от тези системи се използват в METTENCA.
Оптимална концентрация на суспендирани вещества В метананата, в която се наблюдава висока интензивност на метанообразуването, е в интервала от 2-10%. При концентрацията на твърди частици над 10-12% смесването на средата е затруднено и това води до намаляване на емисиите на газ. В такива случаи се използват специални проекти на биореактори, осигуряващи необходимото ниво на смесване.
Метанизацията тече при максимална скорост при рН от 6 до 8. С намаляване на рН под 5.5 (в случая на "zaksania" methyenka), активността на метаногенните бактерии се прекратява. Като правило рН не регулира поради високата буферна способност на средата. Но когато средата е подкислена, разтворът NaHC03 е най-доброто неутрализиращо средство.
Процесът на метаногенеза се забавя в присъствието на различни детергенти (при тяхната концентрация от около 15 mg / l), антибиотици и други вещества. От анионни повърхностно активни вещества сравнително падат и слабо забавят процеса на ферментация на алкилсулфати, хлорен сулфанол; Трудно е да се разпадне и забави ферментацията на сулфанола.
Анаеробните реактори са устойчиви на дълги прекъсвания при доставката на отпадъчни води, промени химичен състав Входящите канали, които позволяват ефективно да ги използват за почистване на отпадъчните води на сезонното производство, както и в режимите на малки натоварвания. В случай на намаляване на метаногенната активност, е възможно да се намали скоростта на подаване на субстрат за неговото намаляване, да се учат средата с химикали, разреждайте канализацията с вода, отстранете токсичните съединения чрез преработка на отпадъчни води.
Бактериално извличане. химически елементи от руда, концентрати и планински породи, обогатяване на руди, биосорбция на метали от решения. Отстраняване на сяра масло и въглища. Повдигане на възстановяването на петрола. Отстраняване на метан от въглищни слоеве. Потискане на биокореозията на петролните продукти.
Проучвания за бактериално окисление на желязо и излугване на метали, започнати след подбора през 50-те години на двадесети век от дренажната кисела вода на въглищната мина на микроорганизмите, способни да участват в окислението на двувалентното желязо до тривалентните - киселинни бактерии за фероксидан (преди това наречени Thiobaccilus ferrooxidans). Бактериите, участващи в излужването на металите, вида на храненето се отнасят до хемоавотрофично, за да се получи енергийна катализа на реакции на химически окислителни реакции и асимилиране на въглероден диоксид за проектиране на клетки, т.е. Хранене самостоятелно, без използване на органични вещества.
Дебел велосипед сулфид руда.
В последните години За да се приготвят упорити суровини до цианиране, започна да се използва парен бактериално извличане на концентрати или руди. Повече от дузина промишлени предприятия, които практикуват тази технология, вече действат в света, но капиталовите разходи за такава технология са много високи, така че за малките и средните полета не са оправдани.
Използването на строго ацидофилни бактерии предполага, че рН на пулпата или разтвора 2 и по-долу. Ако се използват бактерии от ферооксидани за излугване, процесът на биологично окисление на минералите може да отиде по два начина: тези бактерии не са само окислени от серни съединения, но също така могат да получат енергия за окисляване на оксидните форми на желязо до оксид. Времето за лечение зависи от състава на сулфидната руда, формата и разпределението на метал в рудата и количеството, налично за микроорганизми за сяра. Има и редица по-тесни проблеми, например, токсичността на високите концентрации на получените тежки ценни метали за някои видове или щамове на микроорганизми.
Така един от подходите за подобряване и развитие на технологии и методи за преиздаване е изборът на бактерии и арки, устойчиви на токсичността на металите. Други критерии за подбор на култури са: простотата на работа с тях в промишлени условия, активност в окисляването на минерални съединения, отношението към рН, температурата, аералния режим и способността за стимулиране на тяхната активност чрез допълнителни вещества.
Понастоящем е редица раждане (групи, разделени от свойства и систематично положение) на бактерии и архиви (два микроорганизми на телевизора), чиито представители са способни да излушават метали чрез сулфид окисление са: ацидиобацилус, халотиобацил, тиобацилус, лептоспирил, киселиферий, сулфобацил, фероплазма , Сулфлубус, металосхаера и киселианец. По този начин развитието на биовахинговите технологии може да се основава на двете промени в организацията на процеса (оптимизиране на аерацията, температурния режим, предварителна обработка на минерални суровини и др.) И при избора на нови микробни култури - с по-висока активност или по-лесно от биомасата, или с по-широк спектър на рН, температура и др. Традиционното излугване с киселинни решения доведе до факта, че търсенето на нови култури на микроорганизми се фокусира именно върху ацидофилни и свръхцидофилни организми.
^ 20.Хоихимични основи на качество на силата и пътя на неговото развитие
Под силата на мускулите обикновено се разбира като способност за преодоляване на външната резистентност или да го противодейства чрез мускулни напрежения.
Качествата на скоростта са зависими главно от енергийното снабдяване на работните мускули и от техните структурни морфологични характеристики, до голяма степен предопределени генетично.
Проявът на сила и скорост е характерно за физическото натоварване, извършено в зоната на максимална и субмаксимална мощност. Следователно, в енергийното снабдяване с високоскоростни качества, анаеробанските пътища на резинкция ATP - креатин фосфат и гликолит са предимно.
Жилищният ATF се разгръща по-бързо поради реакция на креатин фосфат. Той достига максимум след 1-2 секунди след началото на работата. Максималната мощност на този метод на образуване на АТФ надвишава скоростта на гликолитни и аеробни пътища на ATF синтеза съответно 1,5 и 3 пъти. То е за сметка на креатин фосфатния път на Resintez ATP мускулни натоварвания се извършват с най-голямата сила и скорост. На свой ред, величината на максималната скорост на реакцията на креатин фосфат зависи от съдържанието на креатин фосфат в мускулните клетки и активността на креатиновия ензим. Увеличете креатин фосфатните запаси и създаването на креатинско колоездене е възможно чрез използването на упражнения, което води до бързо изтощение в креатин фосфат мускулите.
За тази цел се използват краткосрочни упражнения, извършвани с най-голяма сила. Добрият ефект дава използването на метод за обучение на интервал, състоящ се от поредица от такива упражнения. Спортистът се предлага серия от 4-5 упражнения за максималната мощност с продължителност 8-10 s. Останалите между упражненията във всяка серия е 20-30 s. Продължителността на почивка между серията е 5-6 минути.
Работата на високоскоростните и мощните натоварвания в зоната за подмяна се осигурява от енергията главно поради гликолитния ресинтрат АТР. Възможностите на този метод за получаване на АТР се дължат на интрамускулни резерви за гликоген, активността на ензимите, участващи в този процес, и тялото резистентност към млечна киселина, генерирана от гликоген. Следователно, за развитието на високоскоростните способности, основани на гликолитни енергийни доставки, се прилага обучение, които отговарят на следните изисквания. Първо, обучението трябва да доведе до рязко намаляване на съдържанието на гликоген в мускулите, последвано от нейната супермаленции. Второ, по време на тренировка в мускулите и в кръвта, млечната киселина трябва да се натрупва за последващото развитие на устойчивостта на организма.
Различните пропуски между отделните упражнения и между серията за упражнения са очевидно недостатъчни за възстановяване на запасите от гликоген и в резултат на това по време на обучение в мускулите има постепенно намаляване на съдържанието на гликоген към много ниски стойности, което е предпоставка за появата на изразена суперскомпенсация.
Структурните морфологични особености на мускулите, които определят възможността за проявление на якост и скорост, са свързани със структурата на отделни мускулни влакна и мускулите като цяло. Мощните качества на отделните мускулни влакна зависят от броя на контрактивните елементи - миофибрилс - и за развитието на саркоплазмената мрежа, съдържаща калциеви йони. Саркоплазмената мрежа също участва в поведението на нервен импулс в мускулната клетка. Съдържанието на миофибрилите и развитието на саркоплазмената мрежа не е същото в мускулните влакна на различни видове. В зависимост от преобладаването на определени методи за образуване на АТР, химическият състав и микроскопската структура се различават три основни вида мускулни влакна: тоник, фасик и преход. Тези видове влакна също се различават по тяхната възбудимост, време, скорост и сила на намаляване, продължителност на експлоатацията.
Тонизираните влакна съдържат относително голямо количество митохондрии, има много миоглобин в тях, но малко контрактивни елементи са миофибрилс. Основният механизъм на ATP Resintez в такива мускулни влакна е аеробна. Следователно те се намаляват бавно, развиват малка сила, но могат да бъдат намалени за дълго време.
Fazic влакна имат много миофибрили, добре развита саркоплазменова мрежа, много нервни окончания са подходящи за тях. Колагенните влакна са добре развити в тях, което допринася за бързото им релаксация. В тяхната саркоплазма, концентрациите на креатин фосфат и гликоген са значителни, креатинната активност на креатините и ензимите на гликолизата е висока. Относителното количество митохондрии в белите влакна е значително по-малко, съдържанието на миоглобин е ниско в тях, така че те имат бледо цвят. Осигуряването на енергията на белите мускулни влакна се извършва поради реакцията на креатин фосфат и гликолиза. Комбинацията от анаеробни пътеки на Resintez на ATF с голямо количество миофибрил позволява на влакната от този тип за развитие на висока скорост и намаляване на редукцията. Въпреки това, поради бързото изчерпване на запасите от креатинефсхати и гликоген, времето за работа на тези влакна е ограничено.
Преходните мускулни влакна в тяхната структура и свойства заемат междинно положение между тоник и фасичното.
Дори и от такъв кратък списък на разликите между видовете мускулни влакна, следва, че белите влакна и преходните влакна, близки до тях, са по-предпочитани за проявяването на сила и скорост. Ето защо, по-изразени качества на скоростта, с други подобни неща, имат тези мускули, в които съотношението между мускулните влакна се измества към бяло.
Съотношението между влакната на различните видове в скелетните мускули е неравномерно. Така че, мускулите на предмишницата, двуглавата ръка на рамото, мускулите на главата и другите съдържат предимно физически влакна. Мускулите на торса, прав мускул на корема, прав мускул на бедрото основно съдържат тонични влакна. Оттук е лесно да се разбере защо тези мускулни групи се различават значително в такива свойства като възбудимост, скорост, сила, издръжливост.
Връзката между различните видове мускулни клетки във всеки човек е генетично предварително определена. Въпреки това, използвайки физическо натоварване на даден характер, е възможно целенасочено да се предизвика спектърът на мускулните влакна. Поради приложението упражнения за власт Този спектър се появява в посока на преобладаване на бели влакна, имащи по-голям диаметър в сравнение с червено и преходно, което в крайна сметка води до хипертрофия на обучени мускули. Основната причина за хипертрофията в този случай е да се увеличи съдържанието в мускулните клетки на контрактилни елементи - миофибрили. Следователно, мускулната хипертрофия, причинена от захранващите товари, принадлежи към миофибриларния тип.
Физическо натоварване, използвано за развитие на мускулната хипертрофия на миофибриларния тип, на биохимичното ниво трябва да увреди миофибрилите с последващата им суперкомпенсация. За тази цел различни упражнения с тежест.
За развитието на силата често се използва методът на повторни упражнения с напрежение от 80-90% от максималната якост. Най-ефективната тежест е 85% от максималната мощност. В този случай броят на повторенията "на неуспех" обикновено е 7-8. Всяко упражнение се извършва от поредицата, чийто броя на която обхваща от 5 до 10, с временен интервал между тях след няколко минути. Скоростта на упражненията се определя от целта на обучението. За преобладаващото увеличение на мускулните масови упражнения се извършват в бавен или умерен темп. За едновременното развитие на силата и скоростта упражненията се извършват в експлозивен режим: началната фаза на движението се извършва при висока скорост и е завършена възможно най-гладко. Ето защо, в типовете на скоростта на спортистите през периода на сила, те трябва да откажат бавно да изпълняват упражненията на властта, тъй като в този случай способността на мускулите към бързото намаляване се губи.
Времето за възстановяване след обучението на скоростта е 2-3 дни. Въпреки това, променящите се мускулни групи, към които са насочени товар, класовете за обучение могат да се извършват чрез по-малки интервали на отдих.
Задължително условие за ефективно обучение на властта е пълноправно, богато на протеиново хранене, тъй като миофибрилите се състоят изключително от протеини. Има доказателства, че развитието на мускулната хипертрофия насърчава ултравиолетовото облъчване. Предполага се, че под влиянието на ултравиолето образуването на сексуални хормони на мъжете, стимулиране на синтеза на протеини в тялото.
21 Биохимични основи на скоростта (скорост) като качество на двигателя
Скоростта като качеството на двигателя е способността на дадено лице да извърши двигател в минимално време за тези условия с определена честота и импулсивност. От естеството на това качество сред специалистите няма единство на мненията. Някои изразяват идеята, че физиологичната основа на скоростта е лесимостта на невромускулния апарат. Други смятат, че мобилността на нервните процеси играе важна роля в проявяването на скоростта. Многобройни проучвания са доказани, че скоростта е сложно качество на двигателя на човек.
Основните форми на проявление на човешка скорост са времето на реакцията на двигателя, времето за максимално бързо извършване на едно движение, времето на извършване на движението с максималната честота, времето на извършване на холистичен двигател. Друга форма на проявление на скоростта ("високоскоростни качества") - бързото начало на движението (фактът, че в спортната практика се нарича "острота"). Скоростта на холистичните актове на двигателя (бягане, плуване и др.) Е почти най-важното, а не елементарните форми на проявяване на скоростта, въпреки че скоростта на холистичното движение само косвено характеризира скоростта на човек.
Скелетният мускул е сложна система, за да бъде химическа енергия в механична работа и топлина. Основните компоненти на мускулести фибри са протеини: актин и miosin.
При извършване на бързи движения за намаляване на мускулите се изисква голямо количество енергия за единица време с недостиг на кислород, поради което основната роля се играе от анаеробните процеси на АТР хидролиза.
Хидролизата на АТР в центъра на атетри на миозичната глава е промяна в конформацията на последната и я прехвърля в ново, високоенергийно състояние. Повторното прикрепване на главата на Мозайката към новия център на актинската спирала отново води до въртене на главата, което се осигурява от енергия в нея. Във всеки цикъл на съединението и молекулата на главата на миозин с актин, една АТР молекула за всеки мост е разделена. Скоростта на въртене се определя от разделянето на АТР. Очевидно е, че бързият фасик в консумация значително повече АТР на единица време и запазва по-малко химическа енергия по време на тонизирано натоварване от бавните влакна. Така, в процеса на хемомеханична трансформация на АТР, тя осигурява изключването на главата на миозин и актин филахиламент и енергия за по-нататъшно взаимодействие на главата на миозин с друга област на актинската нишка. Тези реакции са възможни при концентрации на калций над 106 mol / l.
Нивото на развитие на скоростта, в крайна сметка, определя успеха в огромното мнозинство от спорта. Дори маратоникът трябва, може би бързо да управлява дистанцията си, като същевременно поддържа висока скорост "Cruising" (под "круизиращата" скорост предполага средната скорост на преминаване на разстояние). И успехът на тежестта зависи от това как скоростта ще може да извърши необходимото движение.
Скоростта се определя:
а) чрез измерване на скоростта на движение в отговор на определен сигнал чрез реакции на различни проекти;
б) по отношение на броя движения за определеното време, разтоварен крайник или торс в границите на определена амплитуда;
в) по отношение на преодоляването на накрая на кратко разстояние (например, работещ на 20, 30 m);
г) в скоростта на извършване на едно движение в сложно действие, като отблъскване в скокове, движението на раменния колан и ръцете в хвърляне, удари в бокса, първоначалното движение на бегача до къси разстояния, движения на Гимнаст и др.
Всички прояви на скоростта се развиват ефективно при игра на баскетбол. Можете също така да препоръчате ръчна топка, тенис на маса, движещи се игри с бързо променяне ситуацията на играта и бързо движение. Основната задача в повишаването на скоростта е, че спортистът не се специализира преждевременно във всяко упражнение на скорост, за да не се включва в голямо повторение на това упражнение. Ето защо е толкова важно, че атлетите да използват високоскоростни упражнения, е възможно по-често под формата на мач или игра. В програмата на класовете трябва да бъде в значително количество такива високоскоростни упражнения като спринт, като се движат от самото начало и от курса, работещи с ускорение, прескачане на дълга и височина с изключително бързо отблъскване, хвърляне на светли черупки, мобилни и спортни игри, изключително бързи акробатични упражнения и различни специални подготвителни упражнения.
Важно е да се повиши скоростта и повишаване на скоростта на движението има правилното определяне на дозата на високоскоростни упражнения. Тези от тях, които се изпълняват с максимална интензивност, са силно активни средства за бърза умора. Същото се отнася и за упражненията, насочени към повишаване на скоростта на движението. Следователно, упражненията, извършени с максималната скорост, трябва да се използват често, но в относително малък обем. Продължителността на интервалите за отдих се дължи на степента на възбудимост на централната нервна система и намаляване на показателите на вегетативни функции, свързани с премахването на кислородния дефицит. Обучението за развитие на скоростта трябва да бъде завършено веднага щом субективните чувства на спортиста или свидетелските показания на хронометъра ще покажат за намаляването на инсталираната или максималната скорост.
22.Биихимични основи на издръжливост на дългосрочни товари и начини за развитие
Издръжливостта е най-важното качество на двигателя, от което постигането на спортист е до голяма степен зависимо. Издръжливостта може да се определи като работно време с дадена сила преди появата на умора.
В съответствие с естеството на извършената работа, разпределяне на обща и специална издръжливост. Общата издръжливост отразява способността на спортист да извърши неспецифични натоварвания. Такива товари, например, за футболист може да бъде кръст, ски състезания, плуване, мобилни игри и др., Както и изпълнението на физическата работа на домакинството. Специална издръжливост характеризира работата на физическото натоварване, специфично за определен вид спорт и изискване технически, тактически и. \\ T психологическо обучение Спортист.
Нивото на развитие на молекулярни механизми за обучение на АТР - директен източник на енергия, за да се гарантира, че мускулната контракция и релаксация е от първостепенно значение
В зависимост от метода на енергийното снабдяване на извършената работа, се различава алактат, лактат и аеробна издръжливост. Често се използват термини. "Алактати, лактатни и аеробни издръжливи компоненти.
Алактатната издръжливост се характеризира с най-високото работно време в максималната зона на електроенергия. В зависимост от вида на товара, можете да подчертаете скоростта, скоростта на О-силата и мощността на издръжливостта. Основният източник на енергия за мускулна работа на максималната мощност е реакцията на креатин фосфат. Следователно развитието на алактатна издръжливост се дължи на интрамускулни запаси от креатин фосфат. Както вече бе отбелязано, белите мускулни влакна са по-богати на креатин фосфат. В това отношение мускулите с преобладаване на бели влакна имат по-голяма алактатна издръжливост. Съдържанието на креатин фосфат в мускулите може да бъде значително увеличено с помощта на специални упражнения. Принципът на изграждане на такова обучение в интервалния режим е описан по-горе, като се вземат предвид енергийните доставки на скоростните качества.
Биохимичната оценка на алактатната издръжливост може да бъде дадена чрез определяне на ежедневната селекция с креатининът на урината. Този индикатор характеризира общите резерви в креатин фосфатния организъм. Ръстът на алактатната издръжливост обикновено се придружава от увеличаване на ежедневното разпределение на креатинин. Друг критерий, характеризиращ се развитието на алактатна издръжливост, е амктатен дълг на кислород, измерен след завършване на работата на максималната мощност.
Лактатната издръжливост характеризира работата на физическото натоварване в зоната на субмаксималната сила. Основният източник на енергия при работа с такава сила служи като анаеробно разпадане на мускулен гликоген към млечна киселина, наречена гликолис. Възможностите на гликолития метод за получаване на АТЦ до голяма степен зависят от мускулните резерве за гликоген. Колкото по-високо е пречистването на концентрацията на гликоген в мускулите, толкова по-дълго ще се използва в гликолизма. Следва, че мускулите с преобладаване на бели богати на креатин фосфат и гликогенни влакна също са изразили лактатна издръжливост. Друг фактор, определящ лактатната издръжливост, е съпротивлението на мускулните клетки и целият организъм като цяло до увеличаване на киселинността, дължащо се на натрупването на лактат в мускулите и в кръвта.
Въз основа на такава зависимост от обучението, насочена към развитие на лактатна издръжливост, се изгражда, за да се гарантира изпълнението на две задачи. Първо, поради физическите натоварвания, извършени в мускулите, съдържанието на гликоген трябва да се увеличи. Второ, учебните класове трябва да доведат до резистентност към натрупването на лактат и увеличаване на киселинността.
За тази цел се използват упражнения, причиняващи, от една страна, значително изчерпване на мускулните гликоген резерви, което е предпоставка за последващата си суперкомпенсация, а от друга - водеща до образуването на големи количества млечна киселина. Такива са физическото натоварване на сукаксималната мощност, извършена в интервала или повтарящия се режим. Упражнението на този тип е описано по-горе, когато се има предвид енергийното снабдяване с високоскоростни качества. В зависимост от естеството на натоварванията на товарите е възможно главно да се развие основно мощност или високоскоростен компонент на лактатната издръжливост.
Водещият биохимичен показател за проявата на лактатната издръжливост по време на работа е натрупването на лактат в кръвта. Определянето на концентрацията на млечна киселина в кръвта се извършва след извършване на физическата работа на сукаксималната сила "на провал". Високо ниво Концентрациите на млечна киселина в кръвта показват използването на енергия по време на работа на големи количества мускулен гликоген и развитието на резистентност към киселинността.
Същата информация може да бъде получена чрез определяне на промяната в киселинно-алкалния баланс в кръвта след сукаксимални натоварвания. В този случай високата лактатна издръжливост съответства на значителна промяна на водородния индикатор на кръвта в киселата страна. Друг индикатор за развитието на лактатната издръжливост може да служи като лактатен кислороден дълг, измерен след функционирането на субмаксималната сила "на провал". Колкото по-висока е стойността на този показател, толкова по-голям е приносът на анаеробното разпадане на гликоген към енергийното снабдяване на извършената работа. Спортистите с добра физическа подготовка на величината на дълга на лактатния кислород могат да достигнат 18-20 литра.
В спортната практика много често и лактатната издръжливост се комбинира в анаеробна.
Аеробната издръжливост се изразява при извършване на дълги упражнения с умерена мощност, която се осигурява главно с енергия поради аеробно окисление. Приносът на анаеробното енергийно формиране е ограничен до първоначалния период на работа. В спортната литература, често под термина "издръжливост" означава, че аеробната издръжливост е предназначена.
Аеробната издръжливост се определя от три основни фактора: резерви в организма на наличните енергийни източници, доставка на кислород в работни мускули и развитие в работещи мускули на митохондриално окисление.
Като енергийни източници обикновено се използват въглехидрати, мастни киселини, кетонови тела и аминокиселини. Благодарение на дългата продължителност на аеробната работа, тези енергийни субстрати се доставят на мускулите с кръв, тъй като собствените си енергийни ресурси на мускулните клетки се изразходват в началото на работата.
При предоставянето на мускулни източници на енергия значителна роля принадлежи към черния дроб. Тук е, че по време на изпълнението на дълги натоварвания гликоген се дезинтегрира чрез глюкоза, която след това влиза в скелетни мускули и други органи, участващи в осигуряването на мускулна активност. Друг процес, който се среща в черния дроб по време на работа, окисление на мастни киселини, придружено от образуването на кетонови тела, които също са важни източници на енергия. В допълнение, други химични процеси, допринасящи за работата на мускулната работа по време на работа по време на работа. Във връзка с такава важна чернодробна роля за осигуряване на физическа работа в спортната практика се използват хепатопротектори - фармакологични агенти, които подобряват функционирането на черния дроб и ускоряват процесите на възстановяване в него.
Доставката на кислород в мускулите се извършва от сърдечна система. Следователно, за проявление на аеробната издръжливост, функционалното състояние на сърдечносъдовите и дихателните системи е изключително важно, кислородния капацитет на кръвта, поради броя на еритроцитите и съдържанието на хемоглобина в тях.
Развитието на аеробната издръжливост се определя до голяма степен от състоянието на нервното хормонално регулиране. Водещата роля в този регламент се извършва от надбъбречни жлези, изолирани към кръвта на катехолетинците и глюкокортикоидите - хормони, причиняващи преструктуриране на тялото, насочени към създаване на оптимални условия за мускулна активност. За проявление на аеробна издръжливост, способността на надбъбречните жлези за дълго време да се поддържа повишената концентрация на тези хормони в кръвния поток.
Интрамускулните фактори, отговорни за аеробната издръжливост, са размерът и броят на митохондриите - вътреклетъчни структури, в които участието на кислорода възниква синтеза на АТР, както и съдържанието на миоглобин-мускулен протеин, осигуряващ вътре в мускулните влакна на прехвърлянето на кислород до митохондрия. Както вече беше отбелязано, най-високото съдържание на митохондриите и моглобин се характеризира с червени мускулни влакна. Оттук следва, че по-висока аеробна издръжливост се наблюдава в мускулите с преобладаване на червени влакна.
Аеробна издръжливост, за разлика от анаеробната. Това се дължи на факта, че той до голяма степен се ограничава до различни еластични фактори: функционалното състояние на кардиореспирателната система, черния дроб и невро-хормоналното регулиране, кислородния капацитет на кръвта, запасите в организма на лесно достъпни енергийни източници. Ето защо, спортист, който има добро ниво на аеробна издръжливост, може да го покаже не само под формата на дейности, в които е преминала специализирано обучение, но и в други видове аеробни дейности. Например, квалифициран футболист може да покаже добър резултат В движение на дълги разстояния.
Многофакторността на аеробната издръжливост изисква използването на комплекс от различни продукти за обучение, тъй като всяка специфична професия, причинявайки достатъчно гъвкав ефект върху тялото, все още подобрява главно една от всяка страна на функционалността. В резултат на това обучението, насочено към развитието на аеробната издръжливост, следва да осигури подобряване на работата на системата на кардиоберез, за \u200b\u200bувеличаване на броя на еритроцитите в кръвта и съдържанието на хемоглобина в тях, увеличаването на концентрацията на миоглобина в мускулните клетки , най-доброто предоставяне на работни органи с енергийни субстрати.
За тази цел се прилагат различни възможности за обучение за повторно интервал, както и непрекъснато дългосрочна работа на еднакво или променлива сила.
Като пример за изграждане на обучителни сесии, насочени към развитието на аеробната издръжливост, може да бъде дадено така нареченото обучение на кръвоносните интервала. Този метод е редуващи краткосрочни упражнения за малка интензивност и издръжливост от 30 до 90 s с интервали от отдих със същата продължителност. Такава работа стимулира аеробното енергийно снабдяване на мускулната активност и води до подобрение в кардиореспирателната система.
За да се увеличи съдържанието в мускулите на миоглобина, може да се използва интервалното обучение на миоглобин. Атлетите се предлагат много кратки натоварвания със средна интензивност, редуват се със същите пропуски в късите отпадъци. Извършените краткотрайни товари са снабдени главно с кислород, който се отлага в мускулни клетки под формата на комплекс с миоглобин. Кратка почивка между упражненията е достатъчна за попълване на кислородните резерви.
За увеличаване на кислородния капацитет на кръвта, както и за увеличаване на концентрацията на миоглобин, се дава обучение в условията на средната планина.
Характеристиката на развитието на аеробната издръжливост е възможността за използване на неспецифични упражнения и предимно мобилни игри, което ви позволява да направите процес на обучение с различни и интересни.
Важна информация за оценка на аеробната издръжливост може да бъде получена чрез определяне на съдържанието и съотношението в кръвта на основните енергийни субстрати По време на изпълнението на дълга работа. В необузданите хора между съдържанието на глюкоза и продуктите за мобилизиране на мазнини има реципрочни връзки. Високата концентрация на глюкоза в кръвта възпрепятства мобилизирането на мазнини от депото. Ето защо, в невероятни хора, увеличаването на кръвното съдържание на мастни киселини, глицеринови и кетонови тела се наблюдава само на фона на намаляването на концентрацията на глюкоза. В атлетите, добре обучени в аеробния режим, на фона се наблюдава мощна мобилизация на мазнините, не само нормална, но и за повишено съдържание на кръвната захар. Увеличеното обезвреждане на мазнини и кетонови тела позволява на тялото не само да запази въглехидратите на черния дроб и кръвта, но и забавя консумацията на мускулен гликоген, намаление на концентрацията на която е един от факторите за развитието на умората.
В заключение следва да се отбележи, че всички компоненти на издръжливостта заедно с разглежданите по-горе енергия и структурни фактори са до голяма степен зависими от техническо, тактическо и психологическо обучение. Добро техническо обучение, правилно избрана тактика позволява на спортист икономически и рационално да използва енергийни резерви и по този начин да се запази ефективността. За сметка на висока мотивация, голямата сила на спортиста може да продължи да извършва работа дори при условията на възникване на значителни биохимични и функционални смени.
13.4.1. Реакциите на цикъла на Krebs се отнасят до третия етап на катабазата на хранителните вещества и се появяват в клетъчна митохондрия. Тези реакции се отнасят до общия път на катаболизма и са характерни за срутването на всички класове хранителни вещества (протеини, липиди и въглехидрати).
Основната функция на цикъла е окисляването на ацетиловия остатък с образуването на четири молекули на редуцирани коензими (три молекули Napn и една молекула FADN2), както и образуването на GTF молекулата чрез субстратно фосфорилиране. Въглеродните атоми на ацетиловия остатък се разпределят като две молекули на CO2.
13.4.2. Цикълът на Кребс включва 8 последователни етапа, като обръща специално внимание на реакцията на дехидрогениране на субстрат:
Фигура 13.6. Реакции на цикъла на Krebs, включително образуването на α-кетоглутарата
но) кондензация на ацетил CoA с оксалоацетатВ резултат на който се образува цитрат (фиг.13.6, реакция 1); Следователно цикълът на Krebs също се нарича цитратен цикъл. При тази реакция метил въглеродът на ацетиловата група взаимодейства с кето групата на оксалоацетат; В същото време има разделяне на Thio Ether Communication. COA-SH е освободена в реакцията, която може да участва в окислителния декарбоксилиране на следващата пируватна молекула. Карате реакцията citrantsintaza.Това е регулаторен ензим, инхибира се от високи концентрации на NAPN, сукцинил-СОА, цитрат.
б) трансформация на цитрат в изоцитрат чрез междинно образуване на цис-анитат. Цитратът, съдържащ в първата реакция на цикъла, съдържа третична хидроксилна група и не е в състояние да окислява при клетки. Под действието на ензима aconitase. Има разцепване на водна молекула (дехидратация), а след това неговото добавяне (хидратация), но по друг начин (фиг.13.6, реакция 2-3). В резултат на тези трансформации хидроксилната група се премества в положение, което води до последващо окисление.
в) изоцетрат дехидрогениране С последващото освобождаване на молекула CO2 (декарбоксилиране) и образуването на а-кетоглутарат (фиг. 13.6, реакция 4). Това е първата редукционна реакция в цикъла на Krebs, в резултат на което се образува. Изамоцитрат дехидрогеназа, катализираща реакция, е регулаторен ензим, ADP е активиран. Излишъкът потиска ензим.

Фигура 13.7. Реакции на цикъла на Krebs, започвайки с α-кетоглутарата.
д) окислителен декарбоксилиране на α-кетоглутарата, катализиран от комплекс MULTIMENZA (Фиг. 13.7, реакция 5) е придружен от освобождаването на СО2 и образуването на втората молекула. Тази реакция е подобна на реакцията на пируват дехидрогеназа. Инхибиторът служи на продукта на реакцията - сукцинил-СОА.
д) субстрат фосфорилиране На нивото на сукцинил-икономиката, по време на която енергията, освободена по време на хидролизата на тио естерната връзка, е под формата на GTF молекула. За разлика от окислителното фосфорилиране, този процес продължава без образуването на електрохимичния потенциал на митохондриалната мембрана (Фиг. 13.7, Реакция 6).
д) сукцинат дехидрогениране С образуването на фумаративни и FADN2 молекули (фиг. 13.7, реакция 7). Сукцинат дехидрогеназният ензим е здраво свързан с вътрешната мембрана на митохондриите.
ж) хидратация ФумаратаВ резултат на това в реакционната молекула се появява окислена хидроксилна група (фиг. 13.7, реакция 8).
з) дехидратиране малалат, което води до образуването на оксалоацетат и третата молекула на NADB (фиг.13.7, реакция 9). Оксалоацетатът, образуван в реакцията, може да се използва отново в реакцията на кондензацията със следващата ацетил-кола молекула (Фиг. 13.6, Реакция 1). Следователно този процес носи цикличен характер.
13.4.3. По този начин, в резултат на описаните реакции, пълно окисление Ацетилов остатък CH3 -. Броят на ацетил-СОА молекулите, трансформиран в митохондрия на единица време, зависи от концентрацията на оксалоацетат. Основните начини за увеличаване на концентрацията на оксалоацетат в митохондриите (съответните реакции ще бъдат разгледани по-късно):
а) карбоксилиране на пируват - свързване към пировата молекула на CO2 с цената на енергията на АТР; б) раздробяване или трансаминация на аспартат - разцепване на аминогрупата с образуването на кето група на негово място.13.4.4. Някои метаболити Crex цикли могат да се използват за синтез Структурни блокове за изграждане на сложни молекули. По този начин оксалоацетатът може да се превърне в аспартат аспирак и а-кетоглутат - глутамат в аминокиселината. Sukcinyl-CoA участва в синтеза на хем - протеза на хемоглобин. По този начин реакциите на цикъла на Krebs могат да участват както в процесите на катаболизма, така и в анаболизма, т.е. цикълът на Krebs изпълнява амфиболична функция (Вж. 13.1).
Въглехидратите, протеините и мазнините в тялото са хидролизирани и продуктите на хидролизата - монозахариди, аминокиселини, мастни киселини и глицерин са подложени на трансформации, през които част от тях се окисляват въглероден двуокис и вода, които са продукти от въглеродни и водородни окислителни продукти. Ако системата, в която всеки от продуктите за хидролиза на биополимери, който представлява субстрат за последващо окисление, ще има метаболитен път, тогава такава система ще бъде много тромавна и ненадеждна. Въпреки това, природата решава проблема за обединението на метаболитните пътеки, организирането на катаболни процеси по такъв начин, че при междинните етапи на тези процеси се образува минималният брой на същите метаболити, които се получават по време на окисляването на различни вещества. И наистина, както може да се види от схемата, по-голямата част от окислителните субстрати се превръщат в киселинна киселина - пируват (Сз) и след това в ацетил-прона (С2) и последният може да бъде оформен по време на окисление на пируват. Ацетил-СОА е напълно окислен в цикъла на трикарбоксилни киселини (CTC - това е цикълът на Krebs или цитратен цикъл). Цикълът на Krebs е често срещан по катаболен за въглехидрати, протеини и мазнини. Енергията, освободена по време на катаболните реакции, се разсейва частично чрез топлина, по-голямата част се консумира в анаболни реакции. Предаването на енергия се извършва с помощта на междинни съединения, основната част от тях е АТФ. Ендонерските процеси са синтез на аденосинтосфат (АТР) от аденозин информационен фосфат (ADP) и неорганичен фосфат, както и синтез и други вещества с макроенергични връзки. Този процес се дължи на сдвояването на енергия с катаболни реакции. Процесът на упражняване е хидролиза на АТР, както и други трифосфати. Хидролизата осигурява необходимата енергия за биосинтеза.
По-долу е схемата за сдвояване на анаболни и катаболни процеси:
S 1 окислен субстрат, ΔG< 0ADP + ATF + H 2OH, ΔG< 0
Констация
ATP + H2O → ADF + фосфат, ΔG< 0S 2 продукта биосинтеза, ΔG\u003e 0
По-голямата част от АТР в тялото се формира като резултат окислително фосфорилиранекойто се среща в електронната скорост на предаване (CPE). Основните субстрати на този процес са над * n и fad * H 2, които се образуват главно в ЦТК, така че една от основните задачи на катаболизма е синтеза на АТР - особена батерия на енергията, необходима за последващи реакции на анаболизъм. Повечето биосинтеза са намалени в природата, тъй като биосинтезните продукти са по-малко окислени в сравнение с източниците. Ролята на редуциращия агент в такива процеси се играе над * п. По този начин ключова роля в метаболизма принадлежи към ограничен брой връзки. Това е покуват и ацетил-СОА, веществата, които са завършени специфичните каболизъм; ATP, продукти за хидролиза, към която идва енергия за анаболни процеси; Над * n и fad * h 2 - съвместно, когато основната част на АТР в тялото се образува по време на окислението.
Катаболизъм на въглехидрати
Процесите на въглехидратните въглехидрати започват в устната кухина, тъй като съставът на слюнката включва амилазен ензим, който е способен да разцепи нишестето и гликоген към дизахарид - малтоза, който последният към глюкоза се разцепва от ензима. Потокът от глюкоза в клетките на различни органи зависи от инсулиновия хормон, който регулира скоростта на прехвърляне на глюкоза през клетъчните мембрани. Трансфери - протеини.
Обменът на глюкоза в клетката започва с фосфорилирането си:
Глюкоза + ATF Glucose-6-фосфат + ADP


ATP → + ADP
За разлика от свободната глюкоза, глюк-6-фосфатът не е в състояние да преминава през клетъчни мембрани, така че фосфорилирана глюкоза, както е, "заключена" в клетката и има под формата на гликоген - животинско нишесте, което се синтезира от глюкоза -6-фосфатни молекули.
Катаболизъм Глюкоза в клетка може да следва три основни посоки, които се различават по метода на промяна на въглеродния скелет на молекулата:
1. Дихотомична пътека, при която се получават разделяне на комуникация с C-C между третия и четвъртия въглеродни атоми и от една хексозна молекула, две триоза (от 6 → 2C3).
2. Апотомна пътека (пентозофосфат), в която хексинът се превръща в пентоза (С6 → С5) в резултат на окисление и разцепване на един (първи) въглероден атом.
3. Плъждащ път при окисляване и разцепване на шестия въглероден атом
Основното нещо в разпадането на глюкоза, което води до освобождаването на енергия, е дихотомичен път и по този начин, от своя страна, окислява глюкоза и получава своята енергия по два начина:
1. Независими анаеробно гниене Глюкоза до млечна киселина - glikoliz.
глюкоза → 2-лактат + 134 kJ
Част от тази енергия се изразходва за образуването на две aTF молекулиа останалото се разсейва под формата на топлина.
2.Аеробни (зависими от кислород) Глюкоза разпадането до въглероден диоксид и вода
Това е процесът на обратното фотосинтеза:
От 6 H 12O 6 + 6O 2 ↔ 6CO2 + 6N 2 O + 2850 kJ
60% от тази енергия се възпрепятства под формата на макроестегични връзки на АТР, т.е. в биологично достъпна форма. Както може да се види от горните уравнения, аеробният път е несъмнено по-печеливш в сравнение с гликолис, тъй като в него от същото количество глюкоза се образува през двадесет пъти повече АТР. Аеробният разпад се извършва от повечето телесни тъкани, с изключение на червените кръвни клетки. За злокачествени клетки основният начин за получаване на енергия е гликолизата. Мускулите се използват гликолиз в случай на големи натоварвания, когато достъпът до кислород е труден и се образува млечна киселина в голи мускули.
Реакционната верига на гликоларийната реакция на гликоларий включва единадесет реакции, от които първите десет - често с аеробно разпад, и единадесети са синтез на млечна киселина от растителна киселина (PVC), използвайки над * п. Помислете за реакцията в аеробното разпадане на глюкозата:
1 Реакцията е фосфорилиране на глюкоза, неговото активиране.
2 Реакцията е изомеризация, глюкозо-6-фосфатът се превръща в фруктоза-6-фосфат.
3 Реакция - фруктоза-6-фосфат фосфорилиран до фруктоза-1,6-дифосфат.
Първите три реакции са така нареченият подготвителен етап, на този етап все още има разходи за енергия на АТР при реакцията на фосфорилиране:
1Фосфат на глюкоза-6
2- Имомеризация
|
2-фосфоглицератор споделен път
9 H 2 ATF
Следващият етап е реакцията гликолетика Oxy подаванеКогато разпадането на скелет от шест въглерода се дезинтегрира от два три въглерода и окисляването им към пируват.
4 Реакцията - фруктоза-1,6-дифосфат в отворената си ациклична форма се разпада с алдолазен ензим в два три въглеродни фрагмента: глицералдехидфосфат и диоксиацетон фосфат.
5 Реакцията е изомеризация, превръщането на диоксиацетон фосфат в глицералдехидфосфат.
Допълнителен катаболизъм се появява само чрез глицералдехидфосфат, чиито молекули, от които в 6-та реакция се окисляват над + при 1,3-дитесфоглицератор, и енергията, пусната под формата на АТР. В този случай окисляването на алдехид води до анхидрид на органична и фосфорна киселина. Двата молекули от 1,3-дифосфаглицерат се превръщат в процес на хидролиза в 3-фосфоглицератор, а след това в 8-та реакция, фосфатната група се прехвърля от позиция 3 до позиция 2.
9 Реакцията се свързва с вода, за да се получи фосфонолируват и след това настъпва кето-енолат превръщането, конюгат с хидролиза, когато една молекула на фосфорна киселина и форма на енол се превръщат в кетоформа от диоксиацетонефосфат.
Катаболизъм Липид
При най-високите животни и лицето липидите влизат в стомаха и те я оставят почти отписани от кисела среда. При алкална среда на тънките черва липидите се хидролизират под действието на липази. Хидролизираните липиди се абсорбират в кръвта и се прехвърлят в различни органи за по-нататъшен метаболизъм.
В кръвта преминава през чревната стена на глицерин, LCD, моно- и диглицериди. В кръвта на LCD отново естерифицируема от глицерин, който е свързан с кръвни протеини и се прехвърля в мастна тъкан или черния дроб, където е отложено. В черния дроб има хидролиза с образуването на LCD, които се окисляват до С02 и Н20, голямо количество енергия се освобождава по време на окисление.
Процесът на окисление на LCD дисплея включва много етапи. LCD дисплеят се разрушава (синтезиран) до фрагменти С - С (естественият LCD се състои от четен брой въглеродни атоми). Когато катаболизмът, LCD дисплеят първо се превръща в тиоетери с коесантон А, с отделяне на АТР, след това се окислява в ненаситени киселини, окислителят служи като фазован.
От 15 часа 31 кокси - палмитинова киселина
За Хевско О.
CH3 (CH2) 12 CH2CH2C поша 3 (СН2) 2 СН2С2 с SCA
Ch2 (ch2) 12 ch \u003d sca sna
Пътят на катаболизма на протеините от хидролиза (протеолиза) започва под действието на протеаза и пептидазни ензими.
Хидролизата на протеините започва в стомаха под действието на ензима на пепсин, това допринася за кисела среда от стомашно рН \u003d 1-2, поради освобождаването на солна киселина стомашни клетки.
В тънките черва при рН \u003d 7.8-8.4, дезинтеграцията на протеините се катализира от трипсова и грабежи ензими.
AK - Продуктът на протеиновата хидролиза, идваща от стомашно-чревния тракт, е важен фонд за попълване на аминокиселинните резерви на клетки и тъкани. Ограниченото допускане отвън дори на един от незаменяемите пробив причинява рязко разлагане на собствени протеини на тъканите, AK се използва в синтеза на собствените си протеини, нуклеотиди, порфирини и др.
На ден възрастен е 100 g протеин. Протеините могат да бъдат пълни - в присъствието на всички незаменим AK и дефектни - няма всички необходими променлив ток. През деня 400 g протеин се разлага и синтезират. За 35 дни всички протеини се актуализират.
За състоянието на протеиновия обмен може да се прецени с азотен баланс. Тъй като протеините на органите се отличават със строги видове и тъканна специфичност, живият организъм има способността да използва протеина, прилаган само в хидролизирано състояние.
Абсорбцията на AK през мембраната на тънките черва настъпва под действието на глутатион. AK се записва в кръвта на носещата вена, след това в черния дроб, където се подлага трансформацията.