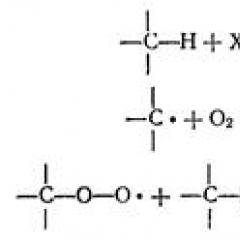
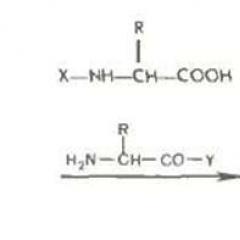
Примери за химически явления 8. "Физични и химични явления (химични реакции)
За последното 200 години човечеството Той проучи свойствата на веществата по-добре, отколкото в цялата история на развитието на химията. Естествено, количеството вещества също се увеличават, това се дължи преди всичко, с разработването на различни методи за получаване на вещества.
В ежедневието Ние сме изправени пред много вещества. Сред тях са вода, желязо, алуминий, пластмаса, сода, сол и много други. Вещества, които съществуват в природата, например кислород и азот, съдържащи се във въздуха, вещества, разтворени във вода и имат естествен произход, се наричат \u200b\u200bестествени вещества. Алуминий, цинк, ацетон, вар, сапун, аспирин, полиетилен и много други вещества в природата не съществуват.
Те се получават в лабораторията и произвеждат индустрия. Изкуствените вещества не са намерени в природата, те са създадени от естествени вещества. Някои вещества, съществуващи в природата, могат също да бъдат получени в химическа лаборатория.
Така че, когато нагрява манган, кислородът се освобождава и когато креда се нагрява - въглероден двуокис. Учените са се научили да превърнат графит в диамант, да отглеждат кристали рубин, сапфир и малахит. Така, заедно с вещества от естествен произход, има огромно разнообразие и изкуствено създадени вещества, които не са намерени в природата.
Веществата, които не са намерени в природата, се произвеждат в различни предприятия: фабрики, фабрики, комбайни и др.
В условията на изтощение природни ресурси Нашата планета, сега химикът е важна задача: да развиват и прилагат методи, с които е възможно изкуствено, в условията на лаборатория или промишлено производство, за получаване на вещества, които са аналози на естествени вещества. Например, запасите от изкопаеми горива в природата на резултата.
Може да дойде този момент, когато ще приключат петролът и природният газ. Новите видове горива вече са в ход, които биха били същите ефективни, но не замърсяват околен свят. Към днешна дата човечеството се е научило да получава изкуствено различни камъни, например, диаманти, изумруди, Берила.
Общото състояние на веществото
Веществата могат да съществуват в няколко агрегирани състояния, три от които знаете: твърд, течен, газообразен. Например, водата в природата съществува във всичките три съвкупни държави: Твърдо (под формата на лед и сняг), течна (течна вода) и газообразно (водна пара). Има вещества, които не могат да съществуват при нормални условия във всичките три съвкупни държави. Например, такова вещество е въглероден диоксид. При стайна температура това е газ без миризма и цвят. При температури -79 ° C Това вещество "замръзва" и преминава в твърдо вещество състояние на агрегацията. Вътрешно (тривиално) име на такъв "сух лед". Това име се дава на това вещество поради факта, че "сухият лед" се превръща в въглероден диоксид без топене, т.е. без преход към течно обобщено състояние, което присъства например във вода.
Така е възможно да се направи важно заключение. Веществото в прехода от едно съвкупно състояние в друго не се превръща в други вещества. Самият процес е определена промяна, трансформация, нарича явление.
Физически явления. Физични свойства на веществата.
Явленията, в които веществата променят съвкупното състояние, но не се превръщат в други вещества, наречени физически. Всяко отделно вещество има определени свойства. Свойствата на веществата могат да бъдат различни или подобни един на друг. Всяко вещество е описано с набор от физични и химични свойства. Помислете за вода като пример. Водата замръзва и се превръща в лед при температура от 0 ° C и кипи и се превръща в пара при температура + 100 ° С. Тези явления се отнасят до физически, тъй като водата не се превърна в други вещества, настъпи само промяна в съвкупното състояние. Данните за температурата на замръзване и кипене са физически свойства, характерни за водата.
Свойства на вещества, които определят измервания или визуално в отсъствието на трансформация на едно вещества в други, наречени физически
Изпаряване на алкохол като изпаряване на водата - физически явления, вещества с обща промяна на състоянието. След опит можете да се уверите, че алкохолът се изпарява по-бързо от водата, е физическите свойства на тези вещества.
Основните физични свойства на веществата включват следното: агрегат, цвят, мирис, водоразтворимост, плътност, точка на кипене, точка на топене, топлопроводимост, електрическа проводимост. Такива физични свойства като цвят, мирис, вкус, форма на кристали, могат да бъдат определени визуално, с помощта на сетива и плътност, електрическа проводимост, топене и точка на кипене се определят чрез измерване. O. Информация физически свойстваах много вещества се сглобяват в специална литература, например в справочници. Физическите свойства на веществото зависят от нейното съвкупно състояние. Например, плътността на лед, вода и водна пара е различна.
Газообразен кислород безцветен и течен син Познаването на физическите свойства помага за "разпознаване" много вещества. Например, мед - единственият метал на червено. Соленият вкус има само таблична сол. Йод - почти черно твърдо вещество, което, когато се нагрява в пурпурна пара. В повечето случаи е необходимо да се вземат предвид няколко свойства за определяне на веществото. Като пример, характеризират физичните свойства на водата:
- цвят - безцветен (в малък обем)
- мирис - без мирис
- общо състояние - при нормални условия, течност
- плътност - 1 g / ml,
- точка на кипене - + 100 ° С
- точка на топене - 0 ° C
- топлопроводимост - ниско
- електрическа проводимост - Чиста вода електричество не се извършва
Кристални и аморфни вещества
Когато се описват физичните свойства на твърдите вещества, е обичайно да се опише структурата на веществото. Ако смятате, че проба от готварска сол под лупа, може да се отбележи, че солта се състои от множество най-малки кристали. Може да се намерят и солни находища и много големи кристали. Кристали - твърди телас формуляр точно полихедра Кристалите могат да имат различна форма и размер. Кристали на някои вещества като готвене сол – крехки, те са лесни за унищожаване. Има кристали по-скоро твърдо. Например, диамантът се счита за един от най-трудните минерали. Ако разгледаме кристалите на табличната сол под микроскопа, може да се отбележи, че всички те имат подобна структура. Ако смятате, например, частици от стъкло, тогава всички те ще имат различна структура - такива вещества се наричат \u200b\u200bаморфен. Аморфните вещества включват стъкло, нишесте, кехлибар, пчелен восък. Аморфни вещества - вещества, които нямат кристална структура
Химически явления. Химическа реакция.
Ако с физически явления на вещества, като правило, променете само съвкупното състояние, след това в химически явления, превръщането на едно вещества в други вещества. Ние даваме няколко прости примера: Изгарянето на мача е придружено от символ на веригата и освобождаването на газообразни вещества, т.е. има необратимо превръщане на дървото в други вещества. Друг пример: С течение на времето бронзовите скулптури са покрити със зелен цвят. Факт е, че медът е включен в бронза. Този метал бавно взаимодейства с кислород, въглероден диоксид и въздушна влага, в резултат на повърхността на скулптурата се образуват нови зелени вещества. Химически явления - явления на трансформации на едно вещества в други Процесът на взаимодействие на вещества за образуване на нови вещества се нарича химическа реакция. Химическите реакции се появяват навсякъде около нас. Появяват се химични реакции в себе си. В нашето тяло, трансформациите на много вещества непрекъснато се появяват, веществата реагират помежду си, образувайки реакционните продукти. Така в химическата реакция винаги реагират вещества и вещества, образувани в резултат на реакцията.
- Химическа реакция - процесът на взаимодействие на веществата, в резултат на което се образуват нови вещества с нови свойства.
- Реагенти - вещества, влизащи в химическата реакция
- Продукти - вещества, образувани в резултат на химична реакция
Химическата реакция е изобразена в общ Реакционна схема Реагенти -\u003e Продукти
- реагенти - изходни вещества, взети за реакция;
- продукти - нови вещества, образувани в резултат на реакционния поток.
Всяко химично явление (реакция) е придружено от определени характеристики, с които химически явления могат да бъдат разграничени от физически. Такива признаци включват промяна на оцветяването на веществата, освобождаването на газ, образуването на утаяване, освобождаване на топлина, радиация на светлината.
Много химична реакция придружени от екскреция на енергия под формата на топлина и светлина. По правило такива явления са придружени от горещи реакции. В жарните реакции при въздушни вещества реагират с кислород, съдържащ се във въздуха. Например, метални магнезий мигат и изгарят в ярък ослепящ пламък. Ето защо избухването на магнезий се използва при създаването на снимки през първата половина на ХХ век. В някои случаи енергията е възможна под формата на светлина, но без изолиране на топлинна енергия. Един от видовете тихоокеански планктон може да излъчва ярка синя светлина, добре забележим в тъмното. Освобождаването на енергия под формата на светлина е резултат от химическа реакция, която протича в организмите на този тип планктон.
Ляв резултат:
- Има две големи групи вещества: вещества от естествен и изкуствен произход
- При нормални условия веществата могат да бъдат в три агрегати.
- Свойства на вещества, които определят измервания или визуално в отсъствието на трансформация на едно вещества в други, наречени физически
- Кристали - твърди тела, имащи форма на правилна полихедра
- Аморфни вещества - вещества, които нямат кристална структура
- Химически явления - явления на трансформации на едно вещества в други
- Реагенти - вещества, които влизат в химическа реакция
- Продукти - вещества в резултат на химическа реакция
- Химичните реакции могат да бъдат придружени от освобождаване на газ, утаяване, топлина, светлина; Чрез промяна на цвета на веществата
- Горенето е сложен физико-химичен процес на преобразуване на първоначалните вещества в горивни продукти по време на химическа реакция, придружена от интензивно освобождаване на топлина и светлина (пламък)
Физическите промени не са свързани с химични реакции и създаването на нови продукти, като топене на лед. Като правило такива трансформации са обратими. В допълнение към примери за физически явления, в природата и в ежедневието, се срещат и химически трансформации, в които се образуват нови продукти. Такива химични явления (примери ще бъдат разгледани в статията) са необратими.
Химични промени
Химичните промени могат да се разглеждат като всяко явление, което позволява на учените да измерват химични свойства. Много реакции също са примери за химически явления. Въпреки че не винаги е лесно да се каже какво е настъпила химическата промяна, има някои контролни знаци. Какво е химически явления? Даваме примери. Тя може да бъде промяна в цвета на веществото, температурата, образуването на мехурчета или (в течности) утаяване. Може да се дават следните примери за химични явления в живота:
- Ръжда на жлеза.
- Горещо дърво.
- Метаболизъм храна в тялото.
- Смесване на киселина и алкали.
- Готвене яйца.
- Храносмилане на захарна амилаза при слюнка.
- Смесване при печене на сода и оцет за производство на газообразен въглероден диоксид.
- Печене на пай.
- Галванизация на метал.
- Батерии.
- Фойерверки експлозия.
- Гниене банани.
- Образуването на млечни киселинни продукти.
И това не е целият списък. Можете да помислите за по-подробно някои от тези елементи.

Външен огън с дърво
Огънят - Това е и пример за химическия феномен. Това е бързо окисление на материала в екзотермичния химичен процес на изгаряне, освобождаването на топлина, светлина и различни реакционни продукти. Пожарът е горещ, защото има превръщане на слаба двойна връзка в молекулен кислород O 2 до по-силни връзки в изгарянето на въглероден диоксид и вода. Различава се високата енергия (418 KJ на 32 гр 2); Комуникация на горивата енергия играе само средна роля тук. В определена точка, реакцията на изгаряне, наречена запалвателна точка, образува пламък.
Това е видимата част на огъня, която се състои главно от въглероден диоксид, водна пара, кислород и азот. Ако температурата е достатъчно висока, газовете могат да станат йонизирани за получаване на плазма. В зависимост от това кои вещества светват и какви примеси се сервират навън, цвета на пламъка и интензивността на огъня ще бъдат различни. Пожарът в най-често срещаната му форма може да доведе до пожар, който може да причини физически щети по време на изгаряне. Пожарът е важен процес, който засяга екологичните системи по целия свят. Положителните ефекти на пожар включват стимулиране на растежа и поддържане на различни екологични системи.
Ръжда
Точно като огъня, ръждясващият процес също е окислителен процес. Това просто не е толкова бързо. Ръждата е железен оксид, обикновено червен оксид, образуван от окислителната и редукционна реакция на желязо и кислород в присъствието на вода или въздух. Няколко форми на ръжда се различават както по визуална, така и в спектроскопия, така и в различни обстоятелства. Като се има предвид достатъчно време, кислород и вода, всяко желязо, което в крайна сметка напълно се превръща в ръжда и се разлага. Неговата повърхностна част е обелване и разхлабена, и не защитава основното желязо, за разлика от образуването на патина върху медни повърхности.
Такъв пример за химическия феномен като ръжда генерал За корозия на желязо и нейните сплави, като стомана. Много други метали са подложени на подобна корозия, но получените оксиди обикновено не се наричат \u200b\u200bръжда. Има и други форми на тази реакция в резултат на реакцията между желязото и хлорида в средата, лишени от кислород. Пример за това е фитингите, използвани в подводни бетонови стълбове, които генерират зелена ръжда.

Кристализация
Друг пример за химическия феномен е кристален растеж. Този процес, при който съществуващият кристал става по-голям, тъй като броят на молекулите или йони се увеличава на техните позиции в кристалната решетка. Кристалът се дефинира като атоми, молекули или йони, разположени в поръчана повтаряща се проба, кристална решетка, разпространяваща се във всичките три пространствени размера. По този начин, растежът на кристалите се различава от растежа на капка течност, тъй като по време на растежа на молекулата или йони трябва да попаднат в правилните позиции на решетката, така че поръчаният кристал може да расте.

Когато молекулите или йони попадат в позиция, различна от позициите в идеална кристална решетка, се образуват кристални дефекти. По правило, молекули или йони в кристална решетка се проследяват в смисъл, че не могат да се движат от своите разпоредби, и следователно растежът на кристалите често е необратим, тъй като когато молекулите или йони се намират в нарастваща решетка, те са фиксирани в него. Кристализацията е обичайният процес както в индустрията, така и в естествен святИ кристализацията обикновено се разбира като състояща се от два процеса. Ако кристалът не съществува по-рано, тогава трябва да се роди новият кристал, а след това трябва да бъде изложен на растежа.

Химически произход на живота
Химичният произход на живота принадлежи към условията, които биха могли да съществуват и следователно допринесоха за появата на първите дублирани форми на живот.

Основният пример за химически явления в природата е самият живот. Смята се, че комбинацията от физически и химични реакции е в състояние да доведе до появата на първите молекули, които, възпроизвеждането, доведе до появата на живота на планетата.
Светът около нас, с цялото си богатство и разнообразие, живее според законите, които са лесни за обяснение с помощта на физиката и химията. И дори в сърцето на жизнената дейност на такъв сложен организъм, като човек, това не е нищо повече от химични явления и процеси.
Определения и примери
Елементарен пример - чайник, доставен на огън. След известно време водата ще започне да се нагрява, след това да заври. Ще чуем характерно съскане, машините на двойката ще летят от шията на чайника. Откъде идва той, защото в ястията първоначално не е! Да, но водата, при определена температура, започва да се превръща в газ, променя физическото си състояние от течност до газообразно. Тези. Оставаше цялата вода, само сега под формата на двойка. то
И ще видим химически явления, ако спуснем чаената чанта в кипяща вода с чаена. Водата в чаша или друга съда е боядисана в червено-кафяв. Ще се появи химическа реакция: под влиянието на топлината на чанките ще започне да се използва, подчертавайки цветните пигменти и ароматизиращите свойства, присъщи на това растение. Ще имаме ново вещество - питие със специфични, характерни за него само с висококачествени характеристики. Ако там има няколко захарни лъжици, тя ще се разтвори (физическа реакция), а чайът ще стане сладка по този начин, а физическите и химичните явления често са свързани и взаимозависими. Например, ако е поставена същата чанта за чай студена водаРеакцията няма да се случи, паулците и водата няма да взаимодействат, а захарта също няма да се разтвори.
По този начин, химичните явления са такива, при които някои вещества се превръщат в други (вода в чай, вода в сироп, дърва за огрев в Аша и др.) В противен случай химическият феномен се нарича химическа реакция.
Физически са явленията, в които химичен състав Веществата остават същите, но промените в процеса на тялото, форма и т.н. (Деформираната пролет, вода, замръзнала в леда, дърво, счупена наполовина).
Условия за възникване и поток
Дали се появяват химични и физични явления, можем да преценим с някои характеристики и промени, които се наблюдават в дадено тяло или вещество. Така че повечето химични реакции са придружени от следните "идентификационни знаци":
- в резултат или по време на потока, утайката пада;
- има промяна в цвета на веществото;
- може да бъде освободен газ, например, въглероден оксид;
- възниква абсорбция или напротив, освобождаването на топлина;
- възможно е излъчването на светлината.
Така че да се наблюдава химически явления, т.е. Възникнаха реакции, някои условия са необходими:
- реагиращите вещества трябва да влязат в контакт, да бъдат един с друг в контакт (т.е., същото заваряване трябва да се излива в кръг с вряща вода);
- веществата са по-добре смилане, след това реакцията ще тече по-бързо, по-скоро взаимодействието (захарният пясък по-скоро ще се разтвори, се топи в гореща вода, отколкото бучка);
- така че могат да възникнат много реакции, трябва да промените температурния режим на реакционните компоненти, охлаждането или нагряването им до определена температура.
Възможно е да се спазва химическото явление по опит. Но за да го опиша на хартия с помощта на химическа реакция).
Някои от тези условия също работят за появата на физически явления, например промяна в температурата или пряк контакт на обектите, тела помежду си. Да предположим, ако ударите много силен чук по шапка за нокти, тя може да деформира, губи обичайната си форма. Но тя ще остане шапка за нокти. Или, когато електроматът е включен в мрежата, волфрамовата нишка вътре ще започне да се затопли и светят. Въпреки това, веществото, от което се прави нишката и ще остане същата волфрам.
Описанието на физическите процеси и явления се извършва чрез физически формули, решаване на физически проблеми.
Изпратете добрата си работа в базата знания е проста. Използвайте формата по-долу
Студентите, завършилите студенти, млади учени, които използват базата на знанието в обучението и работата ви, ще ви бъдат много благодарни.
Публикувано от http://www.allbest.ru/
Zaporizhia. общообразователно училище І-ІІІ стъпки номер 90
Химически явления в ежедневието и ежедневието
Ученик от 7-ми клас
Дмитрий Балуеев
Въведение
окисление за химическа реакция
Светът около нас, с цялото си богатство и разнообразие, живее според законите, които са лесни за обяснение с помощта на физиката и химията. И дори в сърцето на жизнената дейност на такъв сложен организъм, като човек, това не е нищо повече от химични явления и процеси.
Със сигурност не сте забелязали нищо подобно на сребърния пръстен на майката с времето по-тъмни. Или колко ръждя нокът. Или как да изгаря дървени лампи в пепел. Но дори ако майка ви не харесва среброто, и в пешеходен туризъм никога не сте отишли, как чантата е свалена в чаша, която сте видели сигурни.
Какво е общо за всички тези примери? И факта, че всички те се отнасят до химически явления.
Така че най-често срещаните примери за химически явления в живота и ежедневието:
ръждясване на ноктите
гориво изгаряне
загуба на утайка
триене на гроздов сок
кест гниене
синтез на спиртни напитки
щети сребърни обеци
появата на зелена плака на бронз
скрининг в котли
боже сода мрачно
сладуращо месо
изгаряне на хартия
Искате ли за подробности? Елементарен пример - чайник, доставен на огън. След известно време водата ще започне да се нагрява, след това да заври. Ще чуем характерно съскане, машините на двойката ще летят от шията на чайника. Откъде идва той, защото в ястията първоначално не е! Да, но водата, при определена температура, започва да се превръща в газ, променя физическото си състояние от течност до газообразно. Тези. Оставаше цялата вода, само сега под формата на двойка. Това е физическо явление.
И ще видим химически явления, ако спуснем чаената чанта в кипяща вода с чаена. Водата в чаша или друга съда е боядисана в червено-кафяв. Ще се появи химическа реакция: под влиянието на топлината на чанките ще започне да се използва, подчертавайки цветните пигменти и ароматизиращите свойства, присъщи на това растение. Ще имаме ново вещество - питие със специфични, характерни за него само с висококачествени характеристики. Ако там има няколко захарни лъжици, разтваря се (физическа реакция) и чай ще стане сладка (химическа реакция). Така, физичните и химичните явления често са свързани и взаимозависими. Например, ако същата чаена торба е поставена в студена вода, реакцията няма да се случи, паулките и водата няма да взаимодействат, а захарта се разтваря или не желае.
По този начин, химичните явления са такива, при които някои вещества се превръщат в други (вода в чай, вода в сироп, дърва за огрев в Аша и др.) В противен случай химическият феномен се нарича химическа реакция.
За това дали възникват химически явления, можем да преценим с някои характеристики и промени, които се наблюдават в дадено тяло или вещество. Така че повечето химични реакции са придружени от следните "идентификационни знаци":
в резултат или по време на потока, утайката пада;
има промяна в цвета на веществото;
може да бъде освободен газ, например, въглероден оксид;
възниква абсорбция или напротив, освобождаването на топлина;
възможно е излъчването на светлината.
Така че да се наблюдава химически явления, т.е. Възникнаха реакции, някои условия са необходими:
реагиращите вещества трябва да влязат в контакт, да бъдат един с друг в контакт (т.е., същото заваряване трябва да се излива в кръг с вряща вода);
веществата са по-добре смилане, след това реакцията ще тече по-бързо, по-скоро взаимодействието (захарният пясък по-скоро ще се разтвори, се топи в гореща вода, отколкото бучка);
така че могат да възникнат много реакции, трябва да промените температурния режим на реакционните компоненти, охлаждането или нагряването им до определена температура.
Възможно е да се спазва химическото явление по опит. Но е възможно да се опише на хартия, използвайки химическо уравнение (уравнение на химичното реакция).
Някои от тези условия също работят за появата на физически явления, например промяна в температурата или пряк контакт на обектите, тела помежду си. Да предположим, ако ударите много силен чук по шапка за нокти, тя може да деформира, губи обичайната си форма. Но тя ще остане шапка за нокти. Или, когато електроматът е включен в мрежата, волфрамовата нишка вътре ще започне да се затопли и светят. Въпреки това, веществото, от което се прави нишката и ще остане същата волфрам.
Но нека да разберем още няколко примера. В края на краищата всички ние разбираме, че химията се извършва не само в тестовите тръби в училищната лаборатория.
1. Химически явления в ежедневието
Те включват тези, които могат да бъдат наблюдавани в ежедневието модерен човек. Някои от тях са напълно прости и очевидни, всеки може да ги наблюдава в кухнята си като пример с приготвящ чай.
Използвайки примера на силен (концентриран) чай за заваряване, можете да провеждате още един опит самостоятелно: озарявайте чая с помощта на лимона. Благодарение на киселините, съдържащи се в лимонов сок, течността отново ще промени състава си.
Какви други явления можете да наблюдавате в ежедневието? Например, химичните явления се отнасят до процеса на изгаряне на гориво в двигателя.
Ако опростите, реакцията на горивната горива в двигателя може да бъде описана, както следва: кислород + гориво \u003d вода + въглероден диоксид.
Като цяло, има няколко реакции във вътрешната камера на горенето, при които участват гориво (въглеводороди), въздушни и искра. Или по-скоро, не само гориво - горивото и въздушната смес от въглеводороди, кислород, азот. Преди запалване сместа се компресира и нагрява.
Изгарянето на сместа се осъществява в фракцията от секунда, в резултат на това връзката между атомите на водород и въглерод се унищожава. Това се освобождава голям брой Енергия, която води до движението на буталото, а този е коляновият вал.
В бъдеще се образуват водород и въглеродни атоми с кислородни атоми, се образуват вода и въглероден диоксид.
В идеалния случай реакцията на горивната горива трябва да изглежда така: CNH2N + 2 + (1.5N + 0.5) O2 \u003d NCO2 + (N + 1) H2O. В действителност двигателите с вътрешно горене не са толкова ефективни. Да предположим, ако кислородът не е достатъчно, когато реакцията е леко, в резултат на реакцията, се образува СО. И с по-голяма липса на кислород се образува сажди (c).
Образуването на плака върху металите в резултат на окисление (ръжда върху жлезата, патина върху мед, потъмняване на сребро) - също от категорията химически явления за домакинството.
Вземете например желязо. Ръжда (окисление) се появява под влиянието на влага (влажност, пряк контакт с вода). Резултатът от този процес става хидроксид на FE2O3 (по-точно Fe2O3 * H2O). Можете да го видите под формата на свободна, груба, оранжева или червено-кафява плака на повърхността на метални изделия.
Друг пример може да служи като зелена плака (патина) върху повърхността на мед и бронзови продукти. Той се формира с течение на времето под влияние на атмосферния кислород и влажност: 2CU + O2 + H2O + CO2 \u003d CU2CO5H2 (или CUCO3 * CU (OH) 2). Полученият основен карбонатен мед е намерен в природата - под формата на малахитни минерали.
И още един пример е бавен окислителна реакция Метал във вътрешни условия е образуването на тъмна сол на Ag2S сребърен сулфид върху повърхността на сребърните продукти: бижута, прибори за хранене и др.
"Отговорността" за неговото възникване носят частици сяра, които под формата на сероводород се намират във въздуха, които дишаме с вас. Среброто може да DARKE със серни хранителни продукти (например яйца). Реакцията изглежда така: 4AG + 2H2S + O2 \u003d 2AG2S + 2H2O.
Да се \u200b\u200bвърнем в кухнята. Тук можете да помислите за някои по-любопитни химически явления: образуването на мащаб в чайника е един от тях.
В условията на живот няма химически чиста вода, тя винаги се разтваря в различни концентрации на метали и други вещества. Ако водата е наситена с калциеви и магнезиеви соли (въглеводородни), то се нарича трудно. Колкото по-висока е концентрацията на солите, толкова по-твърда е водата.
Когато такава вода се нагрява, тези соли са изложени на въглероден диоксид и неразтворима утайка (SAS3 IMGS3). Можете да гледате тези твърди депозити, като погледнете чайника (както и да гледате нагревателните елементи на миене и съдомиялни машини, ютии).
В допълнение към калций и магнезий (от която се получава карбонатна скала), желязото често присъства във вода. По време на химичните реакции на хидролиза и окисление от него се образуват хидроксиди.
Между другото, чрез събиране, за да се отървете от мащаба в чайника, можете да наблюдавате друг пример за забавна химия в ежедневието: обичайният оцет на масата и лимонената киселина се справят с депозитите добре. Чайник с разтвор на оцет / лимонена киселина и вода се варя, след което скалата изчезва.
И без различен химически феномен, няма да има вкусни пайове и кифлички: ние говорим за газовия оцет.
Когато мама напусна сода в лъжица оцет, тази реакция се появява: NaHC03 + CH3COOH \u003d CH3COONA + H2O + CO2. Въглеродният диоксид, произтичащ от резултата, се стреми да напусне тестото - и по този начин променя структурата си, прави порести и свободни.
Между другото, можете да кажете на майка ми, че не е необходимо да угасват содата - тя ще реагира, когато тестото влезе във фурната. Реакцията обаче ще се случи малко по-лошо, отколкото с гасене на сода. Но при температура от 60 градуса (и по-добра от 200), сода разлагане върху натриев карбонат, вода и целия същия въглероден диоксид. Вярно е, че вкусът на готовите пайове и кифлите може да бъде по-лош.
Списъкът на химическите явления за домакинството е не по-малко впечатляващ от списък на такива явления в природата. Благодарение на тях имаме пътища (производството на асфалт е химически феномен), у дома (тухлено), красиви кърпи за облекло (оцветяване). Ако мислите за това, става ясно ясно колко многостранно и интересна наука химия. И колко полза може да бъде научена от разбирането на нейните закони.
2. Интересни химически явления
Бих искал да добавя малко интерес. Сред много и много хора, изобретен от природата, и явленията на мъжа са специални, което е трудно да се опише и обяснява. Те включват изгаряне на вода. Като такъв, може би питате, защото водата не свети, огънят го гаси? Как може да изгори? И това е какво.
Изгарянето на вода е химически феномен, при който във вода със соли под влияние на радиовълни от кислородни водородни връзки. В резултат се образуват кислород и водород. И горящи, разбира се, не самата вода, а от водород.
В същото време тя достига много висока температура на горене (повече от половин хиляди градуса), плюс водата отново се образува по време на реакцията.
Това явление отдавна се интересува от учените, които мечтаят да се научат как да използват водата като гориво. Например, за автомобили. Макар че това е нещо от областта на художествената литература, но кой знае, че учените ще могат да измислят много скоро. Един от основните улов е, че с изгарянето на енергия на енергия, повече от реакцията се изразходва.
Между другото, нещо подобно може да се наблюдава в природата. Според една от теориите, големи самотни вълни, които изглеждат от никъде, всъщност са следствие от експлозия на водород. Електролизата на водата, която води до нея, се извършва чрез въвеждане на електрически разряди (светкавица) към повърхността на солената вода на моретата и океаните.
Но не само във вода, но и на земята можете да наблюдавате сими химически явления. Ако имате възможност да посетите естествената пещера, вероятно можете да видите странните, красиви естествени "ледени висулки", висящи от тавана - сталактити. Начинът и защо се появяват, се обяснява с друг интересен химически феномен.
Химс, гледащ сталатит, вижда, разбира се, не е качивал, но калциев калциев карбонат. Основата за неговото образуване е отпадъчната води, естествения варовик, а самият сталактит е построен поради утаяването на калциев карбонат (растеж на надолу) и силата на адхезията на атомите в кристалната решетка (WSHRING растеж).
Между другото подобни образувания могат да се издигнат от пода до тавана - те се наричат \u200b\u200bсталагмити. И ако сталактитите и сталагмитите се срещат и растат в цели колони, те получават името на скобите.
Заключение
Има много невероятни, красиви, както и опасни и плашещи химически явления дневно в света. На много хора се научиха да се възползват: създава строителни материалиПодготовка на храна, прави транспорта да се премества на огромни разстояния и много други.
Без много химически явления ще има евентуално съществуване на живота на земята: без озоновия слой, хората, животните, растенията няма да оцелеят поради ултравиолетови лъчи. Без фотосинтеза на растенията, животните и хората няма да имат нищо за дишането и без химически реакции на дишане, този въпрос изобщо не би бил от значение.
FINY ви позволява да приготвите храна, а химичното явление на гниене разлагате протеини в по-прости съединения и връщат тези в цикъла на вещества в природата.
Образуването на оксид при отопление на мед, придружено от ярко блясък, изгаряне на магнезий, топене на захар и др. Също така обмисля химически явления. И те намират полезна употреба.
Публикувано на AllBest.ru.
...Подобни документи
Проблемът със смъртта на хората в пожарите е въпрос на специална загриженост. Определение за пожарна безопасност, основни функции на нейната система за сигурност. Причини и източници на пожари в производството. Пожарна безопасност в ежедневието. Събития за предотвратяване на пожар.
резюме, добавено 02/16/2009
Причини за пожари в ежедневието и основните правила за пожарна безопасност. Правила за обработка на газови и газови уреди. Пушенето в леглото е една от основните причини за пожарите в апартаментите. Мерки за гасене на пожар, евакуация на хора и собственост преди пристигането на пожарната единица.
резюме, добавен 01/24/2011
Същността на психиката, физическата и социалната сигурност на детето. Правила безопасно поведение Деца в ежедневието пътник Пешеходно и пътническо превозно средство. Методи за формиране на внимателно отношение към потенциално опасни ситуации.
курсова работа, добавена 24.10.2014
Концепцията за социално-опасни явления и причините за тяхното възникване. Бедност в резултат на намаляване на жизнения стандарт. Глад в резултат на недостиг на храна. Криминализиране на обществото и социалната катастрофа. Начини за защита срещу социално опасни явления.
изследване, добавено 05.02.2013
Разглеждане на характеристиките на развитието на пожари, започващи с етапа на изгаряне. Основните признаци на огън от източник на запалване с ниска мощност. Изучаване на версията на появата на пожар в резултат на производството на самостоятелни процеси.
презентация, добавена 09/26/2014
Електротраматизъм в производството и в ежедневието. Ефектите на електрическия ток върху човешкото тяло. Електричество. Условия за поражение токов удар. Технически методи и средства за електрическа безопасност. Оптимизиране на защитата в разпределителните мрежи.
резюме, добавен 04.01.2009
Причинява и възможни последици от пожари. Основни фасади: изгаряне, огън, запалване. Методи за гасене на пожар. Класификация на средствата и характеристиките на фламестерите. Основни мерки за пожарна безопасност в ежедневието и първа помощ.
есе, добавено 04/04/2009
Определяне на концепциите и видовете опасни хидрологични явления. Запознаване с историята на най-много ужасни наводнения. Описание на опустошителните цунами. Причини и последици от лимбия катастрофа. Механизмът на образуване и сила на потоците седна.
презентация, добавена 22.10.2015
Причини за появата, степента и основните признаци на химически изгаряния. Характеристики на химически изгаряния, хранопровода и стомаха. Правила за работа с киселини и алкали. Първа помощ при получаване на химическо изгаряне. Превантивни мерки на химически изгаряния.
добавено е изследване 05/14/2015
Видове домакински инциденти, причините за тяхното възникване. Отравяне с почистване и препарат, първа помощ. Превенция на хранително отравяне. Изтичане на газ в апартамента. Основни вещества в кипящи течности. Мерки предупреждават изгаряния.